3. PHYSIOLOGISCHE WIRKUNG DES ARABINOXYLANDERIVATS AUS REISKLEIE (Biobran)
3.1 Immun-REGULATION
(a) Erhöhung der Aktivität der menschlichen NK-Zellen mithilfe modifiziertem Arabinoxylan
aus Reiskleie (Biobran MGN-3)
1. 1. In vitro Test
NK-Zellen einer Ratte wurden unter Anwesenheit von Biobran MGN-3 mit Tumorzellen K-562
inkubiert und nachfolgend wurde mit 51Cr-Separationstest die Menge der zerlegten
K-562-Zellen gemessen. Eine erhöhte Konzentration der zerlegten Zellen wurde in Abhängigkeit
von der Biobran MGN-3 Konzentration (die 25 µg/ml, resp. 100 µg/ml betrug), gemessen. Dies
bestätigte, dass der Anstieg der NK-Zellen-Aktivität vom Mittel Biobran MGN-3 verursacht
wurde.
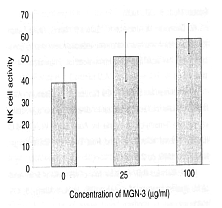 Legende: Aktivität der NK-Zellen > Konzentration MGN-3 (µg/ml)
Legende: Aktivität der NK-Zellen > Konzentration MGN-3 (µg/ml)
2. In vivo Test (an Ratten)
Biobran MGN-3 wurde oral Ratten Sprague-Dawley verabreicht und nach zwei Wochen die
Aktivität der NK-Zellen gemessen. Die Ratten wurden zu fünft mit verabreichten Dosen 0,5 mg,
5 mg, resp. 50 mg/kg/ täglich in drei Gruppen geteilt. In Abhängigkeit von der verabreichten
Dosis Biobran MGN-3 wurde eine erhöhte Aktivität der NK-Zellen verzeichnet. In den Gruppen
mit Dosen 0,5 mg, 5 mg und 5 mg erhöhte sich diese Aktivität gegenüber der Kontrollgruppe um
119 %, 130 %, resp. 142 %. In der Gruppe mit Dosis 50 mg erreichte die Aktivität schon nach
drei Tagen Einnahme das Niveau 132 % gegenüber der Kontrollgruppe. Der, durch das Mittel
Biobran MGN-3 verursachte Anstieg der NK-Zellen-Aktivität kann der erhöhten
Vernichtungskraft der NK-Zellen zugeschrieben werden, ist aber gleichzeitig auch von der
Gesamtanzahl der NK-Zellen abhängig. Es wurde ein Wirkungsunterschied bei Männchen und
Weibchen beobachtet, dabei war die Wirkung bei Weibchen intensiver (Abb. 3).
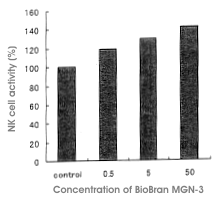 Legende: Aktivität der NK-Zellen (%) > Konzentration BioBran MGN-3
Legende: Aktivität der NK-Zellen (%) > Konzentration BioBran MGN-3
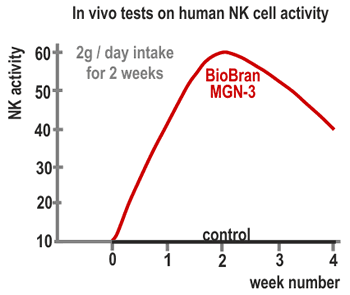
3. Wirkung auf Menschen
Im Rahmen der Teste der Wirkung von Biobran MGN-3 auf Menschen mit 24 Gesunden (15 Frauen
und 9 Männern mit Durchschnittsalter 34 Jahre) wurde das Mittel ununterbrochen 60 Tage
verabreicht und dabei die Aktivität der NK-Zellen beobachtet. Die Teilnehmer wurden in 3
Gruppen mit jeweils 8 Personen mit Tagesdosen 15 mg/kg, 30 mg/kg, resp. 45 mg/kg
Körpergewicht geteilt. Jedem Teilnehmer wurde eine Blutprobe (20 ml) vor Einnahme des
Mittels, nach einer Woche, nach einem Monat, nach zwei Monaten (nach Abschluss der Einnahme)
und einen Monat nach Abschluss der Einnahme entnommen und die Aktivität der NK-Zellen
gemessen. In den Gruppen mit Dosis 30 mg und 45 mg stieg die Aktivität der NK-Zellen eine
Woche nach Einnahmebeginn auf das Doppelte und nach zwei Monaten auf das Dreifache. In den
Gruppen mit Dosis 15 mg stieg die Aktivität der NK-Zellen rapid nach einem Monat Einnahme
und erreichte nach zwei Monaten fast das gleiche Niveau wie in den Gruppen 30 mg und 45 mg.
Ein Monat nach Einnahmeabschluss kehrte die Aktivität der NK-Zellen auf das Niveau vor dem
Test zurück (Abb. 4). Diese Ergebnisse deuten an, dass die Aufnahme von 15 - 45 mg/kg
Biobran MGN-3 täglich eine reale Auswirkung auf die Aktivität der menschlichen NK-Zellen
hat.
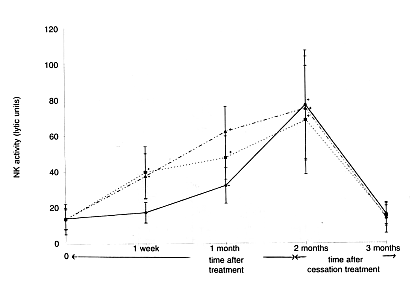
Abb. 4: Zeit- und Dosisabhängigkeit der NK-Zellen-Aktivität mit Biobran
MGN-3 gegenüber
Tumorzellen K562…_.._.._.._ = 45mg/kg/täglich; …………=30mg/kg/täglich; _______=15mg/kg/täglich
4. 4. Wirkungsmechanismus des Mittels Biobran MGN-3 auf die NK-Zellen
Beide Teste, in vitro und in vivo, bestätigten, dass sich die Menge der zytotoxischen
Granula in den mit Biobran MGN-3 stimulierten NK-Zellen erhöht. Es wurde auch die Fähigkeit
dieser Zellen, sich an die Zielzellen zu binden, untersucht. Im Test wurden NK-Zellen des 45
mg/kg Biobran MGN-3 täglich über 30 Tage einnehmenden Individuums mit Zielzellen K-562
inkubiert und nachfolgend die Fähigkeit, sich an die Zielzellen zu binden gemessen. Nach
einer Stunde gemeinsamer Inkubation bei Temperatur 4°C wurden 200 NK-Zellen gemessen und die
gebildeten Bindungen mit K-562 gezählt. Die Bindungsrate der NK-Zellen mit den Zielzellen
(K-562) war bei Individuen nach Einnahme von Biobran MGN-3 markant höher als vor der
Einnahme, um 38,5 % gegenüber 9,4 %. Auf Abb. 6 ist ein Foto solcher Bindungen.
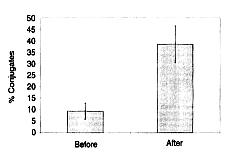 Abb. 5:
Prozentueller Anteil der Bindungen zwischen den natürlichen Killern (NK-Zellen) und den
Zielzellen K-562. Legende: % Bindungen > Vor Einnahme > Nach Einnahme
Abb. 5:
Prozentueller Anteil der Bindungen zwischen den natürlichen Killern (NK-Zellen) und den
Zielzellen K-562. Legende: % Bindungen > Vor Einnahme > Nach Einnahme
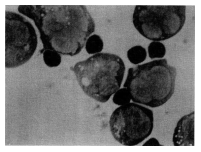 Abb. 6: Tödliche Formation der NK-Zellen und Zieltumorzellen.
Abb. 6: Tödliche Formation der NK-Zellen und Zieltumorzellen.
Ghoneum M. (Universität Ch. R. Drew, USA):INT. IMMUNO THERAPY XIV (2) S. 89-99, 1998
(b) In vitro- Wirkung des Mittels Biobran MGN-3 auf die Aktivität der
Makrophagen-Zellen
Es wurde die Wirkung des Mittels Biobran MGN-3 auf Makrophagen-Zellen, auf die induzierte
Produktion pharmakologischer Mediatoren, konkret der Mediatoren TNF-A, IL-6 und NO
untersucht. Makrophagen wurden mit Biobran MGN-3 verschiedener Konzentrationen (von 1 bis
100 µg/ml) inkubiert und die Supernatanten nachfolgend auf Anwesenheit der genannten
Mediatoren getestet. TNF-a wurde nach Zytotoxizität gegenüber L929, IL-9 nach Zytose B13.19
und NO kolorimetrisch nach Reaktion mit Griess-Test analysiert. Als positive Kontrolle wurde
LPS angewendet.
- Bei Benutzung der Mauszellenlinie der Makrophagen RAW264.7 wies Biobran MGN-3 schon
bei Konzentrationen über 10 µg/ml eine starke Wirkung auf die drei genannten Mediatoren
aus, ebenso wie LPS.
- Benutzen von peritonealen Mausmakrophagen (C3H/He). Der Einfluss des Mittels Biobran
MGN-3 auf das Ausscheiden von Makrophagen aus dem Peritonealraum bei normalen Mäusen ist
auf Abb. 7 dargestellt. Biobran MGN-3 zeigte erneut starke Wirkung bei Konzentrationen
über 10 µg/ml.
- Zelllinie menschlicher Makrophagen U937. MGN-3 induzierte eine starke Aktivität, dies
deutet das gemessene Niveau der produzierten Zytokine TNF-A und IL-6 an, die äquivalent
den LPS auf Niveau 100 µg/ml waren.
Die Ergebnisse zeigen, dass Biobran MGN-3 starkes Potential hat, normale Maus- und auch
menschliche Makrophagen zu aktivieren. Aus der Studie folgt, dass Konzentrationen über 10
µg/ml aktiv sind.
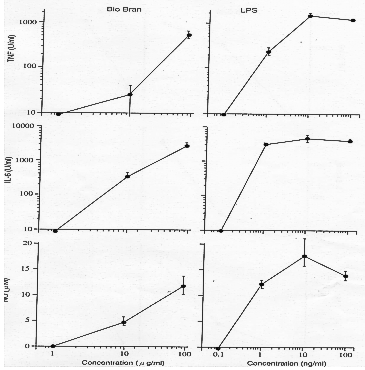 Abb.7: peritoneale Mausmakrophagen (C3H/He)
Abb.7: peritoneale Mausmakrophagen (C3H/He)
Matsuura M. (Medizinische Schule Jichi, JAPAN) : Bericht aus der Medizinischen Schule in
Jichi
(c) Immunstimulation und Krebsvorbeugung
Viele Studien zeigten, dass bei Menschen, die am Arbeitsplatz dem Einfluss verschiedener
Chemikalien ausgesetzt sind, ein erhöhtes Krebsrisiko besteht. Eine dieser Studien setzte
sich das Ziel, die mit dem Einfluss der toxischen Chemikalien zusammenhängende
Immunitätsänderung und die Möglichkeit des Organismus, mithilfe von Biobran MGN-3 besser auf
die chemische Toxizität zu reagieren, zu untersuchen.
An der Studie nahmen elf Personen teil, die in ihrer Arbeit dem Einfluss von Chemikalien
ausgesetzt sind. Die Teilnehmer litten an einer Immunitätsdysfunktion, die sich durch
niedriges Niveau der NK-Zellen-Aktivität (10,2±4,2 LU), blastogenen Antwort der
Blutlymphozyten auf die T-Zellen-Mitogene (PHA, 39060±12517cpm und COMA, 36224±11922cpm) und
B-Zellen-Mitogene (PWM, 16550±6330cpm) gegenüber den Antworten in der Kontrollgruppe zeigte.
Die Teilnehmer erhielten über vier Monate täglich 15 mg/kg Biobran MGN-3. Die Behandlung mit
dem Mittel erhöhte die NK-Zellen-Aktivität nach zwei Monaten vierfach und nach vier Monaten
siebenfach. Das Funktionieren der T- und B-Zellen erhöhte sich auf das Niveau 130, resp. 150
% gegenüber den Anfangswerten.
Ghoneum M. (Universität Ch. R. Drew, USA) : Abstrakt aus dem Konferenzbuch des 7.
internationalen Kongresses über gegen das Altern gerichtete biomedizinische Technologien,
1999
(d) Stimulierte Produktion der TNF-α und IF-γ in den Lymphozyten aus menschlichem
Peripherblut, vermittelt durch modifiziertes Arabinoxylan aus Reiskleie in Biobran
MGN-3.
Es wurde der Mechanismus untersucht, wie Biobran MGN-3 die zytotoxische Aktivität der
NK-Zellen erhöht. Dabei wurde die Wirkung von Biobran MGN-3 auf die Ausscheidungsintensität
des Tumornekrosefaktors α, (TNF-α) und des Interferons-γ (IFN-γ) und auf die Expression der
Schlüsselrezeptoren auf der Zelloberfläche getestet.
Lymphozyten aus dem Peripherblut wurden mit Biobran MGN-3 in Konzentrationen 0,1 und 1 mg/l
inkubiert und die Lösungen wurden dem ELISA Test unterzogen. Die Ergebnisse zeigten, dass
Biobran MGN-3 ein potenter TNF-α-Induktor ist und die Wirkung von der Dosis abhängig ist.
Biobran MGN-3 Konzentrationen im Niveau 0,1 und 1 mg/ml erhöhten die TNF-α-Produktion 22,8-,
resp. 47,1-fach. Biobran MGN-3 erhöhte ebenfalls die Produktion von IFN-γ, wenn auch in
einem geringeren Maß als beim TNF-α. Was die Schlüsselrezeptoren auf der Zelloberfläche
betrifft, erhöhte Biobran MGN-3 die Expression der Antigene der frühzeitigen CD69
Aktivierung nach 16 Stunden Inkubation. Außerdem wurde nach Inkubierung mit Biobran MGN-3
eine Hochregulation der Rezeptoren des Interleukin-2, CD25 und der interzellulären
Zelladhäsionsmoleküle ICAM-1 (CD54) beobachtet. Auch die Inkubierung hoch purifizierter
NK-Zellen mit MGN-3 hatte erhöhte Ausscheidungsniveaus der TNF-α und IFN-γ in Kombination
mit einer Verbesserung der zytotoxischen NK-Zellen-Funktion zur Folge. Weiter hatte das
Zufügen von Biobran MGN-3 zu den mit Interleukin-2 aktivierten NK-Zellen eine synergische
Induktion der TNF-α und IFN-γ Ausscheidung zur Folge.
Ghoneum M. (Universität Ch. R. Drew, USA), Jewett A. (UCLA, USA) : Cancer Detection and
Prevention (Aufdeckung und Vorbeugung von Krebs) Zv.24/Nummer 4, 2000
(e) Wirkung modifizierten Arabinoxylans aus Reiskleie auf die NK-Zellen-Aktivität
menschlicher Lymphozyten des Peripherbluts.
Untersucht wurde die Wirkung von Biobran MGN-3 und seiner molekulären Fraktionen auf die
NK-Zellen-Aktivität. Menschlichen Lymphozyten aus dem Peripherblut wurden Fraktionen mit
hohem Molekulargewicht (10 - 50 kD) hinzugefügt, die durch Gelfiltration mit Benutzung der
Medien G-25 und G-75 gewonnen wurden. Nach 3-tägiger Inkubierung wurde die Aktivität der
NK-Zellen ermittelt. Als Zielzellen wurden fluoreszierend markierte Zellen der Linie K-562
benutzt und die Aktivität der NK-Zellen wurde mit Fluoreszenzmethode Tere Scan bestimmt. Das
gleiche Experiment wurde unter Anwesenheit von IL-2 wiederholt.
Die Versuche zeigten keine grundsätzlichen Differenzen in der Aktivierung der NK-Zellen mit
dem Mittel Biobran MGN-3 oder seiner Fraktionen höheren Molekulargewichts. Als aber dem
Medium IL-2 zugefügt wurde, konnte in den Lösungen, in denen außerdem auch Biobran MGN-3
oder seine Fraktion anwesend waren, eine höhere NK-Zellen-Aktivität als in der Lösung, in
der nur IL-2 anwesend war, beobachtet werden. Das deutet an, dass Biobran MGN-3 die
NK-Zellen in Anwesenheit von IL-2 aktiviert und diese Aktivität auch mit seinen Fraktionen
mit höherem Molekulargewicht anwesend ist.
Ueda Y., Shimomura C. (Universität in Chiba, JAPAN) : Abstrakt vom Jahrestreffen der
Japanischen Gesellschaft für Biowissenschaften, Biotechnologie und Agrochemie 2002
3.2. Antivirenwirkung
Antivirenwirkung des Mittels Biobran MGN-3 gegen HIV in vitro
Zuerst wurde die Antivirenwirkung von Biobran MGN-3 gegen die Produktion von HIV-1 Antigen
p24 in vitro bewertet. Von drei Gesunden gewonnene mononukleare Zellen wurden unter
Anwesenheit von Biobran MGN-3 in Konzentrationen von 0 bis 100 µg/ml bei einer Temperatur
von 37°C eine Stunde mit dem Stamm HIV-1 SF inkubiert. In Abhängigkeit von der Konzentration
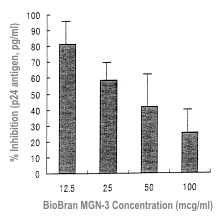
inhibierte Biobran MGN-3 die Bildung syncytialer Formationen, wobei die höchste Inhibition
bei Konzentration 100/ml 75 % betrug (Tabelle 1).
 |
|
Tabelle 1
| Inhibition syncytialer Formationen durch das Mittel Biobran
|
| Dosis Biobran (μg/ml) |
Syncytiale Formation (SF) |
| Anzahl SF |
% Inhibition |
0
12.5
25
50
100
|
42.0±8
25.8±7
21.5±5
15.8±4
10.5±3
|
00.0
38.5
50.0
62.5
75.0
|
|
| Abb. 8 Legende: % Inhibition (Antigen
p24, pg/ml) > Konzentration BioBran MGN-3 (µg/ml)
|
|
|
Ghoneum M. (Universität Ch. R. Drew, USA): Biochemical and Biophysical Research
Communications (Kommunikation zwischen der biochemischen und biophysikalischen Forschung)
243, (1998)
3.3. Tumorhemmende Wirkung
(a) Studie der Wirkung des modifizierten Arabinoxylans aus Reiskleie auf die Inhibition des
Wachstums von Krebszellen verschiedener Linien
In dieser Studie wurde die Inhibitionswirkung des modifizierten Arabinoxylans aus Reiskleie,
das Bestandteil von Biobran MGN-3 ist, auf das Wachstum von Krebszellen verschiedener Linien
wie HL60, K562 und HLE und auf die potentielle induzierte Differenzierung bei HL60 und K562
untersucht. Biobran MGN-3 wurde Kulturen mit Zelllinien beigefügt. Nach 3-tägiger Inkubation
senkte sich das Verhältnis der überlebenden Zellen proportional zur beigefügten Menge
Biobran MGN-3.
Nach Präzipitation mit Äthanol wurde die Ausfällung mit destilliertem Wasser gemischt und
der entstandene Supernatant mittels Säule Sephadex G-25 in 3 Fraktionen (A, B, C) getrennt,
die dann den Kulturen der Zelllinie beigefügt wurden. Die Inhibitionswirkung auf das
Wachstum wurde bei Fraktion auf Linie HL60 und K562 und bei den Fraktionen B und C auf die
Linie HLE beobachtet. Auf Zuwaage, Färbung nach Giems und unspezifische Esterase zeigte sich
eine potentielle induzierte Differentiation bei HL60 und K562. Diese Ergebnisse deuten an,
dass Biobran MGN-3 Bestandteile enthält, die eine Inhibition des Krebszellenwachstums und
eine potentielle induzierte Differentiation der Linien HL60 und K562 aufweisen.
Masada M. (Universität in Chiba, JAPAN) : Abstrakt vom Jahrestreffen der Japanischen
Gesellschaft für Biowissenschaften, Biotechnologie und Agrochemie 2002
(b) Einfluss des Mittels Biobran MGN-3 auf das Wachstum von Krebszellen
Untersucht wurde der direkte Einfluss des Mittels Biobran MGN-3 auf das Wachstum von
Hautkrebszellen und auf die Produktion von Zytokinen. Im Vergleich mit der Kontrollgruppe
der Zellen eines squamösen Karzinoms der Zelllinie SCC13, die in MEM-Medium kultiviert wurde
und das Wachstum der Zellen fortschritt, stellte die Inkubierung der Zellen dieser Linie
[SCC13] mit Biobran MGN-3 das Wachstum der Krebszellen ein (es wurden um 30 % weniger Zellen
nach 48 Stunden und um 50 % weniger nach 72 Stunden Kultivierung gegenüber der
Kontrollgruppe beobachtet).
Analysen mit Durchflusszytometrie zeigten, dass schon nach 16 Stunden Inkubierung der Zellen
SCC13 mit Biobran MGN-3 eine fünffache Erhöhung des Interleukin 10 [IL-10]-Niveaus in den
Zellen eintrat, aber keine sichtbare Änderung im Inhalt des Interferons-γ [INF-γ]. Die
ELISA-Teste des Kultivationsmediums mit Zellen SCC13 wiesen eine 8-fache Erhöhung des
IL-10-Spiegels und 3-fachen Anstieg des IL-12 nach. Es wurde nur eine geringfügige Änderung
der INF-γ - Konzentration verzeichnet. Außerdem wurde der Einfluss des Mittels Biobran MGN-3
auf weitere Zelllinien wie normale Zellen und Brustkrebszellen und Prostatakrebszellen
bewertet.
Diese Ermittlungen deuten an, dass Biobran MGN-3 nicht nur eine Verbesserung der Immunität
des Gastorganismus hervorruft aber auch durch direkten Einfluss auf das Krebszellenwachstum
und die Zytokinproduktion wirkt. Gleichzeitig kann hinter diesen Ermittlungen der bis jetzt
unbekannte Wirkungsmechanismus stehen, der den klinischen Erfolg und den imposanten
Heilungsbeitrag des Mittels Biobran MGN-3, der vom Autor in den vergangenen 4 Jahren
beobachtet wurde, erklären könnte.
Ghoneum M. (Universität Ch. R. Drew, USA) : Abstrakt aus dem Konferenzbuch des 8.
internationalen Kongresses über gegen das Altern gerichtete biomedizinische Technologien,
2000
3.4. Zusatzeffekt bei der Krebstherapie
(a) Auswertung des Zusammenhangs der NK-Zellen-Aktivität und der Überlebensrate bei
Patienten mit verschiedenen Krebstypen bei Applikation von multiimmunologischen
Therapieprotokollen
Ziel der vorgelegten Studie war es, an einem Muster von 205 onkologischen Patienten mit
progressivem und teileweise metastasierendem Krebs fortgeschrittenem III. - IV. Stadium,
nach chirurgischem Eingriff zu bestimmen, ob die Administration des Mittels Biobran MGN-3
einen Effekt auf die Verlängerung des Lebens und die Verbesserung der Überlebensqualität
hat. An der klinischen Studie nahmen Patienten der chirurgischen Klinik Sano in Japan teil.
Sie wurden mit alternativen Ergänzungsmedikamenten und konventionellen Krebsmedikamenten mit
schwachen Nebenwirkungen behandelt.
Die 205, 6 Monate im Krankenhaus aufgenommenen Patienten wurden in zwei Gruppen geteilt: 109
Patienten der Kontrollgruppe wurden mit klinischen, alternativen
Standardergänzungsmedikamenten behandelt und 96 Patienten erhielten zusätzlich ein und ein
halbes Jahr das Mittel Biobran MGN-3.
Bei allen Patienten wurde zur Ermittlung der Immunparameter die Aktivität der NK-Zellen
gemessen. Gleichzeitig wurde bei allen Patienten die Überlebensqualität kontrolliert. Die
NK-Zellen-Aktivität war bei den Patienten nach dem chirurgischen Eingriff überwiegend
niedrig, bei Patienten, denen Biobran MGN-3 gereicht wurde, wurde ein höhere Überlebensrate
verzeichnet, wobei der Effekt umso höher war, umso höher die NK-Zellen-Aktivität war.
(Tabelle 2) Diese Ermittlungen deuten an, dass das Niveau der NK-Zellen-Aktivität bei
progressiven Krebstypen als pathologischer Kennwert angesehen werden kann. In der Gruppe mit
Biobran MGN-3 wurde gleichzeitig eine verbesserte Lebensqualität beobachtet.
Tabelle 2: Beziehung zwischen der Gesamtüberlebensrate, der NK-Zellen-Aktivität und der
Überlebensrate in den beiden beurteilten Gruppen
| Gruppe |
Gruppe Biobran |
Kontrollgruppe |
| Gesamtüberlebensrate |
52/96 (54.2%) |
19/63 (33.9%) |
Kategorie nach NK-Zellen-Aktivität
Niedriger als 19,9 %
20%-40%
Höher als 40%
|
17/40 (42.5%)**
18/35 (51.4%)*
17/21 (81.0%)
|
2/16 (12.5%)
7/25 (28.0%)
10/15 (66.7%)
|
% der Bedeutung gegenüber der Kontrollgruppe **p<0.01 *p<0.05
Takahara K. (Chirurgische Klinik in Sano, JAPAN) : Abstrakt des 3. Jahrgangs des Treffens
der Japanischen Gesellschaft für ergänzende und alternative Medizin und Therapie, 2000
(b) Immunmodulations- und krebshemmende Wirkung des Mittels Biobran MGN-3 bei 5 Patientinnen
mit Brustkrebs
Fünf Patientinnen mit Brustkrebs wurde Biobran MGN-3 in einer Dosis von 3g/täglich gereicht
und nachfolgend mit 51Cr-Separationstest die NK-Zellen-Aktivität an den Zielkrebszellen der
Linie K562 gemessen. Die Ergebnisse zeigten folgendes:
-
Bei niedrigem Niveau der NK-Zellen-Aktivität (12,7 – 58,3 %) und Verhältnissen
Effektor : Target 12 und 100:1 erhöhte sich bei der Behandlung mit Biobran MGN-3 die
NK-Zellen-Aktivität markant (41,8 – 89,5 %), wobei das Verhältnis Effektor : Target
erhalten blieb.
-
Eine erhöhte NK-Zellen-Aktivität wurde schon nach 1-2 Wochen ab Therapiebeginn
beobachtet und bei fortschreitender Administration des Mittels Biobran MGN-3 erhöhte
sie sich weiter.
-
Zwei Patientinnen, die an der Studie von Anfang an teilnahmen (6-8 Monate behandelt
wurden), gelangten in vollständige Remission.
Ghoneum M. (Universität Ch. R. Drew, USA) : Buch der außerordentlichen Konferenz des
Amerikanischen Verbunds für Krebsforschung, 1995)
(c) Immunmodulationswirkung des in Biobran MGN-3 enthaltenen modifizierten Arabinoxylan aus
Reiskleie auf die NK-Zellen in einer Gruppe 27 onkologischer Patienten
Es wurde der Immunmodulationseffekt des Mittels Biobran MGN-3 an 27 onkologischen Patienten
untersucht. Die Patienten litten an verschiedenen fortgeschrittenen Malignitäten. 7
Patienten hatten Brustkrebs, 7 Prostatakrebs, 8 ein mehrfaches Myelom, 3 Leukämie und 2
Gebärmutterhalskrebs. Alle Patienten unterzogen sich der konventionellen Therapie, die um
das Mittel Biobran MGN-3 in einer Dosis von 3g/täglich ergänzt wurde. Nachfolgend wurde nach
2 Wochen, 3 Monaten und 6 Monaten die Aktivität der NK-Zellen untersucht. Die Aktivität der
NK-Zellen wurde mit 51Cr-Separationstest gemessen, als Zielzellen wurden Tumorzellen der
Linie K562 benutzt, wobei das Verhältnis Effektor : Target 12:1 bis 100:1 betrug. Die
Ergebnisse deuteten folgendes an:
-
Die Grundaktivität der NK-Zellen war bei den Patienten auf niedrigem Niveau.
-
Die Behandlung mit Biobran MGN-3 verursachte eine markante Erhöhung der
NK-Zellen-Aktivität schon nach 2 Wochen. Die Induktion der Aktivität war bei den
einzelnen Krebstypen in Prozenten ausgedrückt wie folgt: Brustkrebs 154-332 %,
Prostatakrebs 174-385 %, Leukämie 100-240 % mehrfaches Myelom 100-537 % und
Gebärmutterhalskrebs 100-275 %.
-
Die NK-Zellen-Aktivität erhöhte sich kontinuierlich auch nach 3 und 6 Monaten Therapie.
Ghoneum M. (Universität Ch. R. Drew, USA): Abstrakt des 87. Treffens des Amerikanischen
Verbunds für Krebsforschung, 1996
(d) Ergänzende Therapie metastasierendem Lungenkrebs mit Biobran MGN-3
In diesem Bericht wird ein Fall präsentiert, bei dem durch ergänzende Therapie mit Biobran
MGN-3 bei einem Patienten mit in die Knochen metastasierendem Lungenkrebs günstige
Ergebnisse erreicht wurden.
Patient war ein 67-jähriger Mann. Im August kam er wegen drastischer Gewichtsabnahme und
starkem Husten und Aushusten zum Arzt. Es wurde Lungenkrebs (squamöses Karzinom),
kompliziert durch Tuberkulose (M. tuberculosis) diagnostiziert. Nach antibiotischer
Behandlung der Tuberkulose wurde im Oktober die Bestrahlung des Krebs begonnen. Im Dezember
des gleichen Jahres wurde operativ die untere Hälfte der rechten Lunge mit Tumor entfernt.
Nach der Bestrahlungstherapie wurde der Patient im Januar 1997 aus dem Krankenhaus
entlassen.
Im Juni des gleichen Jahres besuchte der Patient erneut den Arzt und beschwerte sich über
Schmerzen im Brustkorb rechts. Eine Untersuchung mit Knochenszintigrafie bestätigte
zahlreiche Knochenmetastasen. Der Tumor verbreitete sich hauptsächlich in den rechtsseitigen
Rippen, war aber praktisch im ganzen Körper im Knochengewebe vorhanden. Im Juli wurde
analgetische Therapie mit retardiertem Morphin angesetzt. In der Zwischenzeit, ab Ende Mai
wurde ebenfalls die Therapie mit Biobran MGN-3 in Dosis 3 g täglich initiiert. Ab Januar
1998 begannen die Schmerzen zurückzugehen. Biobran MGN-3 wurde ununterbrochen weiter
gereicht aber dabei das retardierte Morphin schrittweise gesenkt und im Juni ganz
ausgesetzt. Der Tumormarker ICPP war zur Zeit der Bestätigung der Krankheitsrückkehr auf
Niveau 16,8 ng/ml und sank schrittweise auf 7,6 ng/ml im Dezember 1997 und 6,7 ng/ml im Juni
1998. Die Knochenszintografie zeigte eine markante Verbesserung und bestätigte, das die
Tumorausbreitung in die Knochen rückgängig ist. Die NK-Zellen-Aktivität war zur Zeit der
Krankheitsrückkehr auf Niveau 9,0 % und erhöhte sich allmählich und hält sich gegenwärtig
auf hohem Niveau.
Sobajima T. (Krankenhaus Hoshigaoka Kosei Nenkin, JAPAN) : Abstrakt des 2. Jahrgangs des
Treffens der Japanischen Gesellschaft für ergänzende und alternative Medizin und Therapie,
1999
(e) Applikation des Mittels Biobran MGN-3 in nachkonventioneller Therapie
Die Behandlung eines schlafenden Tumors wird im Zutritt zum Krebs in Japan
Hauptbehandlungskonzept. Hauptziel dieser Therapie ist die Verlängerung des Lebens des
Patienten und gleichzeitig das Erhalten einer hohen Lebensqualität. Dr. Tunekawa verschreibt
sie den Patienten auf Wunsch und sieht dabei die Erhöhung der Lebensqualität als wichtiges
therapeutisches Ziel an. In seinem Bericht führt er an, dass er vierunddreißig onkologische
Patienten hat, bei denen er eine Kombination aus Chemotherapie zur Unterdrückung des
schlafenden Tumors und ergänzende und alternative Therapie appliziert und gewährt eine
Abschrift der Therapie von drei Patienten:
-
Patienten (Hauptkrankheiten): 3 Magenkrebs, 3 Lungenkrebs, 2 malignes Lymphom, 6
Dickdarmkrebs (rektaler Abschnitt), 3 Brustkrebs, 17 andere Krebstypen
-
Therapiedauer: 6-18 Monate
-
Fallstudien
-
iv. T.S. (60), Frau, Magenkrebs (IV. Stadium), karzinomatöse Entzündung des
Bauchfells: Der Patientin wurde im Januar 2000 operativ ein scirrhöses Magengeschwür
entfernt. Im Februar 2000 entwickelte sich eine karzinomatöse Bauchfellentzündung
und sie unterzog sich im IV. Stadium einer Gastrektomie. CA19-9 war 108. Im August
2000 besuchte sie unsere Klinik und beschwerte sich über Bauchschmerzen,
Verstopfung, Anämie und Anorexie. CA19-9 war 390 und die NK-Zellen-Aktivität 25,6.
Es wurde ihr eine Kombination Chemotherapie (TS1) und holistischer Behandlung
verordnet. Zur Verbesserung der Immunität wurde ihr Biobran MGN-3 in Dosis 3 g
täglich gereicht. Einen Monat war CA19-9 auf dem Niveau 63. Die Werte der
Tumormarker sanken schrittweise und die NK-Zellen-Aktivität stieg. Im August 2001,
11 Monate später, war CA19-9 auf Niveau 25 und die NK-Zellen-Aktivität betrug 51,5.
Gegenwärtig hat die Patientin fast keine subjektiven Symptome und ist auch gut
ernährt.
-
v. F.A. (46), Frau, Brustkrebs, mit Metastasen im Lendenwirbel und in der
Gebärmutter: Die Patientin unterzog sich im Juli 1998 einer Brustkrebsoperation und
es wurde Hormon- und Antikrebstherapie angesetzt. Im März 2001 wurden Metastasen im
Lendenwirbel und im April auch in der Gebärmutter entdeckt. Im Mai 2001 wurde eine
Hysterektomie der Gebärmutter durchgeführt. Sie wurde nach Hause entlassen und
Paclitaxel und Paraplatin angesetzt. Im Juli 2001 besuchte sie wegen
Knochenschmerzen Dr. Tunekawa. In dieser Zeit betrug CA 153, NCC-ST war 439 und die
NK-Zellen-Aktivität 9,3. Paraplatin wurde in der Therapie belassen und mit
holistischer Behandlung begonnen. Zur Verbesserung der Immunität wurde Biobran MGN-3
in Dosis 3 g täglich hinzugefügt. Zwei Monate später betrugen die CA Marker nur 18,
NCC-ST 28,9, die NK-Zellen-Aktivität 22,0 und die Schmerzen gingen zurück.
Nachfolgend wies die Patientin eine stabile Senkung der Tumormarker und eine
Erhöhung der NK-Zellen-Aktivität aus. Im Juli 2002 war CA auf Niveau 14, NCC-ST 3,2,
die NK-Zellen-Aktivität 59, die Schmerzen voll zurückgegangen und die Ermittlungen
der Knochenszintigrafie weniger auffällig. Gegenwärtig ist die Patientin gut ernährt
und freut sich, dass sie sich wieder dem Schlagzeugspielen widmen kann.
Tunekawa H. (Tokioter Gesellschaft für die Propagation holistischer Medizin, JAPAN):
Abstrakt des dem Mittel Biobran gewidmeten Workshop in Berlin, 2002
(f) Bewertung der Wirkung des Mittels Biobran MGN-3 bei der Behandlung von Krebs im
progressiven Stadium
Dr. Mizukami hat Erfahrungen mit dem Mittel Biobran MGN-3 an einem Muster von 97
onkologischen Patienten mit verschiedenen Krebserkrankungen progressiven Stadiums. Die
Patienten hatten Magen-, Dickdarm-, Brust-, Lungen-, Bauchspeicheldrüsen-, Leber-,
Gallengang-, Rachen-, Eierstock- Gebärmutterhals-, Gebärmutter-, Schilddrüsen-, Prostata-,
Mundhöhlenkrebs, mehrfaches Myelom usw. Obwohl die Patienten schon chirurgische Eingriffe,
Chemotherapie oder Bestrahlungen in großen Krankenhäusern hinter sich hatten, war die
Prognose für die meisten schlecht. Sie hatten Metastasen und Rezidive und entschieden sich
deshalb Dr. Mizukamis Klinik aufzusuchen und eine Immunbehandlung zu versuchen. Fast alle
Patienten, denen Biobran MGN-3 angesetzt wurde, hatten zu dieser Zeit schon keine
Chemotherapie oder Bestrahlungen mehr. Auf Grundlage der klinischen Beobachtungen und
Fragebogen wurde anschließend detailliert die Überlebensqualität untersucht. Bei allen,
Biobran MGN-3 einnehmenden Patienten wurde ein gemeinsames Phänomen beobachtet.
In mehreren Fällen verbesserte sich die Überlebensqualität bei der Einnahme von Biobran
MGN-3 offensichtlich. Auch wenn allgemein die Überlebensqualität bei Krebspatienten im
fortgeschrittenen Stadium mit zunehmender Zeit gleichmäßig fallende Tendenz hat, war diese
Tendenz bei Biobran MGN-3 einnehmenden Patienten geringer und änderte sich sogar in Tendenz
längeren Überlebens bei guter Lebensqualität und wurden auch Fälle langfristigen Überlebens
verzeichnet.
Bezüglich der Lebensqualität wurden diese Beobachtungen gemacht:
-
Obwohl das Beherrschen starker Schmerzen nicht einfach ist und bei Krebspatienten im
fortgeschrittenen Stadium in vielen Fällen einzige Möglichkeit Morphin ist,
benötigten einige der Biobran MGN-3 Patienten kein Morphin und bei anderen konnte
dessen Dosis verringert werden.
-
Insgesamt wurde eine verringerte Tendenz zu Schwächegefühlen beobachtet.
-
Es wurde eine verringerte Tendenz zu Appetitverlust beobachtet.
-
Tendenz zur Fähigkeit zu Hause bleiben und sich vor dem Tod relativ gut fühlen zu
können.
-
Tendenz, kurz vor dem Tod klaren Geist und die Fähigkeit zur Kommunikation mit der
Familie zu behalten.
Dr. Mizukami fasste seine Beobachtungen im Konstatieren zusammen, dass für Patienten mit
Krebs im hohem Stadium die Tatsache grundsätzlich ist, dass sich die Lebensqualität bei
Einnahme von Biobran MGN-3 nicht so schnell verschlechtert. Dies erscheint für die Zukunft
als wichtiger Aspekt auch für das medizinische Vorgehen bei der Krebsbehandlung.
Mizukami O. (Forschungsinstitut für die Unterstützung der Gesundheit und Layman-Stiftung New
Life, JAPAN): Abstrakt des dem Mittel Biobran gewidmeten Workshop in Berlin, 2002
3.5. Wirkung auf die Apoptose
Biobran MGN-3 sensitiviert menschliche leukämische T-Zellen auf durch Todesrezeptor (CD95)
induzierte Apoptose.
In dieser Studie wurde der Effekt von Biobran MGN-3 auf die durch Todesrezeptor induzierte
Apoptose in menschlichen leukämischen Zellen der Linie HUT 78 untersucht. Die Zellen HUT 78
wurden zuerst mit Biobran MGN-3 behandelt und anschließend mit agnostischem Antistoff des
Todesrezeptors (Fas, CD95) inkubiert. Die Apoptoserate wurde mittels Durchflusszytometrie
FACScan unter Benutzung von Propidiumiodid bestimmt. Die Aktivierung der Caspasen 3,
Caspasen 8 und Caspasen 9 wurde durch Durchflusszytometrie ermittelt. Das Potential auf
Mitochondrium wurde mithilfe FACScan unter Benutzung des Farbstoffs DIOC6 gemessen. Die
Expression CD95 und BCI-2 wurde mit Durchflusszytometrie gemessen.
Nach Ermittlungen erhöht Biobran MGN-3 in Abhängigkeit von der Dosis das durch Anti-CD95
induzierte Apoptosemaß. Die erhöhte Rate des Zelltods korrelierte mit dem Anstieg der
Potentialdepolarisierung auf das Mitochondrium und mit der erhöhten Aktivierung der Caspasen
3, Caspasen 8 und Caspasen 9. Die Behandlung mit Biobran MGN-3 hatte keinen Einfluss auf das
Niveau der Expression CD95, verursachte aber eine Herabregulation der Expression BCI-2.
Diese Ergebnisse deuten an, dass Biobran MGN-3 die Neigung des Krebses zur durch
Todesliganden vermittelten Apoptose erhöht, das kann bei der Krebstherapie eine wesentliche
Tatsache sein..
Ghoneum M. (Universität Ch. R. Drew, USA) : Cancer Letter (Onkologische Blätter), 2003
3.6. Aktivierung der vitalen Abwehr
(a) Aktive Wirkung des Mittels Biobran MGN-3 bei der Eliminierung von Sauerstoffradikalen
Der Bericht referiert über die Erforschung der Eliminierungswirkung des Mittels Biobran
MGN-3 und seiner Fragmente auf Sauerstoffradikale. Biobran MGN-3 wurde an Fragmente mithilfe
der Säule Sephadex G-25 fraktioniert. Die einzelnen Fragmente wurden nach Größe mit den
Buchstaben L, M und S (L Molekularmasse > 10000), M (Molekularmasse von 10000 bis 3000) und
S (Molekularmasse < 3,000) gekennzeichnet.
Die Eliminationswirkung der aktiven Enzyme wurde durch Messen dieser Wirkung auf das
Superoxidanion-Radikal (•O2), auf das, aus der Fentonreaktion stammenden Hydroxylradikal
(•OH) und auf das durch ultraviolette Strahlung generierte Hydroxylradikal bewertet.
Die Messergebnisse sind in der Tabelle dargestellt. Am besten von allen inhibierte die
Bildung des Hydroxylradikals •OH generiert durch •O2 und ultraviolette Strahlung Biobran mit
der Kennzeichnung S (mit der niedrigsten Molekularmasse). Eine hohe Wirkung zeigten alle
Fragmente des Mittels bei der Eliminierung des durch Fentonreaktion generierten Hydroxyls
(•OH). (Tabelle 3)
Tabelle 3
Eliminierungswirkung des Mittels Biobran MGN-3 auf aktive Sauerstoffradikale
(•O2 und •OH und UV induzierte •OH)
| Typ des aktiven Sauerstoffs und der Wirkung SOD |
Eliminierungsmaß des Superoxidanionradikals (%) |
Wirkung SOD (Superoxiddismutase) (U/ml) |
Eliminierungsmaß des UV generierten Hydroxylradikals (%) |
| 20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
BioB
BioB-L
BioB-M
BioB-S
|
64.6
39.9
49.5
90.4
|
23.0
10.4
15.6
68.1
|
4.4
0
0
26.4
|
7.6
5.0
7.2
70.5
|
0.9
0.8
1.4
15.7
|
0
0
0
2.6
|
94.9
(72.6)
97.2
(41.8)
97.0
(45.4)
96.5
(71.0
|
78.9
(35.9)
34.4
(16.5)
68.4
(9.9)
55.1
(54.9)
|
3.3
(11.5)
3.3
(1.0)
8.7
(3.9)
4.2
(19.6)
|
·O2:HPX-XOD Reaktion,·OH:Fenton-Reaktion
·OH generiert durch UV-Reaktion:365nm,4×103J/m2/min×5
Tazawa K. Medizinische und Pharmazeutische Universität in Tojama, JAPAN): Biotherapy
(Biotherapie) Band 14, 2000
(b) Basisstudie des Einflusses der Arabinoxylanverbindung (Biobran MGN-3) auf die
Aktivierung der vitalen Abwehr.
In dieser Studie wurde in einem Tierexperiment der Einfluss von Biobran MGN-3, seine
biophylaktische Wirkung auf die Überlebensrate nach Induktion einer tödlichen Sepsis durch
Lipopolysaccharide (LPS) beobachtet.
Für das Experiment wurde der Mausstamm BALB/c (Männchen im Alter von 5-7 Wochen) benutzt.
Den Mäusen der getesteten Gruppe wurde zwei Wochen lang jeden zweiten Tag, also insgesamt
sieben Mal, über orale Sonde 20 mg/kg, resp. 200 mg/kg Biobran MGN-3 aufgelöst in 0,5 ml
phosphatgepufferter Salzlösung (PBS) gereicht. Die Mäuse der Kontrollgruppe erhielten in den
gleichen Intervallen 0,5 ml PBS. 12 Stunden nach der letzten oralen Dosis wurde jeder Maus
intraperitoneal 200 µg LPS in den Körper gebracht und nachfolgend ihr Zustand beobachtet. Im
weiteren Experiment wurde den Mäusen beider Gruppen, der Biobran- und der Kontrollgruppe,
intraperitoneal 100 µg LPS in den Körper gebracht. Die Mäuse wurden anschließend 0, 2, 4 und
8 Stunden nach der Verabreichung der LPS getötet und Peripherblut aus dem Herz entnommen.
Nach Abtrennen des Serums wurden die Werte IL-6 und TNF gemessen. Die IL-6 Aktivität wurde
unter Benutzung der Zelllinie B9 und die TNF-Aktivität mit biologischer Prüfung an Zellen
der Linie WEHI164-13 gemessen.
Wie auf Abb. 9 ersichtlich, war die Überlebensrate nach Verabreichen von 200 µg LPS im
Vergleich mit der Kontrollgruppe wesentlich besser in den Gruppen, wo den Mäusen täglich 20
mg/kg und 200 mg/kg Biobran MGN-3 verabreicht wurde (Gruppe Biobran MGN-3 20 mg/kg versus
Kontrollgruppe p = 0,0456; Gruppe Biobran MGN-3 200 mg/kg versus Kontrollgruppe P = 0,0232,
Analyse mit Mantel-Cox-Test). Nach Verabreichen von 100 µg LPS den Mäusen, denen vorab
täglich 20 mg/kg und 200 mg/kg Biobran MGN-3 gegeben wurde, überlebten alle Mäuse, wobei in
der Kontrollgruppe 3 von 10 Mäusen starben.
Um den Mechanismus aufzudecken, der hinter der verbesserten Überlebensrate in der Gruppe
Biobran MGN-3 steht, wurden die Blutkonzentrationen IL-6 und TNF gemessen. In der Gruppe mit
Biobran MGN-3 war die Blutkonzentration IL-6 zwei Wochen nach Verabreichen LPS markant
niedriger als in der Kontrollgruppe (Kontrollgruppe 702,9 ± 24,7 ng/ml, Gruppe Biobran
MGN-3 403,1 ± 59,6 ng/ml; p < 0.01), erhöhte sich aber 8 Stunden nach Verabreichen stark
(Kontrollgruppe 88,5 ± 50,0 ng/ml, Gruppe Biobran MGN-3 441,0 ± 115,0 ng/ml; p < 0.05). Die
Blutkonzentration TNF erhöhte sich 4 Stunden nach der Gabe von LPS in der Gruppe Biobran
MGN-3 stark im Vergleich mit der Kontrollgruppe (Kontrollgruppe 492 ± 187, Gruppe Biobran
MGN-3 1816 ± 307 pg/ml; p < 0.01).
Beim experimentellen Modell mit LPS induzierter tödlicher Sepsis wurde vorausgesetzt, dass
die große Menge der Entzündungszytokine (IL-1, 6, TNF-α) die aus den Zellen des
retikuloendothelialen Systems in den Organismus freigegeben werden, ein Versagen zahlreicher
Organe verursacht und dies zum Tod führt. In dieser Studie wurde aber in der Gruppe mit dem
Mittel Biobran MGN-3 eine markante Erhöhung der Überlebensrate beobachtet. Mögliche Gründe
sind, dass die Aufnahme des Mittelos Biobran MGN-3 die Bildung von Makrophagen produzierter,
histotoxischer Zytokine inhibiert oder dass Biobran MGN-3 den Weg zur Histotoxizität auf
Niveau der Zielzellen blockiert.
Sudo N., Kubo C. (Kyushu Universität, JAPAN): The Japanese Journal of Clinical and
Experimental Medicine (Japanische Zeitschrift für klinische und experimentelle Medizin),
Band 78, 1, 2001
(c) Reduktion der Gewichtsabnahme bei Mäusen nach Verabreichen von Cisplatin dank Biobran
MGN-3.
Bei der Krebstherapie verursachen Platin enthaltende Medikamente oft ernste Nebenwirkungen
wie Unwohlsein, Erbrechen, Nephropathie und durch Beschädigung der Nierenkanälchen
hervorgerufene Hypomagnesiämie (Lajer & Dangaard). Weiter kommt es auch zu Gehörverlust,
peripherer Neuropathie und zu einer der am meist devastierenden Nebenwirkungen, der
Myelosuppression (Prestayko und Koll. 1979), die zur Immunschwächung führt. Jedes
Einschränken der Nebenwirkungen von Cisplatin ist deshalb sehr wertvoll und erwünscht. Im
Rahmen unserer Bemühungen haben wir den Einfluss von Biobran MGN-3 auf die Verringerung des
Gewichtsverlustes bei Mäusen studiert, denen die maximal tolerierbare Dosis Cisplatin
gereicht wurde.
Eine Woche vor der Gabe des Cisplatin begannen wir in zwei Gruppen mit Biobran MGN-3 in
Dosis 10 mg/ml (Trockenmasse) in Wasser, resp. intraperitoneal in Injektion 0,1 ml, wo die
äquivalente Dosis in physiologischer Phosphatlösung (PBS) aufgelöst wurde. Die Dosis 1 mg
pro Tier wurde von der empfohlenen Dosis für Menschen (50 mg/kg) abgeleitet. Cisplatin in
der Menge 15 mg/kg wurde intraperitoneal in 0,1 ml phosphatgepufferter Salzlösung (PBS) mit
0,5 % DMSO als Träger gegeben. Zwei Gruppen erhielten über Sonde Wasser, resp.
intraperitoneal PBS und nach einer Woche wurde beiden Cisplatin gereicht.
Der Gewichtsverlust trat gleich am nächsten Tag nach intraperitonealer Injektion des
Cisplatin in beiden Gruppen ein, in den Gruppen mit Biobran MGN-3 und auch ohne. Der größte
Gewichtsverlust wurde in beiden Gruppen am 5. Tag nach Gabe des Cisplatin beobachtet,
ebenfalls in beiden Gruppen, mit Biobran und ohne, und mit oral und auch intraperitoneal
gegebenem Mittel. Der größte Gewichtsverlust wurde bei Mäusen verzeichnet, denen Cisplatin
ohne Biobran MGN-3 gegeben wurde. Obgleich sich der Gewichtsverlust bei den Mäusen, denen
Biobran MGN-3 gegeben wurde, 20 Prozent des bei den Mäusen der Gruppen, die nur Cisplatin
erhielten, beobachteten Gewichtsverlustes näherte, muss konstatiert werden, das in dieser
Gruppe keine Maus starb, keine Maus Durchfall oder blutenden Kot hatte, Nebenwirkungen, die
in der Regel Cisplatin begleiten. In der Rekonvaleszenzphase erhielten die Mäuse aus den
Gruppen mit Biobran das Gewicht schneller zurück als in den Gruppen ohne Biobran.
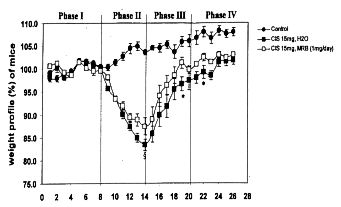 Abb. 10 Legende: Gewichtsprofil der Mäuse (in %)
Abb. 10 Legende: Gewichtsprofil der Mäuse (in %)
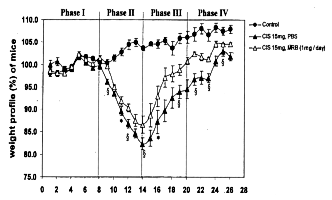 Abb. 11
Abb. 11
Endo Y., Kanbayashi H. (Universität Mac Master, KANADA) : Pharmacology and Toxicology
(Pharmakologie und Toxikologie), 2003
(d) Einfluss des Mittels Biobran MGN-3 auf durch Cisplatin und Adriamycinom induzierte
Toxizität bei Ratten
Biobran MGN-3 ist ein Derivat aus Reiskleie, das durch teilweise Hydrolyse der
wasserlöslichen Fraktion des Reisballaststoffes mit Carbohydrasen aus dem Pilz Lentinus
edodes hergestellt wird [Patent-Nr. in den USA 5560914]. Es wurde nachgewiesen, dass Biobran
MGN-3 Modifikator der biologischen Antwort ist und bei Patienten mit geschwächter Immunität
einen Anstieg der NK-Zellen-Aktivität verursacht [Int. J. Immunother. 14 (1) 1998].
Ziel: Vorbeugen ernster pathologischer Änderungen und des
Gewichtsverlustes, die mit der Gabe einer Dosis Cisplatin (CIS), resp. Adriamycin (ADR)
zusammenhängen, durch tägliche Administration des Mittels Biobran MGN-3 in einer Menge von 5
resp. 50 mg/kg. Nach 13 Tagen Akklimatisierung wurden für den Test auf Grundlage des
Körpergewichts Rattenmännchen des Stamms Spaque-Dawley ausgewählt und in acht Gruppen zu je
10 Stück geteilt (Dosen sind in mg/ml aufgeführt):
-
Biobran 5 mg p.o. + Träger i.p.
-
Biobran 50 mg p.o. + Träger i.p.
-
Kontrollgruppe p.o. + CIS 8 mg i.p.
-
Biobran 5 mg p.o. + CIS 8 mg i.p.
-
Biobran 50 mg p.o. + CIS 8 mg i.p.
-
Kontrollgruppe p.o. + ADR 10 mg i.p.
-
Biobran 5 mg p.o. + ADR 10 mg i.p.
-
Biobran 50 mg p.o. + ADR 10 mg i.p.
Den Ratten wurde 11 Tage täglich peroral (p.o.) Biobran MGN-3 (aufgelöst in destilliertem
Wasser), resp. Träger gegeben. Das Chemotherapeutikum resp. der Träger wurde jeder
getesteten Ratte am 3. Tag mit Injektion intraperitoneal (i.p.) gegeben. Über 11 Tage wurden
bei den Ratten täglich die klinischen Symptome verfolgt. Das Gewicht wurde jeden zweiten Tag
aufgezeichnet. Am 11. Tag wurden die Tiere durch CO2 Inhalation getötet und die Obduktion
vorgenommen. Visuell wurden die wichtigsten Organe kontrolliert und die Beschädigung des
gastrointestinalen Trakts ermittelt.
Ergebnisse: Zwischen dem 7. und 11. Tag starben fünf Ratten der 3. Gruppe,
drei der 5. Gruppe und eine der 4. Gruppe. Ratten denen nur Biobran MGN-3 in einer Menge von
5 oder 50 mg/kg p.o. gegeben wurde wiesen einen statistisch bedeutenden Gewichtsanstieg aus
(+72 %). Ratten, die nur CIS oder ADR erhielten, verzeichneten einen geringen
Gewichtsanstieg (-1,5 % bei CIS und +30 % bei ADR). Ratten, die Biobran MGN-3 in Menge 5
oder 50 mg plus CIS oder ADR erhielten wiesen einen wesentlich größeren Gewichtsanstieg als
die Ratten der rein chemotherapeutischen Gruppe aus (+11 % in der Gruppe Biobran MGN-3 5 mg
+ CIS und +46 % in der Gruppe + ADR). In der Gruppe Biobran MGN-3 50 mg + CIS betrug der
Gewichtsanstieg +44 % und in der Gruppe Biobran MGN-3 50 mg + ADR 43 %. Überlebende Ratten,
denen Biobran MGN-3 gegeben wurde, sahen im Vergleich mit den Ratten, die nur CIS oder ADR
ohne Biobran MGN-3 erhielten, gesünder aus, sie nahmen zu und es wurde auch niedrigeres
Auftreten ernster intestinaler Pathologien beobachtet.
Tabelle 4: Wirkung des Mittels Biobran auf den durch Cisplatin und
Doxorubicin induzierten Gewichtsverlust
| Therapie (alles intraperitoneal) |
Tag 0 |
Tag 3 |
Tag 5 |
Tag 7 |
Tag 9 |
Tag 11 |
5mg/kg p.o. + Träger
50mg/kg p.o. + Träger
Kontrollgruppe p.o + Cp8mg/kg
5mg/kg p.o. + Cp8mg/kg
50mg/kg p.o. + Cp8mg/kg
Kontrollgruppe p.o. + Dx10mg/kg
5mgn/kg p.o. + Dx10mg/kg
50mg/kg p.o. + Dx10mg/kg
|
100
100
103
99
101
103
101
101
|
100
98
101
99
99
100
100
101
|
100
100
82
85
92
88
92
92
|
100
97
69
76
90
82
89
87
|
100
97
55
68
85
77
86
85
|
100
97
57
65
84
76
85
83 |
p.o.- peroral, Dx-Doxorubicin, Cp-Cisplatin
Jacoby H. I. (USA) : Journal of Nuturaceuticals, Function & Medical Foods (Zeitschrift für
Naturheilkunde und Funkrions- und Gesundheitsnahrungsmittel) Band 3 (4) 2001
(e) Effekt des Mittels Biobran MGN-3 auf die durch Radiotherapie induzierte Toxizität bei
Mäusen
Ziel dieser Studie war die Untersuchung der Modifikationswirkung von Biobran MGN-3 auf die
sich durch Abnahme des Knochenmarks bei Bestrahlung des Organismus zeigenden
Radiosensivität. Mit der Bemühung, eine eventuelle klinische Anwendbarkeit zu
berücksichtigen, testeten die Autoren die Wirkung quantitativ über das gesamte Spektrum der
Bestrahlungsdosen von 4,5 bis 8,5 Gy.
Dem Versuch wurden 4-, bzw. 5-Wochen alte Mausmännchen des Stamms SPF BALB/c (Gruppe F2)
unterzogen. In ausgewählten Gruppen wurde den Tieren das Mittel MGN-3 in einer Menge von 50
mg/kg Körpergewicht in der Nahrung beigefügt. Die Gruppen bestanden aus 10 bis 50 Tieren.
Nach zwei Tagen Akklimatisierung wurde der Nahrung der Mäuse der Testgruppe (F2) Biobran
MGN-3 beigefügt. Nach 8, resp. 15 Tagen Zugabe des Mittels MGN-3 wurden die Tiere
Bestrahlung ausgesetzt. Anschließend wurde 3-mal täglich ihr Gewicht und täglich das Sterben
verfolgt. In einigen Fällen wurde den Mäusen im Rahmen des Experiments Biobran MGN-3 ganze
zwei Wochen vor der Bestrahlung gegeben, in anderen die Gabe erst nach der Bestrahlung
begonnen.
Obwohl in der Gruppe F2 schon ab siebten Tag nach der Bestrahlung ein Sterben der Mäuse
infolge Knochenmarkabnahme beobachtet wurde, konnte bei den Mäusen der Biobran MGN-3 Gruppe
eine Tendenz zu späterem Unterliegen bemerkt werden. Die Dosis LD50 (die bei mindestens der
Hälfte der bestrahlten Tiere den Tod verursacht) betrug etwa 5,15 Gy, wobei DRF (die Dosis
reduzierender Faktor) etwa auf Niveau 1,14 lag. Was das Körpergewicht betrifft, wurde in den
Gruppen Biobran MGN-3 eine Tendenz zur Erhaltung eines höheren Gewichts beobachtet. Der
Effekt des früheren Beginns der Administration des Mittels Biobran MGN-3 deutet an, dass es
günstiger ist, mit der Einnahme des Mittels noch vor der Bestrahlung zu beginnen.
Die Bestrahlungsdosis der Mäuse in Organismusmitte wurde als 1,21-faches der aufgeführten
Dosen errechnet, das bedeutet, dass die Dosis LD50 für die Tiere der Kontrollgruppe 6,23 Gy
betrug. Auch wenn der radioprotektive Effekt (DRF) des Mittels Biobran nicht sehr hoch war
(1,14), muss hinzugefügt werden, dass im Rahmen der gesamten Studie keine Nebenwirkungen
beobachtet wurden.
Nakatugawa S. (Universität in Nagoya, JAPAN) : The Report of Nagoya Univ. (Bericht der
Universität in Nagoya), 2003
(f) Effekt des Mittels Biobran MGN-3 auf experimentell hervorgerufene Leberdysfunktion bei
Ratten
In dieser Studie wurde die Wirkung von Biobran MGN-3 auf eine Dysfunktion der Leber
untersucht. Konkret wurde die Wirkung des Mittels auf die Entwicklung einer experimentell
durch die Gabe von Galactosamin (GaIN) und Acetaminophen (AAP) hervorgerufenen
Leberdysfunktion untersucht. GaIN wurde in den Experimenten Nr. 1 und 3, AAP in den
Experimenten 4 und 5 gegeben.
Im Experiment Nr. 1 erhielten die Ratten intraperitoneal Biobran MGN-3 verschiedener
Konzentrationen und nach 1 Stunde GaIN in einer Menge von 800 mg/kg.
Im Experiment Nr. 2 wurde oral unfraktioniertes Biobran MGN-3 gegeben und intraperitoneal
seine Fraktion mit hoher, resp. niedriger Molekularmasse gereicht. Nach 1 Stunde wurde den
Ratten GaIN in Menge von 800 mg/kg gegeben.
Im Experiment Nr. 3 wurde Biobran MGN-3 intraperitoneal gegeben, nachdem es vorab erwärmt,
hydrolysiert und über Ionenaustauscherharz gefiltert wurde. Nach 1 Stunde wurde den Ratten
GaIN in Menge von 800 mg/kg gegeben.
Im Experiment Nr. 4 wurde Biobran MGN-3 intraperitoneal und oral gegeben und nach 1 Stunde
wurde den Ratten AAP in Menge von 700 mg/kg gegeben.
Im Experiment Nr. 5 wurde Biobran MGN-3 intraperitoneal gegeben, nachdem es zuerst erwärmt,
hydrolysiert und über Ionenaustauscherharz gefiltert wurde. Nach 1 Stunde wurde den Ratten
AAP in Menge von 500 mg/kg gegeben.
In allen Experimenten wurden die Ratten 24 Stunden nach Gabe GaIN, resp. AAP getötet und die
Werte der Transaminasen (GOT, GPT) ermittelt.
Ergebnisse
Experiment 1: In allen Gruppen, in denen Biobran MGN-3 gereicht wurde, war
die Serumaktivität GOT und GPT, die durch GaIN induzierte Leberdysfunktion hervorgerufen
wurde, im Vergleich mit der in der Kontrollgruppe gemessenen Aktivität, stark unterdrückt.
Die Suppressionswirkung des Mittels Biobran MGN-3 auf die GaIN induzierte Leberdysfunktion
gipfelte bei einer Dosis 20 mg/kg und erhöhte sich bei höheren Dosen des Mittels Biobran
MGN-3 nicht weiter.
Experiment 2: In allen Gruppen, in denen Biobran MGN-3 nicht fraktioniert
oder auch fraktioniert und mit höherer oder niedrigerer Molekularmasse gegeben wurde, wurde
der Anstieg der Serumaktivität GPT infolge der durch GaIN induzierten Leberdysfunktion im
Vergleich mit dem Anstieg in der Kontrollgruppe stark unterdrückt. Die Suppressionswirkung
des fraktionierten und nicht fraktionierten Mittels Biobran MGN-3 war ähnlich.
Experiment 3: In Gruppen, in denen hydrolysiertes Biobran MGN-3 gegeben
wurde, wurde der Anstieg der Serumaktivität GOT infolge der durch GaIN induzierten
Leberdysfunktion im Vergleich mit dem Anstieg in der Kontrollgruppe stark unterdrückt.
Experiment 4 : In Gruppen, in denen Biobran MGN-3 intraperitoneal und auch
oral gegeben wurde, wurde der Anstieg der Serumaktivität GOT infolge der durch AAP
induzierten Leberdysfunktion im Vergleich mit dem Anstieg in der Kontrollgruppe stark
unterdrückt.
Experiment 5: Ähnliche Ergebnisse wie bei Experiment Nr. 3 wurden mit
hydrolysiertem Biobran MGN-3 auch nach Gabe von AAP erreicht. In Gruppen, in denen
hydrolysiertes Biobran MGN-3 gegeben wurde, wurde der Anstieg der Serumaktivität GOT im
Vergleich mit dem Anstieg in der Kontrollgruppe stark unterdrückt.
Es wurde bestätigt, dass Biobran MGN-3 Suppressionswirkung auf die durch GaIN oder AAP
induzierte Leberdysfunktion hat. Es scheint, dass der HCl aktive Bestandteil des Mittels
nicht hydrolisiert.
Yamada T. (Universität in Chiba, JAPAN) : Abstrakt des 6. Treffens des Japanischen Verbunds
für Forschung von Nahrungsmittelballaststoffen, 2002
(g) Oral eingenommenes Mittel Biobran MGN-3 lindert das Erkältungssyndrom bei älteren
Menschen
Bei Risikogruppen wie alten Menschen und Kindern ist es wichtig, auf Infektionen
unterdrückende Vorbeugungsmaßnahmen wie Grippeimpfungen zu achten und vor allem auf
Maßnahmen, die sekundäre Bakterieninfektionen verhindern können. Bei Untersuchungen von
Fällen einer Lungenentzündung, die sich aus der Verschlimmerung einer normalen Erkältung
entwickelten, hinsichtlich des Alters, wurde festgestellt, dass das Risiko einer sekundären
bakteriellen Infektion bei Menschen mit 75 und mehr Jahren höher ist. Das Risiko einer
begleitenden Lungenentzündung ist ebenfalls bei älteren Patienten mit neurologischen
Krankheiten mit hohem Aspirationsrisiko höher. Aus diesem Grunde untersuchten wir den
klinischen Beitrag des Mittels Biobran MGN-3 als Prävention der Entwicklung von normalen
Erkältungen bei älteren Menschen, bei denen die Immunreaktion infolge verschiedener Faktoren
gesenkt ist.
Unter den Klienten der medizinischen Einrichtung „Atreyu Uozaki“ in Kobe, Präfektur Hjógó,
wurde in den Monaten Januar bis März 2002 eine Gruppe älterer Klienten ausgewählt, die keine
ernste Krankheit hatten und mit der Teilnahme an der Studie einverstanden waren. Getestet
wurde eine Nahrungsergänzung, eine Fraktion des Mittels Biobran MGN-3 (HRB). In der
Kontrollgruppe wurde Reisballaststoff benutzt, der vor allem wasserlösliche Bestandteile
(RB) enthielt.
Bezüglich der Erkältungssymptome (Fieber, Kopfschmerzen, Müdigkeit, Schüttelfrost, Husten,
Verschleimung, Ausfluss aus der Nase, verstopfte Nase, Halsschmerzen, Brustschmerzen) wurden
die Tage gezählt, an denen auch nur ein Symptom auftrat. Jedes Symptom wurde mit einer Zahl
nach seiner Intensität gekennzeichnet (nicht aufgetreten = 0, leicht aufgetreten = 1, mittel
= 2, stark = 3) und nachfolgend durch Teilen der Gesamtpunktzahl jedes Patienten durch die
Anzahl der Tage mit Einnahme des getesteten Stoffs die „symptomatische Punktzahl der
Erkältung“ ermittelt.
Ergebnisse: Unter den einzelnen Symptomen erschienen „Husten“, „Müdigkeit“
und „Halsschmerzen“ zu Beginn der Behandlung in beiden Gruppen in hohem Maße. In der Gruppe
HRB war die Gesamtanzahl der Tage, in denen die Symptome auftraten, gegenüber der Gruppe RB
kleiner. In der Gruppe RB wurde eine insgesamt höhere Punktanzahl der Erkältungssymptome
aufgezeichnet. Auch wenn die Punktanzahl der „Nasensymptome“ in der Gruppe RB niedriger war,
die Anzahl der Punkte der übrigen Symptome wie „Husten“, „Müdigkeit“ und „Fieber“ war höher.
Daraus wurde der Abschluss gefolgert, dass die Symptome einer normalen Erkältung in der
Gruppe HRB in geringerem Maße auftraten.
Die Studie wies nach, dass bei älteren Menschen mit normaler Erkältung bei oraler Einnahme
von HRB dank der immunstimulierenden Wirkung des Extrakts die Zeit der symptomatischen
Erscheinungen gekürzt wurde, sich die Symptome nicht verschlechterten und der Bedarf einer
symptomatischen Therapie gesenkt wurde.
Tazawa K. (Medizinische und pharmazeutische Universität Toyama, JAPAN): Magazin der
traditionellen Medizin, 20 (3), 2003
3.7. Antiallergische Wirkung
(a) Bewertung der präventiven Wirkung des Mittels Biobran MGN-3 und Linderung der
Asthmasymptome im Mausasthmamodell
Im Rahmen dieser Studie wurde die präventive Wirkung des Mittels Biobran MGN-3 und Linderung
der Asthmasymptome im Mausasthmamodell induziert mit Toluoldiisocyanat (TDI) verfolgt.
Zu Beginn wurde eine Lösung aus Trinkwasser und Biobran MGN-3 in Konzentration 2 g/l
hergestellt und in vier Gruppen (A-D) geteilten Mäusen (Männchen des Stamms BALB/c) gegeben:
Gruppe A: Biobran MGN-3 wurde einen Monat vor, während der
Sensitivierungsphase mit TDI und weiter über folgenden Zeitraum gegeben.
Gruppe B: Biobran MGN-3 wurde einen Monat vor und über die Zeit bis zum
Abschluss der Sensitivierungsphase mit TDI gegeben.
Gruppe C: Biobran MGN-3 wurde nur über die Dauer der Sensitivierungsphase
mit TDI gegeben.
Gruppe D: Kontrollgruppe.
In Gruppe B wurde die präventive Wirkung und in Gruppe C der Effekt der Symptomlinderung
bewertet. Die Wirkung des Mittels Biobran wurde nach Histaminkonzentration im Blut, Anzahl
der Eosinophile in bronchoalveoläre Lavage (BALF), Applikationstest TDI aus Ohrläppchen und
typenspezifischen Werten der Antistoffe IgG1, IgG2a, IgE im Blut während der Sensitivierung
bewertet.
Die höchste Konzentration des Bluthistamins wurde 7 Minuten nach Gabe TDI gemessen und war
wie folgt: Gruppe A: 2.5±0.53, Gruppe B: 4.2±0.75, Gruppe C: 4.3±7.8, Gruppe D: 6.4±0.87
(ng/ml), also wiesen die Gruppen, in denen Biobran MGN-3 gegeben wurde, gegenüber der
Kontrollgruppe bedeutend niedrigere Werte aus. Beim Testen der Sensitivität bei
verschiedenen TDI-Konzentrationen (0,01-10 %) kam es in den Gruppen mit Biobran MGN-3 zu
einer bis zu 10-100-fachen Verringerung der Sensibilität gegenüber der Kontrollgruppe.
Außerdem wurde in den Gruppen Biobran MGN-3 eine bedeutend niedrigere Menge Eosinophile im
BALF und auch niedrigere Werte im Applikationstest TDI ermittelt. Demgegenüber wurden in den
Werten der Blutantistoffe zwischen den einzelnen Gruppen keine bedeutenden Differenzen
verzeichnet.
Abschließend wird konstatiert, dass das Verabreichen von Biobran MGN-3 nachweislich
präventiv wirkt und durch Toluoldiisocyanat (TDI) induzierte Asthmasymptome im
Mausasthmamodell lindert. Die Studie deutet ebenfalls an, dass Biobran MGN-3 keinen Einfluss
auf die Bildung von Th2 induzierten Antistoffen des Typs IgG1 oder IgE hat und dass das
Mittel Suppressionsfaktor gegenüber Mastzellen hat.
Kobayashi H., Endo Y. (Universität Mc Master, KANADA) : Abstrakt des 52. Treffens der
Japanischen Gesellschaft der Allergologen, 2002
(b) Inhibierende Wirkung des Mittels Biobran MGN-3 auf die Progression atopischer Dermatitis
bei Mäusen NC
In dieser Studie wurde die Immunregulationswirkung des Mittels Biobran MGN-3 auf Mäuse NC
untersucht, bei denen sich natürlich ein erhöhter IgE-Spiegel im Serum und in Reaktion auf
die Sensitivierung mit Ovalbumin (OVA) eine Dermatitis ähnliche Hautläsion entwickelt.
Biobran MGN-3 wurde oral durch Trinken Mäusen NC gegeben, die danach mit der Kontrollgruppe
ohne Biobran MGN-3 verglichen wurden. Die Mäuse wurde anschließend mit Ovalbumin
sensitiviert. Blutproben wurde alle zwei Wochen vor und nach der Sensitivierung entnommen.
Die Gesamtmenge IgE und auch OVA der spezifischen IgE im Serum, ermittelt mit ELISA-Test,
waren bei mit Biobran MGN-3 behandelten Mäusen im Vergleich mit den Tieren der
Kontrollgruppe bedeutend niedriger. Außerdem, während sich bei den Mäusen NC ohne Biobran
MGN-3 atopischer Dermatitis ähnliche Hautläsionen entwickelten, traten bei den mit Biobran
MGN-3 behandelten Mäusen bei fünf von fünf Tieren keine solche Läsionen auf. Gleichzeitig
wurde konstatiert, dass Biobran MGN-3 inhibierend auf die Progression atopischer Dermatitis
bei Mäusen NC wirkt.
Nonoyama S. Universität für Medizin und Zahnmedizin in Tokio, JAPAN): Abstrakt des 11.
Treffens des Internationalen Kongresses der Immunologen, 2001
© Autorenrechte 2003: Hiroaki Maeda / Daiwa Pharmaceutical
(Dank für die Genehmigung, diesen Artikel auf den Seiten Biobran.org zu veröffentlichen.)
 Leiter der Forschungen zu
Biobran ist Dr. Mamdooh Ghoneum, Professor am Katheder Immunologie der Medizinischen und
naturwissenschaftlichen Universität Charles R. Drew in den Vereinigten Staaten. Dr.
Ghoneum, gegenwärtig internationale Kapazität im Bereich immuntherapeutische
Krebsbehandlung, erlangte den Titel PhD. der Radioimmunologie an der Universität in
Tokio und widmet sich seitdem dem Gebiet Immunologie an der Kalifornischen Universität
in Los Angeles. In den vergangenen 20 Jahren untersuchte er verschiedene Stoffe, welche
die Funktion des Immunsystems verbessern. Nach seinen Worten ist Biobran MGN-3 der
potenteste Immunkomplex, den er je getestet hat. Die Ergebnisse begeisterten ihn in
einem solchen Maße, dass er jetzt seine gesamte wissenschaftliche Aufmerksamkeit der
Behandlung mit dieser Verbindung widmet.
Leiter der Forschungen zu
Biobran ist Dr. Mamdooh Ghoneum, Professor am Katheder Immunologie der Medizinischen und
naturwissenschaftlichen Universität Charles R. Drew in den Vereinigten Staaten. Dr.
Ghoneum, gegenwärtig internationale Kapazität im Bereich immuntherapeutische
Krebsbehandlung, erlangte den Titel PhD. der Radioimmunologie an der Universität in
Tokio und widmet sich seitdem dem Gebiet Immunologie an der Kalifornischen Universität
in Los Angeles. In den vergangenen 20 Jahren untersuchte er verschiedene Stoffe, welche
die Funktion des Immunsystems verbessern. Nach seinen Worten ist Biobran MGN-3 der
potenteste Immunkomplex, den er je getestet hat. Die Ergebnisse begeisterten ihn in
einem solchen Maße, dass er jetzt seine gesamte wissenschaftliche Aufmerksamkeit der
Behandlung mit dieser Verbindung widmet.
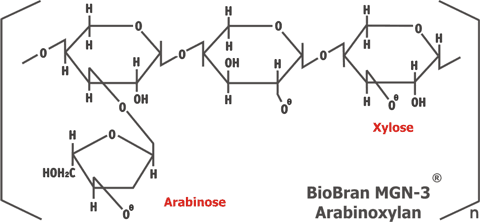 Legende: Arabinose > Xylose > Arabinoxylan Biobran MGN-3®
Legende: Arabinose > Xylose > Arabinoxylan Biobran MGN-3®
 Legende: Aktivität der NK-Zellen > Konzentration MGN-3 (µg/ml)
Legende: Aktivität der NK-Zellen > Konzentration MGN-3 (µg/ml)
 Legende: Aktivität der NK-Zellen (%) > Konzentration BioBran MGN-3
Legende: Aktivität der NK-Zellen (%) > Konzentration BioBran MGN-3

 Abb. 5:
Prozentueller Anteil der Bindungen zwischen den natürlichen Killern (NK-Zellen) und den
Zielzellen K-562. Legende: % Bindungen > Vor Einnahme > Nach Einnahme
Abb. 5:
Prozentueller Anteil der Bindungen zwischen den natürlichen Killern (NK-Zellen) und den
Zielzellen K-562. Legende: % Bindungen > Vor Einnahme > Nach Einnahme
 Abb. 6: Tödliche Formation der NK-Zellen und Zieltumorzellen.
Abb. 6: Tödliche Formation der NK-Zellen und Zieltumorzellen.
 Abb.7: peritoneale Mausmakrophagen (C3H/He)
Abb.7: peritoneale Mausmakrophagen (C3H/He)

 Abb. 10 Legende: Gewichtsprofil der Mäuse (in %)
Abb. 10 Legende: Gewichtsprofil der Mäuse (in %)
 Abb. 11
Abb. 11