3. A RIZSKORPÁBÓL KIVONT MÓDOSÍTOTT ARABINOXILÁN (Biobran) FIZIOLÓGIAI AKTIVITÁSA
3.1 Az immunrendszer működésének szabályozása
(a) Az emberi NK-sejtek aktivitásának növelése a rizskorpából nyert módosított arabinoxilán
(Biobran MGN-3) segítségével
1. In vitro vizsgálat
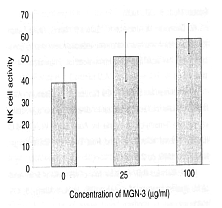
Patkányból származó NK-sejteket inkubáltak K-562 tumorsejtekkel (a célsejtekkel) Biobran
MGN-3 jelenlétében, és a feloldott K-562 tumorsejtek mennyiségét 51Cr-kibocsátásvizsgálattal
mérték. A feloldott mennyiség a Biobran MGN-3 koncentrációjától (25 μg/ml és 100 μg/ml)
függően nőtt, ami igazolta, hogy az NK-sejtek aktivitása a Biobran MGN-3 készítménynek volt
köszönhető.
2. In vivo vizsgálat (patkány)
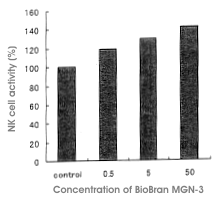
A Biobran MGN-3 készítményt szájon át juttatták be a Sprague-Dawly patkányok szervezetébe,
és két hét elteltével mérték az NK-sejtek aktivitását. A patkányokat három csoportra
osztották, mindegyikben 5 db patkány volt, ezek adagjai napi 0,5 mg, 5 mg és 50 mg/kg
voltak. Az NK-sejtek aktivitása a dózistól függően nőtt a Biobran MGN-3 készítmény
bevitelével. A kontrollcsoporttal összehasonlítva, az aktivitás-növekmény mértéke 119%, 130%
és 142% volt a 0,5 mg, 5 mg és 50 mg dózisú csoportok esetén. Az 50 mg dóziscsoportban az
aktivitás 132%-kal nőtt a kontrollcsoporthoz viszonyítva, az adagolás megkezdésétől
számított három napon belül. Az NK-sejtek aktivitásának a Biobran MGN-3 által elért
növekedését az NK-sejtek jobb megsemmisítőképességének tudhatnánk be, azonban ez az
NK-sejtek számától is függött. Némi hatáskülönbség jelentkezett a hím és nőstény patkányok
között - a nősténypatkányok esetén a hatás markánsabb volt (3. sz. ábra).
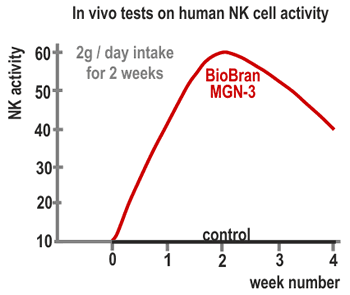
3. Az emberre kifejtett hatás
A Biobran MGN-3 készítmény 60 napos folyamatos alkalmazási vizsgálatát 24 egészséges
vizsgálati alanyon (15 nő, 9 férfi, átlagéletkoruk 34 év) végezték el, és figyelték az
NK-sejtek aktivitásának változását. A vizsgálati alanyokat három csoportra osztották,
mindegyikben 8 alany volt, ezek adagjai napi 15 mg/kg, 30 mg/kg és 45 mg/kg voltak. Minden
vizsgált személytől 20 cm3 vért vettek le: a Biobran MGN-3 bevitele előtt, egy héttel
később, egy hónappal később, két hónappal később (a vizsgálat befejeztével), valamint a
befejezést követő egy hónap elteltével; minden alkalommal mérték az NK-sejtek aktivitását. A
30 mg és 45 mg dóziscsoportokban az NK-sejtek aktivitása mintegy kétszeresére nőtt a bevitel
megkezdésétől számított egy héten belül, és háromszorosára két hónap alatt. A 15 mg
dóziscsoportban az aktivitás a kezdést követő egy hónap után gyorsan nőtt, és szinte azonos
szintet ért el, mint a 30 mg és 45 mg dóziscsoportokban, két hónap alatt. Egy hónappal a
bevitel beszüntetését követően az NK-sejtek aktivitása visszatért a bevitelt megelőző
szintre (4. sz. ábra). Az eredmények azt mutatták, hogy a Biobran MGN-3 készítmény 15-45
mg/kg/nap dózisban való bevitele befolyásolja az emberi NK-sejtek aktivitását.
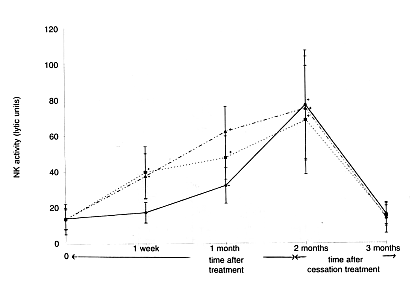
4. sz. ábra A természetes gyilkos sejtek (NK-sejtek) aktivitásának a Biobran
MGN-3 készítménnyel való viszonya az idő és a dózis függvényében a K562 tumorsejtekkel
szemben;
…_.._.._.._ = 45mg/kg/nap;
…………=30mg/kg/nap;
_______=15mg/kg/nap
4. A Biobran MGN-3 hatásmechanizmusa az NK-sejtek esetén
Az in vitro és in vivo vizsgálatok egyaránt kimutatták, hogy a Biobran MGN-3 által stimulált
NK-sejtekben megnőtt a citotoxikus granulák száma. Kutattuk a célsejtek kötődési
képességének növekedését is. Egy, 30 napon át 45 mg/kg/nap dózisban Biobran MGN-3
készítményt szedő személy NK-sejtjeit K-562 célsejkekkel inkubálták, majd mérték a kötődési
képesség növekményét. Miután az NK-sejtek és a K-562 tumorsejtek 4°C hőmérsékleten egy óráig
inkubálódtak, megmértek 200 NK-sejtet és kiszámították a a K-562 sejtek kötődési
képességének mértékét. A Biobran MGN-3 készítményt szedő személy NK-sejtjeinek a
célsejtekhez (K-562) való kötődési képessége jelentősen javult: 38,5%-ra, a szedést megelőző
9,4%-kal szemben (5. sz. ábra). A kötődés jellegzetes esete a 6. számú ábrán látható.
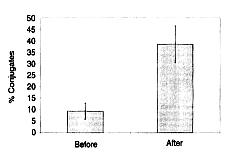 5. sz. ábra: A természetes gyilkos sejtek (NK-sejtek) és a K-562 célsejtek
közötti konjugátum-képződés százalékaránya.
5. sz. ábra: A természetes gyilkos sejtek (NK-sejtek) és a K-562 célsejtek
közötti konjugátum-képződés százalékaránya.
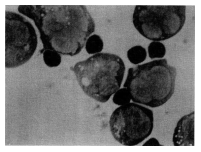 6. sz. ábra: A természetes gyilkos effektorsejtek (NK-sejtek) - tumor
célsejtek konjugátumának képződése.
6. sz. ábra: A természetes gyilkos effektorsejtek (NK-sejtek) - tumor
célsejtek konjugátumának képződése.
Ghoneum M. (Drew Egyetem, USA) :INT. IMMUNO THERAPY XIV (2) PP. 89-99, 1998
(b) a Biobran MGN-3 in vitro hatása a makrofág sejtekre
Vizsgálták a Biobran MGN-3 hatását a makrofág sejtekre, a farmakológiai mediátorok
termelésének indukálása tekintetében. A TNF-a, az IL-6 és az NO anyagokat mediátorként
vizsgálták. A makrofág sejteket a Biobran MGN-3 különféle koncentrációi (1-100µg/ml) mellett
inkubálták, a szupernatánsokat pedig mediátorvizsgálat címén összegyűjtötték. Vizsgálták a
TNF-a citotoxicitását az L929 sejtvonalra, az IL-6 citózisát a B13.19 sejtvonalra, ill. az
NO-t kolorimetriás vizsgálatnak vetették alá - az utóbbinak a Griess-reagenssel való
reakcióját vizsgálták. Az LPS volt a pozitív kontrollcsoport.
- Az egerek RAW264.7 makrofág sejtvonala esetén a Biobran MGN-3 erős aktivitást
mutatott a 10µg/ml-t meghaladó koncentrációk esetén, mindhárom mediátor kapcsán.
- Egérből származó peritoneális makrofágok (C3H/He). A Biobran MGN-3 hatása az egerek
peritoneális üregéből vett makrofágok esetén a 7. sz. ábrán látható. A Biobran MGN-3
ebben az esetben is nagyfokú aktivitást mutatott 10µg/ml feletti koncentráció
alkalmazása mellett.
- U937 emberi makrofág sejtvonal. A Biobran MGN-3 erős aktivitást indukált, ahogyan az a
TNF-a és az IL-6 citokinek termelésén látszott, amely az LPS értékeivel volt egyenlő
100µg/ml dózis mellett.
Az eredmények azt mutatják, hogy Biobran MGN-3 a normál egér- vagy emberi makrofágok
aktiválásának hatékony eszköze. A tanulmányok szerint aktív koncentrációnak a 10µg/ml
feletti koncentráció tekinthető.
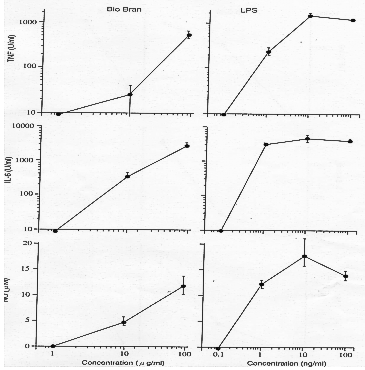 7. sz. ábra: Egérből származó peritoneális makrofágok (C3H/He egerek).
7. sz. ábra: Egérből származó peritoneális makrofágok (C3H/He egerek).
(c) Az immunrendszer stimulálása és a rák megelőzése
Számos tanulmányban szerepel, hogy a munkahelyen jelenlevő különféle vegyi anyagok az ott
dolgozók esetében fokozzák a rák kialakulásának veszélyét. Tanulmány készült a mérgező vegyi
anyagok hatásának kitett immunrendszer változásairól is, ill. arról, hogyan ellensúlyozható
a Biobran MGN-3 készítmény segítségével ezek káros hatása.
A tanulmányban tizenegy olyan személy vett részt, akik munkahelyükön vegyszereknek voltak
kitéve. A tanulmányban részt vevők az immunrendszer helytelen működését mutatták, ami a
következőkből tűnt ki: a természetes gyilkos sejtek (NK-sejtek) aktivitásának alacsony
szintje (10.2±4.2 LU), a limfociták blasztogén válaszreakciója a T-sejtek mitogénjeire (PHA,
39060±12517cpm és COMA, 36224±11922cpm) és a B-sejtek mitogénjeire (PWM, 16550±6330cpm), a
kontroll válaszreakciókkal összehasonlítva. A vizsgálat alanyai négy hónapig 15 mg/kg/nap
dózisban kapták a Biobran MGN-3 készítményt. A Biobran MGN-3 készítménnyel való kezelés az
NK-sejtek aktivitását 4×, ill. 7× növelte 2, ill. 4 hónap leforgása után, míg a T- és
B-sejtek működése 130-150%-kal túllépte az alapszintet.
Ghoneum M. (Drew Egyetem, USA): A 7. nemzetközi öregedést gátló és orvosbiológiai
technológiákról szóló konferencia összefoglalója, 1999.
(d) A TNF-α és IF-γ termelése az emberi PBL-ből Biobran MGN-3 módosított arabinoxilán -
rizskorpa-kivonat segítségével.
A kutatók azt a mechanizmust vizsgálták, amellyel a Biobran MGN-3 készítmény növeli az
NK-sejtek citotoxikus aktivitását. Ezt a Biobran MGN-3 az alfa tumor nekrotizáló faktor
(TNF-α) és a gamma (IFN-γ) szekréciójának szintjére, valamint a kulcsfontosságú sejtfelületi
receptorok expressziójára kifejtett hatásának vizsgálatával vizsgálták.
A perifériás vér limfocitáit 0,1 mg/ml és 1 mg/ml koncentrációjú Biobran MGN-3 készítménnyel
kezelték, a szupernatánsokat enzimekhez kötött immunoszorbens vizsgálatnak vetették alá. Az
eredmények kimutatták, hogy a Biobran MGN-3 a TNF-α indukálásának hatékony anyaga, és a
hatás dózisfüggő volt. A 0,1 mg/ml és 1 mg/ml koncentrációjú Biobran MGN-3 a TNF-α-termelést
22,8×, ill. 47,1× növelték. A Biobran MGN-3 növelte az IFN-gamma termelését, azonban kisebb
mértékben, mint a TNF-alfa. A kulcsfontosságú sejtfelületi receptorok kapcsán a Biobran
MGN-3 növelte a CD69, egy korai aktivációs antigén expresszióját, a kezelést követő 16
órával. Ezen felül a CD25 interleukin-2 receptor és az ICAM-1 (CD54) adhéziós molekula
szintjét a Biobran MGN-3 készítménnyel való kezelés upregulálta. A nagyfokú tisztaságú
NK-sejtek Biobran MGN-3 készítménnyel való kezelése szintén a TNF-alfa és az IFN-gamma
szekréció magasabb értékeit mutatta az NK-sejtek citotoxikus funkciójának növekedésével.
Ezen túl a Biobran MGN-3 készítmény hozzáadása az interleukin-2 által aktivált NK-sejtekhez
a TNF-α és IFN-γ kiválasztás szinergikus indukcióját eredményezte.
Ghoneum M. (Drew Egyetem, USA), Jewett A. (UCLA, USA): Cancer Detection and Prevention [Rák
azonosítása és megelőzése] 24. évf./4. kiadás, 2000
(e) A rizskorpából származó módosított arabinoxilán hatása az emberi perifériás vér
limfocitáinak NK-aktivitására.
A Biobran MGN-3 és molekuláris részei NK-sejtek aktivitására kifejtett hatást is vizsgálták.
A nagy molekulatömegű frakciót (molekulatömeg: 10-50 kDa), amelyet gélfiltrációs technikával
állítottak elő Sephadex G-25 és G-75 segítségével, hozzáadták az emberi perifériás vér
limfocitáihoz. 3 napnyi inkubáció után meghatározták az NK-sejtek aktivitását. A
fluoreszcens anyaggal megjelölt K-562 sejtvonal voltak a célsejtek, az aktivitást a Tere
Scan berendezéssel, fluoreszcenciás módszerrel határozták meg. Azonos kísérlet került
elvégzésre az IL-2 jelenlétében.
Ezekben a kísérletekben nem jelentkeztek szignifikáns különbségek az NK-sejtek
aktiválásában, sem a Biobran MGN-3 részéről, sem a nagy molekulatömegű frakció részéről. Ha
azonban az IL-2 hozzáadása és inkubálása azonos időben történt, megnövelt NK-aktivitást
tapasztaltak, összehasonlítva az IL-2 egyedüli alkalmazásával. Ez azt mutatja, hogy a
Biobran MGN-3 az NK-sejteket az IL-2 jelenlétében aktiválja, és hogy az ilyen jellegű
aktivitás a nagy molekulatömegű frakcióban is jelen van.
Ueda Y., Shimomura C. (Chiba Egyetem, Japán): A japán biotudományi, biotechnológiai és
agrovegyészeti társaság 2002. évi éves gyűlésének összefoglalója
3.2. Antivírusos hatás
A Biobran MGN-3 in vitro anti-HIV aktivitása
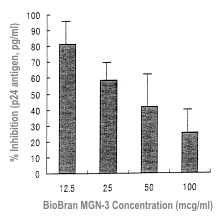
A Biobran MGN-3 anti-HIV aktivitását in vitro vizsgálták. Először is, vizsgálták a HIV-1 p24
antigén termelését gátló hatást. A három egészséges személytől begyűjtött mononukleáris
sejteket a HIV-1 SF lánccal 37°C hőmérsékleten egy óráig, Biobran MGN-3 jelenlétében
inkubálták. A Biobran MGN-3 dózisok nagysága 0-100 μg/ml volt. A Biobran MGN-3
koncentrációfüggő módon gátolta a HIV-1 p24 antigén termelését (8. sz. ábra).
A következő lépésben vizsgálták a szincitium-képződést gátló hatást. Öt AIDS pácienstől
begyűjtött mononukleáris sejteket PHA-val 37°C hőmérsékleten hét napig, Biobran MGN-3
jelenlétében inkubálták. A Biobran MGN-3 dózisok nagysága 0-100 μg/ml volt. A Biobran MGN-3
koncentrációfüggő módon gátolta a szincitium-képződést, a maximális gátló hatás mértéke 75%
volt, 100 μg/ml mellett 7) (1. sz. táblázat).
 |
|
1. sz. táblázat
| A Biobran szincitium-képződést gátló hatása |
| Biobran dózis (μg/ml) |
Szincitium-képződés (SF) |
| SF sorszám |
Gátlás % |
0
12.5
25
50
100
|
42.0±8
25.8±7
21.5±5
15.8±4
10.5±3
|
00.0
38.5
50.0
62.5
75.0
|
|
| 8. sz. ábra |
|
|
Ghoneum M. (Drew Egyetem, USA): Biochemical and Biophysical Research Communications
[Biokémiai és biofizikai kutatások] 243, (1998)
3.3. Tumorellenes hatás
(a) A rákos sejtek növekedésgátló alkotóeleme növekedésének vizsgálata a módosított
rizskorpából nyert arabinoxilánból származtatott sejtvonal-kultúrák esetén
Ebben a tanulmányban a Biobran MGN-3 - módosított rizskorpából nyert arabinoxilán
növekedésgátló hatását vizsgálták különféle rákos sejtvonalak tekintetében - HL60, K562, HLE
- valamint a HL60 és K562 potenciális differenciáció-indukálását. A kultivált sejtvonalakhoz
Biobran MGN-3 készítményt adtak. 3 napos inkubálás után az élő sejtek aránya minden
sejtvonalban csökkent a növekvő Biobran MGN-3 mennyiséggel.
Az etanolos precipitáció után a precipitátumot desztillált vízzel elegyítették, majd a
szupernatánst Sephadex G-25 toronnyal bontották frakciókra. Három (A, B, C) frakcióra
bontották, amelyeket a kultivált sejtvonalakhoz adtak. A növekedésgátló hatás a C frakció
esetében a HL60 és K562 sejtvonalaknál, a B és C frakciók esetében pedig a HLE sejtvonalnál
jelentkezett. Ezen felül a Giemsa-festés és a nem specifikus eszteráz festés kimutatta a
potenciális differenciáció-indukciót a HL60 és K562 esetén. Ezek az eredmények azt mutatják,
hogy a Biobran MGN-3 alkotóelemei a rákos sejtekre növekedésgátló hatással vannak, a HL60 és
K562 sejtvonalak esetében pedig potenciális differenciálás-indukáló hatással bírnak.
Masada M. (Chiba Egyetem, Japán): A japán biotudományi, biotechnológiai és agrovegyészeti
társaság 2002. évi éves gyűlésének összefoglalója
(b) A Biobran MGN-3 hatékonysága a tumorsejtek növekedésének gátlásában
A Biobran MGN-3 hatását vizsgálták a bőrrákot okozó sejtek növekedésére és a
citokin-termelésre. A pikkelyes sejt karcinóma [SCC13] sejtvonalának inkubációja Biobran
MGN-3 készítmény jelenlétében leállította a sejtnövekedést (30% sejtszám-csökkenés 48 óra
elteltével és 50% 72 órányi kultiváció után) a kizárólag MEM közegben tenyésztett SCC13
kontroll sejtcsoporttal szemben, amely tovább növelte a sejtszámot.
Az átfolyásos citometriai eljárások és elemzések kimutatták, hogy az SCC13 sejtek Biobran
MGN-3 általi kezelését követően 16 órával 5× növekedés jelent meg az interleukin 10 [IL-10]
intracelluláris szintjében, azonban a gamma interferon [INF-gamma] szint evidens változása
nem következett be. Az ELISA 8× magasabb IL-10 szinteket és 3× IL-12 szintet mutatott ki az
SCC13 kultúrában. Kevés változás volt észlelhető az INF-gamma koncentrációban. Vizsgálták a
Biobran MGN-3 hatását az egyéb sejtvonalakra is, mint amilyenek a normál és daganatos
emlősejtek, valamint a rákos prosztata sejtek.
Ezek az eredmények azt mutatják, hogy a Biobran MGN-3 nemcsak az immunrendszert erősíti,
hanem közvetlenül módosítja a tumorsejtek növekedését és a citokinek termelését. Ezek az
eredmények egy olyan hatásmechanizmusra utalhatnak, amely megmagyarázná a nagyfokú klinikai
sikereket és a Biobran MGN-3 kezelés kedvező hatásait, amelyeket a szerző a 4 éves időszak
során tapasztalt.
Ghoneum M. (Drew Egyetem, USA): A 8. nemzetközi öregedést gátló és orvosbiológiai
technológiákról szóló konferencia összefoglalója, 2000.
3.4. Komplementer hatás a rákkezelésben
(a) az NK-sejtek aktivitásának és a túlélési ráta értékelése a többszörös immunterápia
esetén, különféle rákos betegek kapcsán.
Készítettek egy tanulmányt, amelynek célja az volt, hogy megállapítsák, a Biobran MGN-3
készítmény alkalmazása elősegíti-e az élet meghosszabbodását és javíthatja-e az
életminőséget 205 progresszív és részlegesen áttétes rákos páciens esetén, akik sebészeti
beavatkozás után, a betegség késői, III.-IV. stádiumában voltak. A klinikai tanulmány
alanyai a Sano sebészeti klinika (Japán) fekvőbetegei voltak. Komplementer alternatív
gyógyszerekkel és kis mellékhatású hagyományos rákellenes gyógyszerekkel kezelték őket.
A 205 páciens 6 hónapig részesült fekvőbeteg-ellátásban, két csoportra osztva. 109 pácienst
(a kontrollcsoportot) a klinika standard komplementer alternatív gyógyszereivel kezeltek,
míg 96 páciens ezen felül másfél évig szedte a Biobran MGN-3 készítményt (Biobran MGN-3
csoportot).
Minden páciens esetén a természetes gyilkos sejtek aktivitását mérték mint az immunrendszer
paraméterváltozásának indikátorát. Ezzel párhuzamosan a páciensek életminőségét is
vizsgálták. A sebészeti beavatkozás után lévő páciensek NK-aktivitása átlagban alacsony
volt, azonban a Biobran MGN-3 alkalmazásával az NK-sejtek aktivitásának növekedése és az
élet meghosszabbodása volt megfigyelhető. Minél magasabb a páciensnél az NK-sejtek
aktivitása, annál magasabb az életkor megfigyelt meghosszabbodása. (2. sz. táblázat) Az
eredmények azt mutatták, hogy az NK-sejtek aktivitása a progresszív rákos megbetegedések
patológiai mutatója lehet. A Biobran MGN-3 készítmény alkalmazása esetén az életminőség
javulását is tapasztalták.
2. sz. táblázat: A teljes túlélési ráta, az NK-sejtek aktivitása és a két csoport túlélési
rátái közötti viszony
| Csoport |
Biobran csoport |
Kontrollcsoport |
| Teljes túlélési ráta |
52/96 (54.2%) |
19/63 (33.9%) |
NK-aktivitás kategória
19,9% alatti
20%-40%
40% feletti
|
17/40 (42.5%)**
18/35 (51.4%)*
17/21 (81.0%)
|
2/16 (12.5%)
7/25 (28.0%)
10/15 (66.7%)
|
Szignifikáns % a kontrollcsoporthoz viszonyítva **p<0.01 *p<0.05
Takahara K. (Sano sebészeti klinika, Japán) : A Japán komplementer és alternatív
gyógyszerek/kezelések társaságának 3. éves összejövetelének összefoglalója
(b) a Biobran MGN-3 immunomodulátori és rákellenes tulajdonságai öt emlőrákos páciens
esetén
5 emlőrákos páciens napi 3 g dózisban kapott Biobran MGN-3 készítményt, és az NK-sejtjeik
aktivitását 4 órás 51Cr- kibocsátás vizsgálattal mérték, amelyben a K-562 tumorsejtek voltak
a célsejtek. Az eredmények kimutatták a következőket:
-
Azon páciensek esetén, akiknél a bazális NK-sejtaktivitás alacsony (12.7-58.3%),
és az effektor : célsejt (E:T) arány 12 és 100:1, az NK-sejtek aktivitása jelentősen
nőtt a Biobran MGN-3 kezelés hatására (41.8-89.5%) azonos E:T arány esetén.
-
Az NK-sejtek aktivitásának növekedése a kezelést követő 1-2 héten belül
jelentkezett, és a Biobran MGN-3 további alkalmazásával tovább nőtt.
-
Két páciensnél, akik a tanulmány kezdeti időszakában (6-8 hónapig) vettek részt,
teljes mértékű remisszió állt be.
Ghoneum M. (Drew Egyetem, USA): Az Amerikai Rákkutatási Szövetség speciális konferenciájának
összefoglalója, 1995
(c) NK-immunomodulátor funkció 27 rákos páciensnél a Biobran MGN-3, egy rizskorpából nyert
módosított arabinoxilán hatására.
27 rákos páciens esetében vizsgálták a Biobran MGN-3 immunomodulátor funkcióját. A páciensek
különféle típusú előrehaladt malignanciával rendelkeztek: 7 páciensnél jelentkezett emlőrák,
prosztatarák 7 esetben, 8 esetben mielóma multiplex (MM), 3 esetben leukémia és 2 esetben
méhnyakrák jelentkezett. Minden pácienst hagyományos terápiával kezeltek, akik ezek mellett
napi 3 g mennyiségű Biobran MGN-3 készítményt fogyasztottak; a kutatók megmérték az
NK-sejtek aktivitását 2 hét, 3 hónap és 6 hónap leforgása után. Az NK-sejtek aktivitását az
51Cr-kibocsátás vizsgálattal, K562 tumorsejtek célsejtként való alkalmazásával, 12:1 - 100:1
effektor : célsejt arány mellett vizsgálták. Az eredmények kimutatták a következőket:
-
A páciensek bazális NK-aktivitása alacsony volt.
-
A Biobran MGN-3 készítménnyel való kezelés figyelemreméltó NK-aktivitás-növekményt
hozott
2 hét után. Az indukció százalékaránya a következő volt: emlőrák 154-332%, prosztatarák
174-385%, leukémia 100-240%, MM 100-537%, ill. méhnyakrák 100-275%.
-
Az NK-sejtek aktivitásának növekedése a kezelést követő 3 hónappal és 6 hónappal is
nőtt.
Ghoneum M. (Drew Egyetem, USA): Az Amerikai Rákkutatási Szövetség 87. éves találkozójának
összefoglalója, 1996
(d) Esettanulmány - a Biobran MGN-3 kiegészítő kezelésként jelent meg a tüdőrák áttéteinek
gyógyítása során.
Egy eset, amely során kedvező eredmény született, amikor a Biobran MGN-3 készítményt a
tüdőből a jelen tanulmányban bemutatott csontokra is átterjedő tüdőrákkezelés
kiegészítéseként alkalmazták.
A páciens egy 67 éves férfi. 1996 augusztusában orvoshoz fordult testtömegének drasztikus
csökkenése miatt, súlyos köhögésre és felköhögésre panaszkodva. A diagnózis tüdőrák
komplikációja (pikkelyes sejt karcinóma) és tuberkulózis (M. tuberculosis). A tuberkulózis
antibiotikumos kezelése után a tüdőrák sugárkezelése októberben kezdődött, a tuberkulózis
kezelésével egy időben. Azonos év decemberében jobb tüdejének alsó részét kivágták, a tumort
eltávolították. A sugárkezelést követően 1997 januárjában hazaengedték a kórházból.
Azonos év júniusában ismételten orvoshoz fordult, a mellkasának jobb részében érzett
fájdalom miatt. A csontszcintigráfia segítségével készített diagnózis szerint többszörös
áttétek igazolódtak be csontjaiban. A tumor főként mellkasának jobb oldali bordáiban terjedt
szét, azonban egész testének csontozatában megjelentek az áttétek. Júliustól kezdődően
fájdalomcsillapítóként folyamatos felszívódású morfiumot alkalmaztak nála. Időközben
megkezdték a Biobran MGN-3 készítmény alkalmazását napi 3 g mennyiségben, május végétől
kezdődően. 1998 januárjától kezdődően a fájdalmai csökkentek. A Biobran MGN-3 készítmény
folyamatos alkalmazása során a folyamatos felszívódású morfium mennyiségét fokozatosan
csökkentették, júniusban a morfium adagolását teljes mértékben megszüntették. Az ICPP
tumormarker értéke 16.8ng/ml volt, amikor beigazolódott a rekurrencia és fokozatosan
lecsökkent 7.6ng/ml értékre (1997 decembere), ill. 6.7ng/ml értékre (1998 júliusa). A
csontszcintigráfia figyelemreméltó javulást mutatott, és a csontozatban a tumor áttéteinek a
visszahúzódása volt megfigyelhető. Az NK-sejtek aktivitása a betegség rekurrenciája idején
alacsony, 9,0% volt, azonban fokozatosan nőtt és jelenleg magas.
Sobajima T. (Hoshigaoka Kosei Nenkin Kórház, Japán): A Japán komplementer és alternatív
gyógyszerek/kezelések társaságának 2. éves összejövetelének összefoglalója, 1999
(e) A Biobran MGN-3 alkalmazása a hagyományos kezelést követő időszakban
Az alvó tumor- kezelés koncepciója Japánban a rákkezelés egyik vezető koncepciójává válik.
Az alapvető kezelési elv a páciens életének meghosszabbítása a magas életminőség megtartása
mellett. Dr Tunekawa a kezelést a páciens kérésére hajtja végre és életminőségének javulását
fontos terápiás célként jelölte meg. Előadta, hogy 34 rákbetege van, akik nyugvó
kemoterápiás, komplementer és alternatív gyógyszerek (CAM) kombinációját kapják, és ezek
közül három esetben leírta a kezelés folyamatát:
-
Páciensek (elsődleges betegség): gyomorrák 3 esetben, tüdőrák 3 esetben,
rosszindulatú limfóma 2 esetben, bél- (végbél-)rák 6 esetben, emlőrák 3 esetben és
egyéb 17 esetben.
-
kezelési időszak: 6-18 hónap
-
Esettanulmányok
-
T.S. (60), nő, gyomorrák (IV.stádium), Rákos hashártyagyulladás: A pácienst 2000
januárjában műtötték gyomorrák miatt. 2000 februárjában rákos hashártyagyulladás
lépett fel nála és gasztrektómián esett át a IV. stádiumban. A CA19-9 értéke 108
volt. 2000 augusztusában ellátogatott klinikánkra, hasi fájdalomra, székrekedésre,
anémiára és anorexiára panaszkodva. A CA19-9 értéke 390 volt, az NK-sejtek
aktivitásának értéke pedig 25,6. TS1 és holisztikus kezelés kombinációjában
részesült. Az immunrendszer erősítése érdekében napi 3 g Biobran MGN-3 készítményt
kapott. Egy hónap elteltével a CA19-9 értéke már csak 63 volt. A tumormarkerek
fokozatosan csökkentek nála, és növekedett az NK-sejtek aktivitása. 2001
augusztusában, 11 hónappal később a CA 19-9 marker értéke 25, az NK-sejtek
aktivitása 51,5 volt. Szinte nem maradtak fenn szubjektív tünetek, jelenleg rendesen
táplált.
-
F.A. (46 éves), nő, emlőrák, áttétek a derékcsigolyákon és a méhben. A pácienst 1998
júliusában műtötték emlőrák miatt, hormon- és rákkezelést kapott. 2001 márciusában a
derékcsigolyáin, 2001 áprilisában a méhén találtak áttéteket, 2001 májusában
hiszterektómián esett át. A kórházból hazaengedték, Taxol és Paraplatin szedése
mellett. 2001 júliusában meglátogatta Dr. Tunekawa-t, csontfájdalmakra panaszkodva.
Abban az időben CA értéke 153, az NCC-ST értéke 439 és az NK-sejtek aktivitása 9,3
volt. A Paraplatin-kezelés folytatódott, és megkezdték nála a holisztikus terápiát.
Az immunrendszer erősítése érdekében napi 3 g Biobran MGN-3 készítményt kapott. Két
hónappal később a CA értéke 18, az NCC-ST értéke 28,9, az NK-sejtek értéke 22,0
volt, és a fájdalom megszűnt. Ezt követően a tumormarkerek fokozatosan csökkentek
nála, és növekedett az NK-sejtek aktivitása. 2002 júliusában a CA értéke 14, az
NCC-ST értéke 3,2, az NK-sejtek aktivitásának értéke 59 volt, nem voltak fájdalmai
és a csont- szcintigráfia leletei kevésbé voltak markánsak. Jelenleg jól táplált,
nagy élvezettel dobol.
Tunekawa H. (A Holisztikus Orvoslás Népszerűsítésének Tokai Társasága, Japán): A
Biobran-műhely kiadványa, Berlin, 2002
(f) a Biobran MGN-3 vizsgálata a progresszív rák kezelésében
Dr.Mizukami 97 előrehaladott állapotú rákbetegnek adott Biobran MGN-3 készítményt. A kezelt
ráktípusok: gyomor-, vastagbél-, emlő-, tüdő-, hasnyálmirigy-, máj-, epevezeték-, garat-,
petefészekrák, a méhnyak nyálkahártyamirigyeinek rákja, méhtest-, vese-, pajzsmirigy-,
prosztata-, szájüregrák, mielóma multiplex, stb. Bár a páciensek már részesültek műtétben,
kemoterápiában, radioterápiában, stb. nagy kórházakban, többségüknél gyenge volt a javulás.
Áttétek és rekurrencia jelent meg náluk, immunterápiát kértek és felkeresték Dr. Mizukami
kórházába. A Biobran MGN-3 alkalmazási példáiban szinte sosem alkalmaztak párhuzamosan sem
kemoterápiát, sem sugárterápiát. Részletes klinikai megfigyelést végeztek és kérdéseket
tettek fel a Biobran MGN-3 készítményt szedő páciensek életminőségével kapcsolatban.
Megfigyelték a Biobran MGN-3 készítményt szedő páciensek esetén fellépő azonos jelenségeket.
Bizonyos esetekben a Biobran MGN-3 készítmény alkalmazása esetén az életminőség látható
javulását is tapasztalták. Általában, bár az előrehaladott rákos betegek életminősége az idő
előrehaladtával egyenes arányban csökken, a Biobran MGN-3 készítményt alkalmazó páciensek
ezt a tendenciát korlátozott mértékben mutatták, és általában tovább éltek, jó életminőség
mellett. Hosszú idejű túlélést is tapasztaltunk.
Az életminőséggel kapcsolatban a következő konkrét megfigyeléseket tették:
-
Bár az éles fájdalom ellenőrzése nem egyszerű, és az előrehaladott rákos betegek
közül sok esetében morfiumot kellett alkalmazni, a Biobran MGN-3 készítményt szedők
közül egyeseknek nem volt szükségük morfiumra. Még morfium alkalmazása esetén is
kisebb morfiummennyiségeket tapasztaltunk.
-
Összességében az erőtlenség érzésének csökkent tendenciáját tapasztalták.
-
Az étvágytalanság érzésének csökkent tendenciáját tapasztalták.
-
Megfigyelték, hogy közvetlenül a halál előtt is az otthonukban maradhattak a
betegek, és jó volt a közérzetük.
-
A tudat tisztaságának megőrzését, valamint a családdal való beszélgetés képességének
tendenciáját tapasztalták.
Dr. Mizukami úgy találta, hogy az előrehaladott rákos betegek esetében az, hogy az
életminőség nem csökken drasztikusan a Biobran MGN-3 készítmény szedése esetén, fontos a
rákgyógyítás szempontjából.
Mizukami O. (Egészségpromóció kutató intézet, New Life Layman Alapítvány, Japán): A
Biobran-műhely kiadványa, Berlin, 2002
3.5. Az apoptózis hatása
A Biobran MGN-3 érzékennyé teszi az emberi T-sejt leukémia sejteket a halálreceptor (C95)
által indukált apoptózisra
A tanulmányban a Biobran MGN-3 hatását vizsgálták az emberi leukémia HUT 78 sejtvonalának a
halálreceptor által indukált apoptózisára. A HUT 78 sejteket előzetesen Biobran MGN-3
készítménnyel kezelték, majd a halálreceptor agonisztikus antitestével (Fas, CD)inkubálták.
Az apoptózis mértékét a propidium-jodid technikával, FACScan alkalmazásával állapították
meg. A kaszpáz-3, kaszpáz-8 és kaszpáz-9 aktiválását átfolyásos citometria segítségével
állapították meg. DIOC6 festékanyaggal, FACScan segítségével megmérték a mitokondriális
membránpotenciált. A CD95 és BCI-2 expresszióját átfolyásos citometria segítségével
állapították meg.
A Biobran MGN-3 növelte az anti-CD95 által indukált apoptózist, dózisfüggő módon. A
megnövekedett sejthalandóság a mitokondriális membránpotenciál megnövekedett
depolarizációjával és a kaszpáz-3, kaszpáz-8 és kaszpáz-9 megnövekedett aktivitásával
korrelált. A Biobran MGN-3 általi kezelés nem hatott a CD95 expressziójára, azonban
csökkentette a BCI-2 expresszióját. Az eredmények azt sugallják, hogy a Biobran MGN-3 növeli
a rák fogékonyságát a halálligandumok által közvetített apoptózisra, ami releváns lehet a
rákellenes aktivitás esetén.
Ghoneum M. (Drew Egyetem, USA): Cancer Letter [Rákkutatók lapja], 2003
3.6. A szervezet védekező rendszerének aktiválása
(a) Aktív oxigéngyökök Biobran MGN-3 általi scavengelése
Vizsgálták a Biobran MGN-3 oxigéngyökök és azok frakcióinak scavengelésére vonatkozó
képességét. A Biobran MGN-3 készítményt egy Sephadex G-25 készülék segítségével
alkotóelemeire bontották. Minden alkotóelemét elneveztek: csökkenő sorrendben L (L > 10,000
molekulatömeg), M (10,000 > M > 3,000 molekulatömeg) és S (3,000 molekulatömeg > S).
Az aktív enzim scavengelő tevékenységet a következőkkel mérték: a szuperoxid-aniongyök (-O2)
scavengelésének mérésével, a Fenton-reakció hidroxilgyök scavengelésének mérésével (-OH),
valamint az ultraibolya sugarak által előállított hidroxilgyök scavengelésének mérésével.
A mérések eredményei a táblázatban láthatóak. Az S (alacsony molekulatömegű) frakció
túlszárnyalta a többit az -O2 és az UV fény által generált -OH inhibíció területén.
Nagymértékű scavengelést tapasztalnak minden frakció esetén a Fenton-reakció által generált
-OH-scavengelés területén. (3. sz. táblázat)
3. sz. táblázat
Biobran MGN-3 aktív oxigéngyök-scavengelése
(•O2 és •OH, valamint UV által indukált •OH)
| Aktív oxigén és SOD aktivitás típusa |
szuperoxid-anion gyökök scavengelésének aránya (%) |
SOD aktivitás (U/ml) |
UV-indukálású hidroxil-gyökök scavengelésének aránya (%) |
| 20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
BioB
BioB-L
BioB-M
BioB-S
|
64.6
39.9
49.5
90.4
|
23.0
10.4
15.6
68.1
|
4.4
0
0
26.4
|
7.6
5.0
7.2
70.5
|
0.9
0.8
1.4
15.7
|
0
0
0
2.6
|
94.9
(72.6)
97.2
(41.8)
97.0
(45.4)
96.5
(71.0
|
78.9
(35.9)
34.4
(16.5)
68.4
(9.9)
55.1
(54.9)
|
3.3
(11.5)
3.3
(1.0)
8.7
(3.9)
4.2
(19.6)
|
·O2:HPX-XOD reakció,·OH:Fenton reakció
·OH UV fény hatására történő reakció: 365nm,4×103J/m2/min×5
Tazawa K. (Toyama Orvosi és Gyógyszerészeti Egyetem, Japán): Biotherapy [Bioterápia] 14.
évfolyam, 2000
(b) Tanulmány az arabinoxilán összetevőnek a szervezet védekező rendszerére kifejtett
aktivációs hatásáról.
Ebben a tanulmánybanállatkísérletben igazolták a Biobran MGN-3 készítménynek a
lipopoliszacharid (LPS) által indukált halálos szepszis modellben észlelt túlélési rátát
érintő befolyását.
A kísérletben BALB/c (hím, 5-7 hetes) egereket alkalmaztak. 20mg/kg és 200 mg/kg Biobran
MGN-3 készítményt 0,5 ml PBS oldatban feloldva, orális szondán keresztül adtak be nekik
minden második napon, két héten keresztül, összesen hét alkalommal. A kontrollcsoport szájon
át 0,5 ml PBS oldatot kapott orálisan, azonos intervallumokban.
12 órával a befejező orális bevitelt követően az egerek 200 μg/egér adagban LPS-t kaptak
intraperitoneálisan, majd megfigyelték az egerek állapotváltozásait. Egy másik kísérletben
az egerek 100 μg/egér mennyiségű LPS-t kaptak intraperitoneálisan a Biobran MGN-3 csoportban
és a kontrollcsoportban egyaránt - az egereket az LPS bevitele után 0, 2, 4, 8 órával
elaltatták, majd a szívből kinyerték a perifériás vért. A szérum szeparálása után megmérték
az IL-6 és TNF szinteket. Az IL-6 aktivitását a B9 sejtvonallal, a TNF-aktivitást a
WEHI164-13 sejtvonal biovizsgálatával mérték.
Ahogyan az a 9. sz. ábrán látható, a 200 μg/egér LPS-adag bevitele után a túlélési ráta
jelentősen nőtt a napi 20 mg/kg, ill. 200 mg/kg Biobran MGN-3 készítménnyel kezelt
csoportokban, a kontrollcsoporthoz képest (20 mg/kg Biobran MGN-3 csoport kontra
kontrollcsoport, p = 0.0456; 200 mg/kg Biobran MGN-3 csoport kontra kontrollcsoport, p =
0.0232, a Mantel-Cox teszt segítségével). 100 μg/egér LPS-adag mellett a napi 20 mg/kg vagy
200 mg/kg Biobran MGN-3 adagolású csoportokban minden egér túlélte a bevitelt, míg a
kontrollcsoportban 10 egérből 3 elpusztult.
Hogy felfedjék, hogyan javítja a Biobran MGN-3 készítmény a túlélési rátát, megmérték az
IL-6 és TNF koncentrációját a vérben. A Biobran MGN-3-t szedő kísérleti csoportban a
kontrollcsoporthoz képest a vér IL-6 szintje az LPS bevitele után lényegesen alacsonyabb
volt (kontrollcsoport: 702.9 ± 24.7 ng/ml, Biobran MGN-3 csoport: 403.1 ± 59.6 ng/ml; p <
0.01); azonban 8 órával a bevitel után jelentősen nőtt (kontrollcsoport: 88.5 ± 50.0 ng/ml,
Biobran MGN-3 csoport: 441.0 ± 115.0 ng/ml;; p < 0.05). Eközben 4 órával az LPS bevitele
után a vér TNF-szintje jelentősen nőtt a Biobran MGN-3 csoportban a kontrollcsoport
egyedeihez képest (kontrollcsoport: 492 ± 187, Biobran MGN-3 csoport: 1816 ± 307 pg/ml; p <
0.01).
Az LPS által indukált halálos szepszis modellben többszörös szervi elégtelenséget
feltételeztek a szervezet retikuloendoteliális rendszeréből felszabaduló nagy mennyiségű
gyulladási folyamatokra ható citokinek (IL-1, 6, TNF-α) hatására, ami halálhoz vezet. Ebben
a tanulmányban a Biobran MGN-3 készítmény alkalmazása következtében a túlélési ráta jelentős
javulását tapasztalták. Ennek oka valószínűleg az volt, hogy a Biobran MGN-3 szedése gátolja
a makrofágokból eredő hisztotoxikus citokinek termelését vagy a Biobran MGN-3 blokkolja a
hisztotoxicitás útját a célsejtek szintjén.
Sudo N., Kubo C. (Kyushu Egyetem., JAPAN): Japán Klinikai és Kísérleti Orvostudományi
Szaklap, 78. évf., 1, 2001
(c) A Cisplatin gyógyszerrel kezelt egerek súlycsökkenésének Biobran MGN-3 általi mérséklése
A rákkezelésben a platina alapú gyógyszerek gyakran jelentős mellékhatásokkal rendelkeznek,
pl. rosszullét, hányás, valamint a vesetubulusok károsodása következtében fellépő nefropátia
és hipomagneziémia (Lajer & Dangaard 1999). Ezen felül, a halláskárosodás és perifériás
neuropátia mellett a leginkább káros mellékhatások között szerepel a mieloszupresszió is
(Prestayko et al. 1979), ami legyengült immunrendszerhez vezet. Ezért a cél a Cisplatin
mellékhatásainak bárminemű csökkentése. Ennek érdekében vizsgálták a Biobran MGN-3 hatását
az olyan egerek súlycsökkenésének mérséklése terén, amelyek a Cisplatin maximális
tolerálható adagját kapták.
A Cisplatin bevételét megelőző egy hétig a két csoportra osztott egerek Biobran MGN-3
készítményt kaptak, 10 mg/ml dózisban (száraz tömeg), vízben vagy 0,1 ml mennyiségű, PBS-ben
oldott Biobran MGN-3 intraperitoneális injekció formájában. A Biobran MGN-3 1 mg/egér
dózisát az ajánlott emberi dózis (50 mg/kg) alapján számították ki. Egyetlen adag Cisplatint
intraperitoneálisan vittek be 0,1 ml mennyiségben - 15 mg/kg gyógyszerkoncentráció PBS-ben,
amely hordozóanyagként 0,5% DMSO-t tartalmazott. A két csoportban lévő egerek vízben szájon
át vagy PBS-ben intraperitoneálisan kapták meg a készítményt, majd egy héttel később mindkét
csoport Cisplatint kapott.
A Cisplatin intraperitoneális befecskendezését követő napon mindkét, a Biobran MGN-3
készítményt kapott/nem kapott, csoport esetében is súlycsökkenés lépett fel. A legnagyobb
súlycsökkenés mindkét csoportnál a Cisplatin bejuttatását követő 5. napon jelentkezett, a
Biobran MGN-3 készítményt szájon át, ill. intraperitoneálisan megkapó csoport esetében is. A
legnagyobb súlycsökkenés azon egerek esetében jelentkezett, amelyek a Cisplatint a Biobran
MGN-3 bejuttatása nélkül kapták meg. Igaz, hogy a Biobran MGN-3 készítményt kapott egereknél
jelentkező súlycsökkenés a Biobran MGN-3 készítmény nélkül Cisplatinnal kezelt csoportok
esetén tapasztalt súlycsökkenés 20%-ának megfelelő volt, azonban nem pusztult el egy egér
sem, és egyik egérnél sem jelentkezett hasmenés vagy a végbél vérzése, ami a Cisplatin
gyakori mellékhatása. A felépülési fázisban azon egerek, amelyek megkapták a Biobran MGN-3
készítményt, korábban nyerték vissza a korábbi súlyukat.
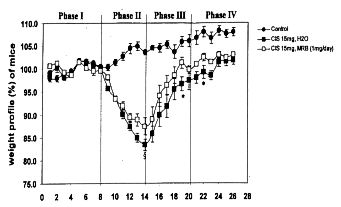 10. sz. ábra
10. sz. ábra
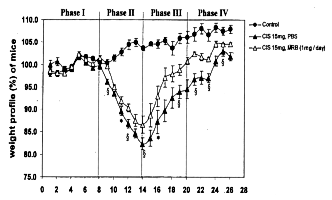 11. sz. ábra
11. sz. ábra
Endo Y., Kanbayashi H. (Mac Master Egyetem, CANADA): Pharmacology and Toxicology
[Gyógyszerészet és toxikológia], 2003
(d) A Biobran MGN-3 hatása a Cisplatin és Adriamycin által okozott toxicitásra patkányoknál
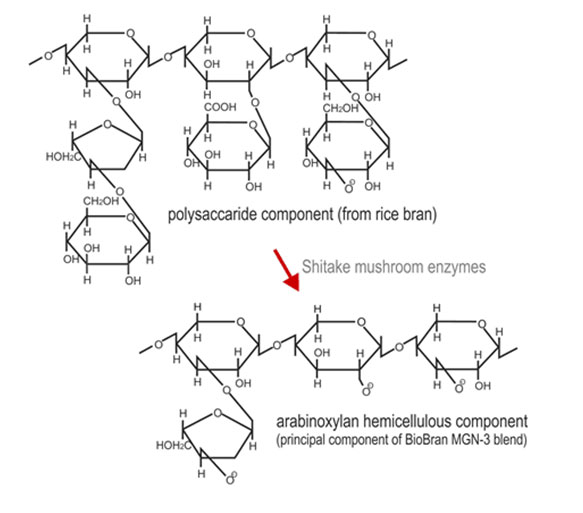
A Biobran MGN-3 rizskorpából, a rizskorpa vízben oldódó hemicellulóz frakciójának a Lentius
edodes micéliumkivonatából származó karbohidrázok általi részleges hidrolízisével készül
(USA szabvány sz.: 5560914]. A Biobran MGN-3 készítményről bebizonyosodott, hogy biológiai
válaszmódosító anyag, amely a károsodott immunrendszerű betegeknél növeli a természetes
gyilkos sejtek aktivitását [Int. J. Immunother. 14 (1) 1998].
Cél: Az egyetlen adagnyi Cisplatin (CIS) vagy Adriamycin (ADR) által
okozott súlyos patológiás változások és testtömeg-veszteség megelőzése napi 5 vagy 50mg/kg
Biobran MGN-3 szájon át történő bevitelével. Egy 13 napos akklimatizációs időszakot követően
hím Spraque-Dawley patkányokat választottak ki a vizsgálathoz testtömegük alapján, az alábbi
csoportokba (10 patkány / csoport) osztva őket (a dózis mg/ml egységben értendő):
-
Biobran 5 gm PO+Veh IP
-
Biobran 50 gm PO+Veh IP
-
Biobran kontroll PO+CIS 8mg IP
-
Biobran 5 gm PO+ CIS 8mg IP
-
Biobran 50 gm PO+ CIS 8mg IP
-
Biobran kontroll PO+ADR 10mg IP
-
Biobran 5 gm PO+ ADR 10mg IP
-
Biobran 50 gm PO+ ADR 10mg IP
A patkányok orálisan (PO) kapták a Biobran MGN-3 készítményt (desztillált víz képezte
szuszpenzió formájában) vagy a hordozóanyagot (veh), naponta, 11 napon át. A kemoterápiás
gyógyszereket, illetve a hordozóanyagot minden patkányba a 3. napon egyetlen IP injekció
formájában juttatták be. A patkányokat klinikailag 11 napon át figyelték. Minden második
napon feljegyezték testtömegüket. A 11. napon minden állatot elaltattak CO_2 segítségével és
felboncoltak. A főbb szervek vizuális jellemzőit kiértékelték, majd feljegyezték az
emésztőrendszer károsodásait.
Eredmények: A 3. csoportban 5 patkány, az 5. csoportban 3 patkány, a 4.
csoportban 1 patkány pusztult el a 7. és 11. nap között. A Biobran MGN-3 készítményből 5
vagy 50 mg/kg dózisban PO részesült patkányok statisztikailag szignifikáns
testtömeg-növekedést értek el (+72%). A kizárólag CIS, ill. ADR gyógyszert kapó patkányok
kisebb testtömeg növekedést mutattak (-1,5%, CIS; +30%, ADR). A Biobran MGN-3 készítményt 5
vagy 50 mg adagban plusz CIS vagy ADR gyógyszert kapó patkányok esetén jelentősen nagyobb
volt a testtömeg-növekmény, mint a kizárólag a kemoterápiás gyógyszert kapó csoportban (5 mg
Biobran MGN-3 esetén a CIS gyógyszerrel kezelt patkányoknál +11%, az ADR gyógyszerrel kezelt
patkányoknál +46%). 50 mg Biobran MGN-3 esetén a CIS gyógyszerrel kezelt patkányoknál +44%,
az ADR gyógyszerrel kezelt patkányoknál +43%. A Biobran MGN-3 készítményt kapott túlélő
patkányok egészségesebbnek tűntek, testtömegük nőtt, a bélrendszer súlyos patológiás
elváltozásai kisebb mértékben jelentkeztek, mint a CIS vagy ADR gyógyszerrel kezelt, Biobran
MGN-3 készítményt nem kapott csoportnál.
4. sz. táblázat: A Biobran hatása cisplatin és a doxorubicin által
előidézett testtömegcsökkenésre
| Kezelés (mind intraperitoneális) |
0. nap |
3. nap |
5. nap |
7. nap |
9. nap |
11. nap |
5mg/kg PO+hordozóanyag
50mg/kg PO+hordozóanyag
Kontroll PO+Cp8mg/kg
?50 mg/kg PO + Dx 10 mg/kg
?50 mg/kg PO + Dx 10 mg/kg
Kontroll PO+Dx 10 mg/kg
5 mg/kg PO+Dx 10mg/kg
50 mg/kg PO + Dx 10 mg/kg
|
100
100
103
99
101
103
101
101
|
100
98
101
99
99
100
100
101
|
100
100
82
85
92
88
92
92
|
100
97
69
76
90
82
89
87
|
100
97
55
68
85
77
86
85
|
100
97
57
65
84
76
85
83 |
PO: orális bevitel, Dx-Doxorubicin, Cp-Cisplatin
Jacoby H. I. (USA): Journal of Nuturaceuticals, Function & Medical Foods [A nutraceutikumok,
funkcionális és orvosi élelmiszerek szaklapja], 3. évf. (4) 2001.
(e) A Biobran MGN-3 készítmény hatása a radioterápia által előidézett toxicitásra egerek
esetén
Ez a tanulmány a Biobran MGN-3 készítménynek a teljes test besugárzása által okozott
csontvelőpusztulásban megnyilvánuló sugárzásérzékenységre gyakorolt módosító hatását
vizsgálta. A lehetséges klinikai alkalmazás reményében a tanulmány szerzői minden hatást
kvantitatív módon vizsgáltak, a sugárkezelés dózisainak széles skáláján (4,5 Gy - 8,5 Gy).
A kísérletek alanyai 4, ill. 5-hetes SPF hím BALB/c egerek voltak (F2). A Biobran MGN-3
készítményt kapó csoportokban az F2 egerek táplálékához 50 mg/kg dózisban Biobran MGN-3
készítményt adtak. Minden csoportban 10-50 egér volt. A ketrecbezárás után 2 nappal a
táplálékot az F2 csoportban a Biobran MGN-3 készítménnyel dúsított táplálékra változtatták.
A 4- és 5-hetes egereket a Biobran MGN-3 készítménnyel való táplálást követően 15 és 8 napig
sugárkezelésnek vetették alá. Hetente 3 alkalommal mérték testtömegüket, és naponta
ellenőrizték az elpusztult egyedek számát. Egyes esetekben a kísérletben alkalmazott egerek
a besugárzást megelőző két hétig kapták a készítményt, egyéb esetekben a besugárzást
követően kezdődött csak el a Biobran MGN-3 készítmény bevitele.
Az F2 csoportban ugyan az egerek pusztulása a csontvelőpusztulás következtében a besugárzást
követő 7. napon következett be, a Biobran MGN-3 készítményt kapó egerek csoportjához tartozó
egerek később pusztultak el. Az F2 csoportban az LD50 értéke mintegy 5,15 Gy volt, míg a
dózisredukciós faktor (DRF) hozzávetőlegesen 1,14 volt. A testtömeget tekintve a Biobran
MGN-3 készítményt kapó csoportok egyedeinek testtömege nagyobb volt. A Biobran MGN-3
készítmény alkalmazásának korábbi kezdetéhez köthető hatás tekintetében elmondható, hogy a
Biobran MGN-3 készítmény alkalmazása még a besugárzást megelőzően ajánlott.
Az egerek sugárdózisát a fenti dózisok 1,21-szeres értékeként határozták meg testük
középpontjára vonatkoztatva, így a kontroll-csoport LD50 értéke 6,23 Gy értéknek felelt meg.
A Biobran radioprotektív hatása ugyan DRF = 1,14 volt, ami nem nagy érték, azonban a
tanulmányban semmilyen mellékhatás jelenléte nem igazolódott.
Nakatugawa S. (Nagoya Egyetem, JAPAN): A Nagoya Egyetem jelentése, 2003
(f) A Biobran MGN-3 hatása a patkányok májának kísérleti diszfunkciójára
A tanulmány a Biobran MGN-3 készítménynek a máj diszfunkciójára gyakorolt hatását vizsgálta.
A kutatók azt vizsgálták, hogy a Biobran MGN-3 készítmény milyen hatást fejt ki a patkányok
májának kísérleti, a galaktózamin (GaIN) és acetaminofen (AAP) által kiváltott
diszfunkciójának alakulására. A máj kísérleti diszfunkciójának előidézése érdekében az 1-3.
kísérletben GaIN, a 4-5. kísérletben AAP került alkalmazásra.
Az 1. sz. kísérletben különféle koncentrációjú Biobran MGN-3 készítményt adtak be
intraperitoneálisan patkányoknak, majd 1 óra elteltével 800 mg/kg GaIN bevitelét végezték
el.
A 2. sz. kísérlet során a Biobran MGN-3 készítményt orálisan, valamint a nagy és alacsony
molekulatömegű frakciókra bontott Biobran MGN-3 készítményt intraperitoneálisan juttatták
be. 1 óra elteltével 800 mg/kg GaIN bevitelét végezték el.
A 3. sz. kísérlet során a Biobran MGN-3 készítményt melegítés, hidrolízis és ioncserélő
gyanta segítségével való feldolgozás után intraperitoneálisan juttatták be. 1 óra elteltével
800 mg/kg GaIN bevitelét végezték el.
Az 4. sz. kísérletben Biobran MGN-3 készítményt adtak be intraperitoneálisan vagy orálisan,
majd 1 óra elteltével 700 mg/kg AAP bevitelét végezték el.
Az 5. sz. kísérlet során a Biobran MGN-3 készítményt melegítés, hidrolízis és ioncserélő
gyanta segítségével való feldolgozás után intraperitoneálisan juttatták be; 1 óra elteltével
500 mg/kg AAP bevitelét végezték el.
A patkányokat a GaIN vagy AAP bevétele utáni 24 órával minden kísérletben felboncolták, majd
meghatározták a szérum transzamináz (GOT, GPT) szintjét.
Eredmények
1. sz. kísérlet: Minden csoportban, amelyben a Biobran MGN-3 készítmény
bevitele megtörtént, a kontroll-csoport eredményéhez képest lényegesen kisebb volt a máj
GaIN által előidézett működési zavarának köszönhető GOT- és GPT-aktivitásnövekmény. A máj
GaIN által előidézett működési zavarának szupressziója 20 mg/kg dózisú Biobran MGN-3
készítmény alkalmazása mellett érte el a tetőfokát, a Biobran MGN-3 készítmény nagyobb
koncentrációja esetén nem jelentkezett a GaIN által előidézett májműködési zavar nagyobb
mértékű szupressziója.
2. sz. kísérlet: Minden csoportban, amelyben a Biobran MGN-3 készítmény
vagy a Biobran MGN-3 nagy/kis molekulatömegű frakcióinak bevitele megtörtént, a
kontrollcsoport eredményéhez képest lényegesen kisebb volt a máj GaIN által előidézett
működési zavarának köszönhető GPT-aktivitásnövekmény. A szupresszió mértéke hasonló volt a
Biobran MGN-3 esetén tapasztalthoz.
3. sz. kísérlet: Minden csoportban, amelyben a hidrolizált Biobran MGN-3
készítmény bevitele megtörtént, a kontrollcsoport eredményéhez képest lényegesen kisebb volt
a máj GaIN által előidézett működési zavarának köszönhető GOT-aktivitásnövekmény.
4. sz. kísérlet: Minden csoportban, amelyben a Biobran MGN-3 készítmény
intraperitoneális vagy orális bevitele megtörtént, a kontrollcsoport eredményéhez képest
lényegesen kisebb volt a máj AAP által előidézett működési zavarának köszönhető
GOT-aktivitásnövekmény.
5. sz. kísérlet: A 3. sz. kísérlet eredményeivel összhangban vizsgálták a
hidrolizált Biobran MGN-3 hatását az AAP alkalmazása esetén. Minden csoportban, amelyben a
hidrolizált Biobran MGN-3 készítmény bevitele megtörtént, a kontrollcsoport eredményéhez
képest lényegesen kisebb volt a GOT-aktivitásnövekmény.
Tehát beigazolódott a Biobran MGN-3 szupresszív hatása a GaIN, ill. AAP által előidézett
májműködési zavar esetén. Az aktív összetevőt a jelek szerint a HCl nem hidrolizálja.
Yamada T. (Chiba Egyetem, JAPAN): A Japán Táplálkozásirost-kutató Szövetség 6. éves
összejövetelének összefoglalója, 2002
(g) A Biobran MGN-3 orális alkalmazása orvosolja az idősek megfázását
A nagy kockázatot jelentő csoportok esetén - pl. az idősek vagy a gyerekek - fontosak a
fertőzések ellen tett megelőző intézkedések, például az infuenza elleni oltás és a
másodlagos baktériumfertőzések következetes megelőzése. A valószínűleg a megfázás
szövődményeként megjelenő, közösségi-eredetű tüdőgyulladások vizsgálata során azt
tapasztalták, hogy a másodlagos baktériumfertőzések kockázata magasabb a 75 év feletti
személyek esetében. A szövődményes tüdőgyulladás kockázata azon neurológiai zavarokkal
küszködő idős páciensek esetén is magas, akiknél magas az aspiráció kockázata. Ezért
vizsgálták a Biobran MGN-3 készítmény klinikai hatékonyságát a megfázás kifejlődése
szempontjából azon időseknél, akik immunrendszerének erőssége különféle tényezők hatására
csökkent.
2002 januárja és márciusa között a Kobe, Hoygo székhelyű "Atreyu Uozaki" idősgondozó
intézmény idősebb ügyfelei közül választották ki azokat, akik nem voltak súlyosan betegek,
és akik beleegyeztek a tanulmányban való részvételbe. A vizsgálat során a Biobran MGN-3
készítmény frakcióját (HRB) alkalmazták vizsgálati táplálékként , valamint a
kontrollcsoportban a főleg a vízben oldódott komponenst tartalmazó rizskorpát alkalmazták.
A megfázás tünetei (láz, fejfájás, fáradtság, hideglelés, köhögés, köpet, orrfolyás,
orrdugulás, torokfájás, mellkasi fájdalom) esetén megszámolták a megfázás egyes tüneteinek
napjait. Meghatározták minden tünet szintjét és a szintnek megfelelő pontszámot (tünetmentes
– 0, enyhe – 1, közepes – 2, súlyos – 3), majd kiszámolták a megfázás tüneteinek pontszámát
az egyes alanyoknál jelentkező összesített pontszám és az vizsgált táplálék bevitele
napjainak hányadosaként.
Eredmények: Az egyes tünetek közül a köhögés, fáradtság, láz és torokfájás
megjelenésének frekvenciája mindkét táplálék fogyasztásának megkezdése idején magas volt. A
HRB csoportban a tüneti napok száma alacsonyabb volt, mint az RB csoportban. A megfázás
tüneteinek pontszámát megvizsgálva az RB csoport összesítésben magas pontszámot tért el. Míg
az "orrtünetek" pontszáma az RB csoportban kisebb volt, a köhögés, a fáradtság és láz
esetében a pontszám magasabb volt. Ennek eredményeképpen úgy találták, hogy a megfázás
tünetei a HRB csoportban kisebb mértékben jelentkeztek.
A tanulmány igazolta, hogy idősek megfázása esetén, szájon át történő alkalmazásakor a HRB
lerövidíti a tünetek megjelenésének idejét, a tünetek súlyossága nem nő, és a tüneti kezelés
szükségessége csökken a kivonat immunrendszer-stimuláló hatásának következtében.
Tazawa K. (Toyama Orvosi és Gyógyszerészeti Egyetem, Japán): Joural of Traditional Medicines
[Hagyományos gyógyászati szaklap] 20 (3), 2003
3.7. Allergiaellenes hatás
(a) A Biobran MGN-3 készítménynek az asztma megelőzésére és tüneteinek csökkentésére
kifejtett hatásának vizsgálata asztmás modellegerek esetén
A Biobran MGN-3 készítménynek az asztma megelőzésére és tüneteinek csökkentésére kifejtett
hatását modellegerek TDI által előidézett asztmáján vizsgálták.
Először 2 g/l Biobran MGN-3 készítményt oldottak fel ivóvízben és naponta adagolták a fenti
modellegereknek (BALB/c, nőstény), amelyeket 4 csoportra (A-D) osztottak, a következők
szerint:
A csoport: Egy hónapig tartó előzetes Biobran MGN-3 bevitel, bevitel a TDI
érzékenység-időszak és a vizsgálati időszak során.
B csoport: Egy hónapig tartó előzetes Biobran MGN-3 bevitel, bevitel a TDI
érzékenység-időszak végéig.
C csoport: Biobran MGN-3 bevitel csak a TDI érzékenység-időszak során.
D csoport: kontrollcsoport.
A B csoport a preventív hatás vizsgálatát szolgálta, míg a C csoport a tünetredukciós hatás
vizsgálatát. A Biobran MGN-3 hatását a következőkkel mérték: a vér hisztaminkoncentrációja,
a BALF-ben levő eozinofilek száma, a TDI fülcimpa-alkalmazási vizsgálat, a vér IgG1, igG2a,
IgE típusú specifikus antitestek értékei.
A vér maximális hisztaminkoncentrációja a TDI alkalmazását követő 7. percben jelentkezett, A
csoport: 2.5±0.53, B csoport: 4.2±0.75, C csoport: 4.3±7.8, D csoport: 6.4±0.87 (ng/ml), míg
a Biobran MGN-3 beviteli csoportok lényegesen alacsonyabb értékeket mutattak a
kontrollcsoporthoz képest. A különféle TDI-koncentrációkkal (0,01-10%) végzett
szenzitizáció-vizsgálatok során a Biobran MGN-3 beviteli csoportok a kontrollcsoporthoz
képest 10-100× kisebb szenzitivitást mutattak.. Ezen felül a Biobran MGN-3 készítményt
alkalmazó csoportok jelentősen kisebb számú eozinofilt mutattak a BALF-ben és alacsonyabb
TDI-alkalmazásvizsgálati eredményeket. Ezzel szemben nem volt szignifikáns különbség a vér
antitestszintjei között.
Összegzésként a Biobran MGN-3 bevitele evidens megelőző és tünetcsökkentő hatást mutatott a
modellegerek TDI által okozott asztmája esetén. Ennek alapján a Biobran MGN-3 nem
befolyásolja az IgG1 vagy IgE típusú antitesteket, amelyek termelését a Th2 idézi elő, és a
Biobran MGN-3 a hízósejtek szupresszív tényezőjeként jelenik meg.
Kobayashi H., Endo Y. (Mc Master Egyetem, Kanada): A Japán Allergológiai Társaság 52. éves
összejövetelének összefoglalója, 2002
(b) A Biobran MGN-3 inhibíciós hatása az NC egerek atópiás dermatitiszének előrehaladtára
Vizsgálták A Biobran MGN-3 készítmény immunrendszer-szabályozó hatását olyan NC egerek
esetében, amelyek az OVA-szenzitizáció hatására természetesen kialakuló megnövekedett
IgE-szintet és atópiás dermatitiszre hasonlító bőrléziókat produkáltak. A Biobran MGN-3
készítményt orálisan 5 NC egérnek adták be, majd összehasonlították őket a Biobran MGN-3
készítményt nem kapó kontrollcsoporttal. Az egereket OVA segítségével szenzitizálták.
Kéthetente vettek vérmintát, a szenzitizálás előtt és után. Mérték a szérum teljes
IgE-szintjét, valamint az OVA-specifikus IgE-szintjét specifikus ELISA vizsgálattal - a
kontrollcsoporttal összehasonlítva a Biobran MGN-3 készítménnyel kezelt NC egereknél
lényegesen alacsonyabb értékek jelentek meg. Ezen felül az atópiás dermatitisz-szerű
bőrléziók nem alakultak ki a Biobran MGN-3 készítménnyel kezelt öt NC egér közül 5-nél, míg
a Biobran MGN-3 készítményt nem kapó NC egerek mindegyikénél bőrléziók alakultak ki. A
szerzők következtetése értelmében a Biobran MGN-3 inhibíciós hatással van az NC egerek
atópiás dermatitiszének előrehaladtára.
Nonoyama S. (Tokyo Orvostudományi és Fogászati Egyetem, Japán): A Nemzetközi Immunológiai
Kongresszus 11. éves találkozójának összefoglalója, 2001
© Copyright 2003 Hiroaki Maeda / Daiwa Pharmaceutical
(köszönjük a cikknek a biobran.org honlapon való megjelentetésére vonatkozó engedélyt).
 The main researcher on
A Biobran vezető kutatója Dr. Mamdooh Ghoneum, aki az amerikai Drew Orvosi és
Tudományegyetem Immunológiai Tanszékének professzora. Dr. Ghoneum, aki jelenleg a rák
immunterápiájának nemzetközileg elismert szakértője a Tokiói Egyetemen végezte
posztgraduális tanulmányait radioimmunológiából, majd az UCLA egyetemen végzett
posztdoktori munkát immunológia tárgyában. Az utóbbi húsz év során különféle anyagokat
kutatott, amelyek képesek támogatni az immunrendszert. Ő mondta, hogy "a Biobran MGN-3 a
legerősebb immunrendszeri komplexum, amelyet valaha vizsgáltam." Annyira érdekesnek
találta az eredményeket, hogy immár minden kutatómunkáját az ezen összetevő segítségével
végzett kezelések kutatásának szenteli.
The main researcher on
A Biobran vezető kutatója Dr. Mamdooh Ghoneum, aki az amerikai Drew Orvosi és
Tudományegyetem Immunológiai Tanszékének professzora. Dr. Ghoneum, aki jelenleg a rák
immunterápiájának nemzetközileg elismert szakértője a Tokiói Egyetemen végezte
posztgraduális tanulmányait radioimmunológiából, majd az UCLA egyetemen végzett
posztdoktori munkát immunológia tárgyában. Az utóbbi húsz év során különféle anyagokat
kutatott, amelyek képesek támogatni az immunrendszert. Ő mondta, hogy "a Biobran MGN-3 a
legerősebb immunrendszeri komplexum, amelyet valaha vizsgáltam." Annyira érdekesnek
találta az eredményeket, hogy immár minden kutatómunkáját az ezen összetevő segítségével
végzett kezelések kutatásának szenteli.



 5. sz. ábra: A természetes gyilkos sejtek (NK-sejtek) és a K-562 célsejtek
közötti konjugátum-képződés százalékaránya.
5. sz. ábra: A természetes gyilkos sejtek (NK-sejtek) és a K-562 célsejtek
közötti konjugátum-képződés százalékaránya.
 6. sz. ábra: A természetes gyilkos effektorsejtek (NK-sejtek) - tumor
célsejtek konjugátumának képződése.
6. sz. ábra: A természetes gyilkos effektorsejtek (NK-sejtek) - tumor
célsejtek konjugátumának képződése.
 7. sz. ábra: Egérből származó peritoneális makrofágok (C3H/He egerek).
7. sz. ábra: Egérből származó peritoneális makrofágok (C3H/He egerek).

 10. sz. ábra
10. sz. ábra
 11. sz. ábra
11. sz. ábra