3. AZIONE FISIOLOGICA DEL DERIVATO DI ARABINOSSILANO DI CRUSCA DI RISO (Biobran)
3.1 ImunoREGOLAZIONE
(a) Aumento dell’attività delle cellule NK umane con l’ausilio di arabinossilano modificato
di crusca di riso (Biobran MGN-3)
1. Test in vitro
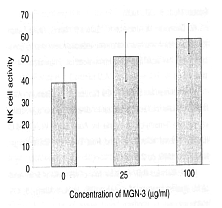
Un certo numero di cellule NK del ratto è stato incubato insieme a cellule tumorali
bersaglio K-562 in presenza di Biobran MGN-3; successivamente, mediante test di separazione
51Cr, è stata misurata la quantità di cellule K-562 decomposte. La concentrazione aumentata
di cellule decomposte è stata valutata in relazione alla concentrazione di Biobran MGN-3 (25
µg/ml o 100 µg/ml). Il risultato ha confermato che l’aumento dell’attività delle cellule NK
è stato causato dall’azione del preparato Biobran MGN-3.
2. Test in vivo (sui ratti)
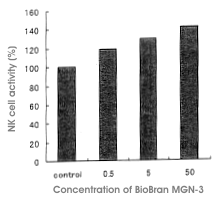
Biobran MGN-3 è stato somministrato oralmente ad alcuni ratti Sprague-Dawley e dopo due
settimane è stata misurata l’attività delle cellule NK. I ratti sono stati suddivisi in tre
gruppi da 5 individui, con somministrazione di dosi con concentrazioni da 0,5 mg, 5 mg, e 50
mg/kg/giorno. A seconda della concentrazione del dosaggio di Biobran MGN-3 somministrato, è
stata misurata anche l’attività aumentata delle cellule NK. Nei gruppi con dosi da 0,5 mg, 5
mg e 5 mg l’attività ha subito incrementi rispettivamente del 119%, 130% o 142% (rispetto al
gruppo controllo). Nel gruppo con dose da 50 mg, l’attività è impennata al 132% rispetto al
gruppo controllo già dopo tre giorni dall’inizio della somministrazione del preparato.
L’incremento dell’attività delle cellule NK, generato dal preparato Biobran MGN-3, può
essere attribuito all’intensificazione della forza distruttrice delle cellule NK, ma allo
stesso tempo è dipeso anche dal numero complessivo di cellule NK. Sono state anche osservate
le differenze negli effetti tra soggetti maschi e femmine ed è stata riscontrata
un’efficacia del prodotto più intensa nelle femmine (Fig. 3).
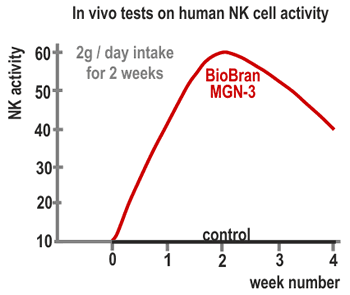
3. Azione sull’uomo
Nell’ambito dei test dell’azione del preparato Biobran MGN-3 sugli esseri umani, sono stati
presi in considerazione 24 individui sani (15 donne e 9 uomini con età media 34 anni).
Questi individui hanno assunto il preparato per 60 giorni ed è stata monitorata l’attività
delle loro cellule NK. I partecipanti sono stati suddivisi in 3 gruppi da 8 persone, con
dosi giornaliere pari a 15 mg/kg, 30 mg/kg e 45 mg/kg/peso corporeo. A ciascun partecipante
è stato prelevato un campione di sangue (20 ml) prima dell’inizio dell’assunzione del
preparato, dopo una settimana di assunzione, dopo un mese, dopo due mesi (dall’inizio
dell’assunzione) e a un mese dal termine dell’assunzione; ed è stata misurata l’attività
delle cellule NK. Nei gruppi con dosi da 30 mg e 45 mg, dopo una settimana di assunzione del
preparato, l’attività delle cellule NK è aumentata del doppio, e dopo due mesi del triplo.
Nel gruppo con dosi da 15 mg l’attività è cresciuta rapidamente dopo un mese dall’inizio
dell’assunzione; e dopo due mesi aveva già raggiunto quasi lo stesso livello dei gruppi da
30 mg e 45 mg. Un mese dopo la cessazione dell’assunzione, l’attività delle cellule NK è
tornata al livello registrato prima del test (Fig. 4). I risultati suggeriscono dunque che
già delle dosi da 15 – 45 mg/kg di Biobran MGN-3 al giorno hanno un impatto reale
sull’attività delle cellule NK umane.
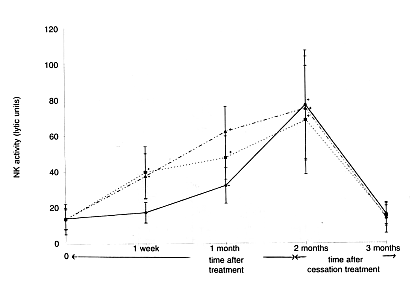
<Figure 4: Dipendenza dell’attività delle cellule NK rispetto all’assunzione
del preparato Biobran MGN-3 (a livello temporale e di dosaggio) contro le cellule tumorali
K562…_.._.._.._ = 45mg/kg/giorno; …………=30mg/kg/giorno; _______=15mg/kg/giorno
4. Meccanismo di azione del preparato Biobran MGN-3 sulle cellule NK
Entrambi i test, in vitro e in vivo, hanno confermato aumenti della quantità di granuli
citotossici nelle cellule NK stimolate da Biobran MGN-3. È stata anche studiata la capacità
di queste cellule di legarsi con le cellule bersaglio. Nel test, le cellule NK di un
individuo sottoposto a dosi da 45 mg/kg di Biobran MGN-3 al giorno per 30 giorni sono state
incubate insieme a cellule bersaglio K-562. Successivamente è stata valutata la loro
capacità di legarsi con le cellule bersaglio. Dopo un’incubazione comune di un’ora alla
temperatura di 4°C è stato misurato un livello pari a 200 cellule NK ed è stato valutato il
tasso di formazione di legami con le cellule K-562. Nell’individuo che assumeva Biobran
MGN-3 il tasso di formazione di legami delle cellule NK con le cellule bersaglio (K-562) è
risultato molto più alto che prima dell’inizio dell’assunzione (38,5% contro il 9,4%). La
Fig. 6 riporta una fotografia di questi legami.
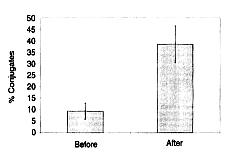 Fig 5: Percentuale di formazione di legami tra natural killer (cellule
NK) e cellule bersaglio K562. Legenda:% di legami > Prima dell’assunzione > Dopo
l’assunzione
Fig 5: Percentuale di formazione di legami tra natural killer (cellule
NK) e cellule bersaglio K562. Legenda:% di legami > Prima dell’assunzione > Dopo
l’assunzione
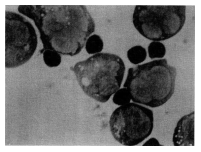 Fig 6: Formazioni letali di cellule NK e cellule tumorali bersaglio.
Fig 6: Formazioni letali di cellule NK e cellule tumorali bersaglio.
Ghoneum M. (Università Ch. R. Drew, USA):INT. IMMUNO THERAPY XIV (2) p.89-99, 1998
(b) Effetto in vitro del preparato Biobran MGN-3 sulle attività di cellule del gruppo dei
macrofagi
È stato analizzato l’effetto del Biobran MGN-3 sulle cellule del gruppo dei macrofagi, per
quanto riguarda l’induzione della produzione di mediatori farmacologici (nello specificto
mediatori TNF-A, IL-6 e NO). I macrofagi sono stati incubati insieme al preparato Biobran
MGN-3 a diverse concentrazioni (da 1 a 100 µg/ml); successivamente sono stati testati i
supernatanti in riferimento alla presenza dei già menzionati mediatori. Il TNF-a è stato
analizzato in base alla citotossicità verso L929, l’IL-6 in base alla citosi B13.19 e il NO
colorimetricamente in base alla reazione con reattivo di Griess. Come controllo positivo è
stato impiegato LPS.
- Con applicazione di linea cellulare murina di macrofagi RAW264.7, Biobran MGN-3 ha
mostrato un effetto assai intenso su tutti e tre i suddetti mediatori già a
concentrazioni superiori a 10 µg/ml, analogamente a LPS.
- Impiego di macrofagi peritoneali murini (C3H/He). La Fig. 7 illustra l’effetto del
preparato Biobran MGN-3 sulla secrezione dei macrofagi dalla cavità peritoneale nel topo
normale. Biobran MGN-3 ha mostrato anche qui un effetto assai intenso a concentrazioni
superiori a 10 µg/ml.
- Linea cellulare di macrofagi umani U937. MGN-3 ha indotto un’attività intensa, come
suggeriscono i livelli misurati delle citochine prodotte (TNF-A e IL-6), ovvero
l’equivalente di LPS a livello 100 µg/ml.
I risultati mostrano che Biobran MGN-3 ha un forte potenziale di attivazione dei macrofagi
normali murini e umani. Dagli studi emerge che l’attività si manifesta a concentrazioni
superiori a 10 µg/ml.
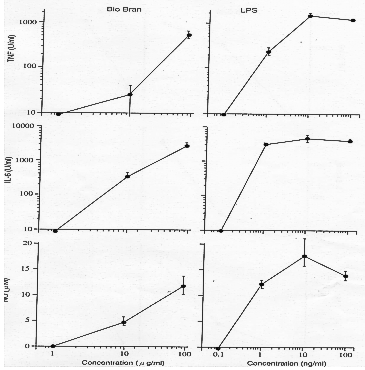 Figure 7: Matsuura M. (Scuola di Medicina di Jichi, GIAPPONE): Rapporto
della Scuola di Medicina di Jichi
Figure 7: Matsuura M. (Scuola di Medicina di Jichi, GIAPPONE): Rapporto
della Scuola di Medicina di Jichi
(c) Immunostimolazione e prevenzione del cancro
Numerosi studi hanno dimostrato un rischio aumentato di cancro nelle persone esposte a
diversi agenti chimici sul luogo di lavoro. L’obiettivo di uno di questi studi è stata
l’analisi della modifica dell’immunità in relazione all’influenza degli agenti chimici
tossici, nonché la possibilità dell’organismo di reagire meglio alla tossicità chimica con
l’ausilio del preparato Biobran MGN-3.
Allo studio hanno partecipato undici persone, normalmente esposte ad agenti chimici sul
luogo di lavoro. I partecipanti soffrivano di una disfunzione ormonale che si manifestava
con bassi livelli di attività di cellule NK (10,2±4,2 LU (unità litiche [ndt]) e scarsa
risposta blastogena dei linfociti del sangue ai mitogeni delle cellule T (PHA,
39060±12517cpm e COMA, 36224±11922cpm) e ai mitogeni delle cellule B (PWM, 16550±6330cpm)
rispetto alle reazioni riscontrate nel gruppo controllo. Ai partecipanti è sono stati
somministrati 15 mg/kg di Biobran MGN-3 per quattro mesi. La terapia col preparato ha
aumentato l’attività delle cellule NK di 4 volte dopo 2 mesi e di ben 7 volte dopo 4 mesi.
Inoltre, il funzionamento delle cellule T e B buniek è salito rispettivamente al 130% e al
150% dei valori originari.
Ghoneum M. (Università Ch. R. Drew, USA): Sintesi estrapolata dalla raccolta degli interventi
alla conferenza tenutasi in occasione del 7° congresso internazionale sulle tecnologie
biomediche contro l’invecchiamento, 1999
(d) Stimolo della produzione di TNF-α e IF-γ nei linfociti del sangue periferico umano
mediata da arabinossilano modificato di crusca di riso contenuto nel preparato Biobran
MGN-3.
Oggetto di analisi è stato il meccanismo mediante il quale Biobran MGN-3 aumenta l’attività
citotossica delle cellule NK. È stata dunque testata l’azione del preparato Biobran MGN-3
sull’intensità di secrezione del fattore di necrosi tumorale α, (TNF-α) e dell’interferone γ
(IFN-γ), nonché l’azione – sempre del Biobran MGN-3 – sull’espressione dei recettori
fondamentali sulla superficie della cellula.
I linfociti del sangue periferico sono stati incubati insieme al Biobran MGN-3 a
concentrazioni di 0,1 e 1 mg/ml e le soluzioni sono state sottoposte a test ELISA. I
risultati hanno dimostrato che il Biobran MGN-3 è un potente induttore di TNF-α, con effetti
che dipendevano dalle dosi. Concentrazioni di Biobran MGN-3 a livello di 0,1 e 1 mg/ml hanno
incrementato la produzione di TNF-α rispettivamente di 22,8 e 47,1 volte. Biobran MGN-3 ha
anche aumentato la produzione di IFN-γ, benche in misura minore rispetto al TNF-α. Per
quanto riguarda i recettori superficiali cellulari chiave, Biobran MGN-3 ha aumentato
l’espressione dell’antigene di attivazione CD69 dopo 16 ore di incubazione. Inoltre, dopo
l’incubazione con il preparato Biobran MGN-3 è stata osservata una regolazione positiva del
recettore dell’interleuchina-2, CD25 e molecola di adesione intercellulare ICAM-1 (CD54).
Anche l’incubazione di cellule NK altamente purificate con MGN-3 ha avuto come risultato
livelli aumentati di secrezione di TNF-α e IFN-γ in associazione ad un miglioramento della
funzionalità citotossica delle cellule NK. Inoltre, l’aggiunta di Biobran MGN-3 alle cellule
NK attivate dall’interleuchina-2 ha avuto come conseguenza l’induzione sinergica della
secrezione di TNF-α e IFN-γ.
Ghoneum M. (Università Ch. R. Drew, USA), Jewett A. (UCLA, USA): Cancer Detection and
Prevention (Rilevamento e prevenzione del cancro) Fasc. 24/Num. 4, 2000
(e) Effetto dell’arabinossilano modificato di crusca di riso sull’attività delle cellule NK
dei linfociti umani del sangue periferico.
Sono stati analizzati gli effetti del Biobran MGN-3 e delle sue frazioni molecolari
sull’attività delle cellule NK. Ai linfociti umani del sangue periferico sono state aggiunte
frazioni con alto peso molecolare (10 – 50 kDa), ottenute da filtrazione del gel con
utilizzo di Sephadex G-25 e G-75. Dopo un’incubazione di 3 giorni è stata stabilita
l’attività delle cellule NK. Come cellule target sono state utilizzate delle cellule
contrassegnate in modo fluorescente della linea K-562 e l’attività delle cellule NK è stata
determinata mediante metodo Tere Scan. Un esperimento analogo è stato realizzato in presenza
di IL-2.
Le prove non hanno rivelato differenze radicali nell’attivazione delle cellule NK né col
preparato Biobran MGN-3 con le sue frazioni con peso molecolare più alto. Quando però è
stata aggiunta IL-2, nelle soluzioni dove c’era anche Biobran MGN-3 o sue frazioni, è stata
osservata un’attività aumentata delle cellule NK rispetto alla soluzione dove era presente
la sola IL-2. Vale a dire che Biobran MGN-3 attiva le cellule NK in presenza di IL-2 e che
questa attività è presente anche con le sue frazioni di peso molecolare più alto.
Ueda Y., Shimomura C. (Università di Chiba, GIAPPONE): Rapporto dell’incontro annuale della
Società Giapponese per la Bioscienza, Biotecnologia e Agrochimica 2002
3.2. Effetti antivirali
Effetto antivirale del preparato Biobran MGN-3 anti-HIV in vitro
In primo luogo è stato valutato l’effetto antivirale del preparato Biobran MGN-3 contro la
produzione dell’antigene p24 dell’ HIV-1 in vitro. Alcune cellule mononucleate ottenute da
tre individui sani sono state incubate insieme al ceppo HIV-1 SF alla temperatura di 37°C
nel corso di un’ora in presenza del preparato Biobran MGN-3 a concentrazioni comprese tra 0
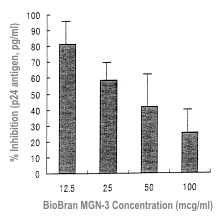
e 100 µg/ml. A seconda della concentrazione, il preparato MGN-3 ha inibito la creazione di
formazioni sinciziali, con il tasso massimo di tale inibizione pari al 75% ad una
concentrazione di 100/ml) (Tabella 1).
 |
|
Tabella 1
| Inibizione delle formazioni sinciziali mediante il preparato
Biobran
|
| Dose di Biobran (μg/ml) |
Formazioni sinciziali (SF) |
| Numero di SF |
% Inibizione |
0
12.5
25
50
100
|
42.0±8
25.8±7
21.5±5
15.8±4
10.5±3
|
00.0
38.5
50.0
62.5
75.0
|
|
| Fig. 8 |
|
Legenda:% di inibizione (antigene p24, pg/ml) > Concentrazione del
preparato BioBran MGN-3 (µg/ml)
|
Ghoneum M. (Università Ch. R. Drew, USA): Biochemical and Biophysical Research
Communications (Comunicazioni tra ricerca biochimica e biofisica) 243, (1998)
3.3. Effetto antitumorale
(a) Studio sull’azione delle componenti di arabinossilano modificato della crusca di riso
sull’inibizione della crescita di cellule tumorali di varie linee
Nell’ambito di questo studio è stato analizzato l’effetto inibitore dell’arabinossilano
modificato della crusca di riso, contenuto nel preparato Biobran MGN-3, sulla crescita di
cellule tumorali di varie linee, come HL60, K562 e HLE, e sulla potenziale induzione della
differenziazione in HL60 e K562. Biobran MGN-3 è stato aggiunto ad una coltura con linee
cellulari. Dopo 3 giorni di incubazione il tasso di sopravvivenza delle cellule (in tutte le
linee cellulari) è andato scemando proporzionalmente alla quantità aggiunta di preparato
Biobran MGN-3.
Dopo precipitazione con etanolo, il precipitato è stato mescolato con acqua distillata. Il
supernatante originatosi è stato poi frazionato mediante una colonna Sephadex G-25 in 3
frazioni (A, B, C); e queste sono state aggiunte alle colture con le linee cellulari. Sono
stati osservati i seguenti effetti inibitori della crescita: per la frazione C sulle linee
HL60 e K562; per le frazioni B e C, sulla linea HLE. Inoltre, la colorazione di Giemsa e con
esterasi aspecifica hanno mostrato una potenziale induzione della differenziazione in HL60
e K562. Questi risultati suggeriscono che Biobran MGN-3 contiene componenti che favoriscono
l’inibizione della crescita delle cellule tumorali e la potenziale induzione della
differenziazione delle linee HL60 e K562.
Masada M. (Università di Chiba., GIAPPONE): Rapporto dell’incontro annuale della Società
Giapponese per la Bioscienza, Biotecnologia e Agrochimica 2002
(b) Influenza del preparato Biobran MGN-3 sulla crescita delle cellule tumorali
Oggetto di studio è stato l’effetto diretto del preparato Biobran MGN-3 sulla crescita delle
cellule tumorali cutanee e sulla produzione di citochina. Rispetto al gruppo controllo di
cellule di carcinoma squamoso della linea cellulare SCC13 (coltivata in MEM, con crescita
del numero di cellule in continuo aumento), l’incubazione delle cellule di questa linea
[SCC13] insieme al preparato Biobran MGN-3 ha invece arrestato la crescita delle cellule
tumorali (è stato osservato il 30% in meno di cellule dopo 48 ore, e il 50% in meno dopo 72
ore di coltivazione, rispetto alla coltivazione di controllo già citata).
Le analisi con citometria di flusso hanno mostrato che, dopo 16 ore di incubazione delle
cellule SCC13 con il preparato Biobran MGN-3, si è verificato un incremento di cinque volte
dei livelli intracellulari di interleuchina 10 [IL-10], ma nessuna modifica manifesta quanto
a contenuto di interferone-γ [INF-γ]. I test ELISA del mezzo di coltivazione con le cellule
SCC13 hanno mostrato livelli di IL-10 di ben otto volte superiori e una crescita tripla
dell’IL-12. È stata poi osservata una modifica solo di carattere esiguo nella concentrazione
di INF-γ. Inoltre, è stata valutata l’influenza del preparato Biobran MGN-3 anche su
ulteriori linee cellulari (come cellule mammarie normali e tumorali e cellule tumorali della
prostata).
I dati rilevati suggeriscono che Biobran MGN-3 non solo migliora l’immunità dell’organismo
ospitante, ma ha anche un’influenza diretta sulla crescita delle cellule tumorali e sulla
produzione di citochine. Al tempo stesso, queste rilevazioni potrebbero svelare quel
meccanismo finora ignoto che spiegherebbe i successi clinici e l’enorme apporto favorevole
della terapia con Biobran MGN-3, come osservato dall’autore nel corso degli ultimi 4 anni.
Ghoneum M. (Università Ch. R. Drew, USA): Sintesi estrapolata dalla raccolta degli
interventi alla conferenza tenutasi in occasione dell’8° congresso internazionale sulle
tecnologie biomediche contro l’invecchiamento, 2000
3.4. Effetto integrativo nella cura del cancro
(a) Valutazione della correlazione tra attività delle cellule NK e tasso di sopravvivenza
nei pazienti con diversi tipi di cancro, con applicazione di protocolli terapeutici
multi-immunologici
Lo studio in questione si è prefissato come obiettivo quello di stabilire gli eventuali
effetti della somministrazione del preparato Biobran MGN-3 sull’allungamento della vita e
sul miglioramento della qualità della sopravvivenza, su un campione di 205 pazienti
oncologici con cancro progressivo e parzialmente metastatizzante in stadio III – IV
avanzato, dopo intervento chirurgico. Allo studio clinico hanno partecipato alcuni pazienti
ricoverati presso la clinica chirurgica di Sano, in Giappone. I pazienti erano in cura con
farmaci integrativi alternativi e medicinali anti-cancro convenzionali con deboli effetti
collaterali.
I 205 pazienti ricoverati per 6 mesi sono stati suddivisi in due gruppi: 109 pazienti del
gruppo di controllo sono stati sottoposti a trattamento con terapia alternativa integrativa
standard clinica, mentre agli altri 96 è stato somministrato in aggiunta il preparato MGN-3
per un periodo di un anno e mezzo.
Ai fini del rilevamento della variazione dei parametri immunitari è stata misurata in tutti
i pazienti l’attività delle cellule NK. Al tempo stesso, sempre in tutti i pazienti è stata
verificata la qualità della loro sopravvivenza. Nei pazienti dopo intervento chirurgico
l’attività delle cellule NK era prevalentemente bassa. Nei pazienti che assumevano Biobran
MGN-3 è stato osservato un tasso più alto di apotanasia (prolungamento della vita) – più
alta era l’attività delle cellule NK osservata, maggiore era quest’effetto sui pazienti
(Tabella 2). Tali rilevazioni hanno suggerito che il livello dell’attività delle cellule NK
può essere considerato come un indicatore patologico nei tipi di cancro progressivi. Nel
gruppo cui era stato somministrato anche Biobran MGN-3 è stato osservato allo stesso tempo
anche un miglioramento della qualità della vita.
Tabella 2: Rapporto tra tasso generale di sopravvivenza, attività delle cellule NK e tasso
di sopravvivenza nei 2 gruppi esaminati
| Gruppo |
Gruppo Biobran |
Gruppo controllo |
| Tasso generale di sopravvivenza |
52/96 (54.2%) |
19/63 (33.9%) |
Categorie in base all’attività delle cellule NK
Inferiore al 19.9%
20%-40%
Superiore al 40%
|
17/40 (42.5%)**
18/35 (51.4%)*
17/21 (81.0%)
|
2/16 (12.5%)
7/25 (28.0%)
10/15 (66.7%)
|
% di significatività rispetto al gruppo controllo **p<0,01 *p<0,05
Takahara K. (Clinica chirurgica di Sano, GIAPPONE): Sintesi estrapolata dalla riunione
tenutasi in occasione del 3° incontro annuale della Società giapponese per la medicina e
terapia integrativa e alternativa, 2000
(b) Effetti immunomodulatori e anti-cancro del preparato Biobran MGN-3 in 5 pazienti con
cancro della mammella
A cinque pazienti con cancro della mammella è stato somministrato il preparato MGN-3 alla
dose di 3 g/giorno; successivamente, mediante il test di separazione 51Cr è stata misurata
l’attività delle cellule NK sulle cellule tumorali bersaglio della linea K562. I risultati
hanno mostrato quanto segue:
-
A bassi livelli di attività delle cellule NK base (12,7 – 58,3%) e con rapporti
effector : target pari a 12 e 100 : 1, nella terapia con Biobran MGN-3 l’attività
delle cellule NK nelle pazienti ha fatto registrare notevoli aumenti (41,8 – 89,5%)
– e i rapporti effector : target sono rimasti invariati.
-
L’aumento dell’attività delle cellule NK è stato osservato già dopo 1-2 settimane
dall’inizio della terapia; man mano che si proseguiva con la somministrazione del
preparato Biobran MGN-3 i livelli andavano aumentando.
-
Due pazienti, che hanno partecipato allo studio fin dall’inizio (6-8 mesi di
terapia) sono giunte a completa remissione.
Ghoneum M. (Università Ch. R. Drew, USA): Raccolta degli inverventi della Conferenza
straordinaria dell’Associazione americana per la ricerca sul cancro, 1995
(c) Effetto immunomodulatore dell’arabinossilano modificato della crusca di riso contenuto
nel preparato Biobran MGN-3 sulle cellule NK in un gruppo di 27 pazienti oncologici
Oggetto di studio è stato l’effetto immunomodulatore del preparato Biobran MGN-3 su 27
pazienti oncologici. I pazienti soffrivano di vari tipi di malignità avanzate: 7 casi di
carcinoma mammario, 7 prostatici, 8 mielomi multipli, 3 leucemie e 2 carcinomi del collo
dell’utero. Tutti i pazienti sono stati sottoposti a terapia convenzionale, integrata con
MGN-3 alla dose di 3 g/giorno; successivamente è stata valutata l’attività delle cellule NK
dopo 2 settimane, 3 mesi e 6 mesi. L’attività delle cellule NK è stata valutata con test di
separazione 51Cr. Come cellule bersaglio sono state utilizzate delle cellule tumorali della
linea K562, con rapporti effector : target da 12:1 fino a 100:1. I risultati hanno mostrato
quanto segue:
- Livelli bassi di attività di cellule NK basilare nei pazienti.
- La terapia con Biobran MGN-3 ha dato adito ad un notevole aumento dell’attività delle
cellule NK già dopo 2 settimane. L’induzione dell’attività, nei singoli tipi di cancro,
è stata la seguente (in termini percentuali): carcinoma mammario 154-332%, carcinoma
prostatico 174-385%, leucemia 100-240%, mieloma multiplo 100-537% e carcinoma del collo
dell’utero 100-275%.
- L’attività delle cellule NK è stata continuamente in aumento anche dopo 3 e 6 mesi di
terapia.
Ghoneum M. (Università Ch. R. Drew, USA): Sintesi dell’intervento all’87° incontro annuale
dell’Associazione americana per la ricerca sul cancro, 1996
(d) Caso di terapia integrativa di cancro metastatizzante dei polmoni mediante
somministrazione del preparato Biobran MGN-3
Questo rapporto presenta un caso in cui sono stati raggiunti risultati positivi in
conseguenza dell’applicazione di terapia integrativa con il preparato Biobran MGN-3 in un
paziente con cancro dei polmoni metastatizzante con invasione di ampie zone ossee.
Il paziente era un maschio di 67 anni. Nell’agosto 1996 si è recato dal medico in seguito ad
un drastico calo ponderale e forte tosse con espettorato. Gli è stato diagnosticato un
cancro polmonare (carcinoma squamoso) complicato da tubercolosi (M. tuberculosis). Dopo
terapia antibiotica preliminare della tubercolosi, nel mese di ottobre è stata iniziata la
radioterapia contro il cancro. Nel dicembre dello stesso anno è stata chirurgicamente
rimossa la metà inferiore del polmone destro affetta da tumore. Dopo la radioterapia, nel
gennaio 1997, il paziente è stato dimesso dalle cure ospedaliere.
Nel giugno dello stesso anno il paziente è tornato dal medico lamentando dolore alla parte
destra del torace. La scintigrafia ossea ha confermato numerose metastasi alle ossa. Il
tumore si allargava soprattutto alle costole a destra, ma era diffuso nel tessuto osseo
praticamente in tutto il corpo. Nel mese di luglio è stata iniziata la terapia analgesica
con morfina. Nel frattempo, alla fine di maggio, era stata avviata anche la somministrazione
di Biobran MGN-3 a dosi di 3 al giorno. Dal gennaio 1998 i dolori si sono andati
affievolendo. Il Biobran MGN-3 continuava ad essere sistematicamente somministrato, mentre
la morfina veniva gradualmente ridotta fino alla sua eliminazione nel mese di giugno. Al
momento della conferma del ritorno della patologia, il marker tumorale ICPP era pari a 16,8
ng/ml, ma si è gradualmente ridotto a 7,6 ng/ml nel dicembre 1997 e a 6,7 ng/ml nel giugno
1998. La scintigrafia ossea mostrava ora un netto miglioramento, con conferma che la
diffusione del tumore alle ossa era in regressione. Al momento del ritorno della patologia
l’attività delle cellule NK era pari al 9,0%, ma è andata poi gradualmente incrementandosi e
tuttora si mantiene ad alti livelli.
Sobajima T. (Ospedale di Hoshigaoka Kosei Nenkin, GIAPPONE): Sintesi dell’intervento al
secondo incontro annuale della Società giapponese per la medicina e terapia integrativa e
alternativa, 1999
(e) Applicazione del preparato Biobran MGN-3 nella terapia post-convenzionale
Per quanto riguarda l’approccio alla cura del cancro in Giappone, la terapia del tumore
“dormiente” sta diventando sempre di più un concetto terapeutico. L’obiettivo principale di
tale cura è prolungare la vita del paziente e al tempo stesso mantenere una sua alta
qualità. Il Dr. Tunekawa la prescrive ai pazienti su loro richiesta, poiché ritiene che il
miglioramento della qualità della vita sia una finalità terapeutica importante. Nel suo
rapporto riporta di avere trentaquattro pazienti oncologici cui somministra una combinazione
di chemioterapia (per sopprimere tumori dormienti) e terapie integrative e alternative. In
tre casi specifici descrive anche la concreta procedura terapeutica:
-
Pazienti (patologie principali): cancro dello stomaco in 3 casi, carcinoma
polmonare in 3 casi, linfoma maligno in 2 casi, carcinoma colorettale (parte
rettale) in 6, carcinoma mammario in 3 casi e altri tipi di cancro in 17 casi
-
Periodo di terapia: 6-18 mesi
-
Studi di caso
-
T.S. (60), sesso femminile, cancro dello stomaco (IV stadio), infiammazione
carcinomatosa del peritoneo: nel gennaio 2000 è stato chirurgicamente asportato un
tumore scirroso dello stomaco. Nel febbraio 2000 si è sviluppata un’infiammazione
carcinomatosa del peritoneo e la paziente (al IV stadio) è stata sottoposta a
gastrectomia. Il CA19-9 era pari a 108. Nell’agosto 2000 ha visitato la nostra
clinica lamentando dolori all’addome, costipazione, anemia e anoressia. Il CA19-9
era pari a 390 e l’attività delle cellule NK 25,6. Le è stata prescritta una
combinazione di chemioterapia (TS1) e terapia olistica. Per migliorare l’immunità le
è stato prescritto il preparato Biobran MGN-3 a dosi da 3 g al giorno. Un mese dopo
i valori di CA19-9 erano pari a 63. I valori dei marker tumorali si sono andati
gradualmente riducendo e l’attività delle cellule NK invece aumentava. Nell’agosto
2001, ovvero 11 mesi dopo, il valore di CA19-9 era pari a 25 e l’attività delle
cellule NK a 51,5. Attualmente la paziente non avverte più alcun sintomo soggettivo
ed è ben nutrita.
-
F.A. (46), sesso femminile, carcinoma mammario, con metastasi a vertebra lombare e
utero: nel luglio 1998 la paziente è stata sottoposta ad operazione per carcinoma
mammario ed è stata instaurata terapia ormonale anticancro. Nel marzo 2001 sono
state riscontrate metastasi alla vertebra lombare e nel mese di aprile anche
all’utero. Nel maggio 2001 è stata sottoposta ad isterectomia. È stata poi dimessa
con somministrazione di Taxol e Paraplatin. Nel luglio 2001 si è recata dal Dr.
Tunekawa lamentando dolori alle ossa. In quel momento il livello di CA era = 153,
NCC-ST = 439 e attività delle cellule NK = 9,3. La cura è stata modificata
conservando il Paraplatin e aggiungendo terapia olistica. Per migliorare l’immunità
è stato aggiunto anche il preparato Biobran MGN-3 a dosi da 3 g al giorno. Due mesi
dopo i marker CA erano = 18, NCC-ST = 28,9 e attività delle cellule NK = 22,0, con
inoltre diminuzione del dolore. Successivamente nella paziente è stata osservata una
riduzione stabile dei livelli di marker tumorali, con aumento dell’attività delle
cellule NK. Nel luglio 2002 i livelli di CA erano = 14, NCC-ST = 3,2 e attività
delle cellule NK = 59. Il dolore era completamente scomparso e le rilevazioni alla
scintigrafia ossea erano meno manifeste. Attualmente la paziente è ben nutrita ed è
tornata felicemente a suonare la batteria.
Tunekawa H. (Società di Tokai per la promozione della medicina olistica, GIAPPONE): Sintesi
del workshop sul preparato Biobran, Berlino, 2002
(f) Valutazione dell’azione del preparato Biobran MGN-3 nella cura del cancro in stadio
progressivo
Il Dr. Mizukami ha descritto la propria esperienza di somministrazione del preparato Biobran
MGN-3 ad un gruppo campione di 97 pazienti oncologici affetti da diversi tipi di tumore in
stadio progressivo (cancro dello stomaco, colon-retto, mammella, polmoni, pancreas, fegato,
cistifellea, faringe, ovaio, collo dell’utero, reni, tiroide, prostata, cavità orale,
mieloma multiplo, ecc). I paziente erano già stati sottoposti ad interventi chirurgici,
chemioterapia o radioterapia in grandi ospedali, ma le prognosi non erano incoraggianti.
Presentavano metastasi e recidive. Hanno pertanto deciso di recarsi presso la clinica del
Dr. Mizukami e tentare con l’immuno-terapia. Quasi tutti i pazienti cui era stato prescritto
il Biobran MGN-3 in quel periodo aveva già terminato la chemioterapia o radioterapia. Sulla
base delle osservazioni cliniche e dei questionari è stata poi analizzata dettagliatamente
la qualità della sopravvivenza. In tutti i pazienti che assumevano il Biobran MGN-3 è stato
osservato un fenomeno comune.
In alcuni casi, con il preparato Biobran MGN-3 la qualità della sopravvivenza ha subito
miglioramenti significativi. Nonostante il fatto che nei pazienti con cancro in stadio
avanzato la qualità della sopravvivenza tenda col tempo a peggiorare, nei pazienti che
assumevano Biobran MGN-3 la tendenza era ben più moderata e addirittura è stata osservata
una sopravvivenza ben più prolungata, con buona qualità della vita, compresi casi di
sopravvivenza a lungo termine.
Per quanto riguarda la qualità della sopravvivenza si riportano le seguenti
osservazioni:
-
Non è affatto semplice tenere sotto controllo dolori atroci. Nei pazienti con cancro
in stadio avanzato non v’è altra possibile soluzione se non la morfina. Eppure
alcuni pazienti in cura con Biobran MGN-3 non hanno avuto bisogno della morfina,
mentre in alcuni altri (sempre facenti uso di Biobran MGN-3) è stata registrata una
tendenza alla riduzione delle dosi di morfina.
-
In generale è stata osservata una tendenza minore in termini di sensazioni di
debolezza.
-
È stata osservata una tendenza minore in termini di perdita di appetito.
-
Tendenza alla capacità di rimanere a casa e sentirsi relativamente bene prima della
morte.
-
Tendenza a conservare una mente chiara prima della morte e comunicare con i
familiari.
Il Dr. Mizukami ha riepilogato le proprie osservazioni constatando un dato di fatto
fondamentale, ovvero che nei pazienti con cancro in stato avanzato, con l’impiego del
preparato Biobran MGN-3, la qualità della sopravvivenza non subisce peggioramenti rapidi ed
improvvisi. Questa constatazione appare per il futuro come un aspetto importante anche per
l’approccio medico generale al trattamento del cancro.
Mizukami O. (Istituto di ricerca per la promozione della salute e Fondazione Layman New
Life, GIAPPONE): Sintesi del workshop sul preparato Biobran, Berlino, 2002
3.5. Effetto sull’apoptosi
Biobran MGN-3 sensibilizza le cellule T leucemiche umane all’apoptosi indotta dal recettore
di morte (CD95)
Oggetto di studio è stato l’effetto del preparato Biobran MGN-3 sull’apoptosi indotta dal
recettore di morte nelle cellule leucemiche umane della linea HUT 78. Le cellule HUT 78 sono
state dapprima trattate con Biobran MGN-3 e successivamente incubate con anticorpo del
recettore di morte (Fas, CD95). Il tasso di apoptosi è stato stabilito con citometria di
flusso FACScan con colorazione con ioduro di propidio. L’attivazione della caspasi 3,
caspasi 8 e caspasi 9 è stata stabilita con citometria di flusso. Il potenziale di membrana
mitocondriale è stato misurato mediante FACScan con colorazione DIOC6. L’espressione di CD95
e BCI-2 è stata misurata con citometria di flusso.
In base alle rilevazioni, Biobran MGN-3 (a seconda del dosaggio) aumenta il taso di apoptosi
indotta da anti-CD95. Il tasso aumentato della morte cellulare è risultato correlato
all’aumento della depolarizzazione del potenziale di membrana mitocondriale e ad
un’attivazione aumentata della caspasi 3, caspasi 8 e caspasi 9. Il trattamento con Biobran
MGN-3 non ha influito sull’espressione di CD95, ma ha causato una sottoregolazione
dell’espressione di BCI-2. I risultati suggeriscono che Biobran MGN-3 incrementa la
sensibilità del cancro all’apoptosi mediata da leganti di morte cellulare. Si tratta di
un’osservazione potenzialmente di fondamentale importanza nell’ambito della lotta contro il
cancro.
Ghoneum M. (Università Ch. R. Drew, USA): Cancer Letters (Lettere oncologiche), 2003
3.6. Attivazione della difesa vitale
(a) Azione attiva del preparato Biobran MGN-3 nell’eliminazione dei radicali ossigeno
Il rapporto verte su un’esperienza di ricerca finalizzata all’azione di eliminazione dei
radicali ossigeno da parte del preparato Biobran MGN-3 e sue frazioni. Il Biobran MGN-3 è
stato frazionato mediante colonna Sephadex G-25. In base alle dimensioni le singole frazioni
sono state contrassegnate come L, M e S (L peso molecolare > 10000), M (peso molecolare da
10000 a 3000) e S (peso molecolare < 3,000).
L’azione di eliminazione degli enzimi attivi è stata valutata misurando l’azione di
eliminazione a danno di: anione superossido – radicale (•O2), radicale ossidrile originato
da reattivo di Fent (•OH) e radicale ossidrile generato da raggi ultravioletti.
I risultati delle misurazioni sono raffigurati nella tabella riportata qui di seguito. Per
quanto concerne la formazione di radicale idrossile •OH generato da •O2 e raggi
ultravioletti, i migliori risultati in termini di inibizione sono stati ottenuti dalla
frazione del preparato Biobran contrassegnata come S (con il peso molecolare più basso). Per
quanto concerne invece l’eliminazione dell’idrossile (•OH) generato da reattivo di Fent,
tutte le frazioni del preparato hanno mostrato un alto tasso di efficacia. (Tabella 3)
Tabella 3
Azione di eliminazione del preparato Biobran MGN-3 a danno dei radicali ossigeno attivi
(•O2 e •OH e •OH indotti da raggi ultravioletti)
| Tipo di ossigeno attivo e azione SOD |
Tasso di eliminazione dell’anione superossido – radicale (%) |
Azione SOD (superossidismutasi) (U/ml) |
Tasso di eliminazione del radicale idrossile indotto da raggi UV (%)
|
| 20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
BioB
BioB-L
BioB-M
BioB-S
|
64.6
39.9
49.5
90.4
|
23.0
10.4
15.6
68.1
|
4.4
0
0
26.4
|
7.6
5.0
7.2
70.5
|
0.9
0.8
1.4
15.7
|
0
0
0
2.6
|
94.9
(72.6)
97.2
(41.8)
97.0
(45.4)
96.5
(71.0
|
78.9
(35.9)
34.4
(16.5)
68.4
(9.9)
55.1
(54.9)
|
3.3
(11.5)
3.3
(1.0)
8.7
(3.9)
4.2
(19.6)
|
·O2: reazione HPX-XOD,·OH: reattivo di Fent
·OH generato da reazione UV: 365nm,4×103J/m2/min×5
Tazawa K. (Università di Medicina e Farmacia di Toyama, GIAPPONE): Biotherapy (Bioterapia)
Vol.14, 2000
(b) Studio basilare dell’influenza del composto di arabinossilano (Biobran MGN-3)
sull’attivazione delle difese vitali.
Mediante sperimentazione su animali, questo studio si è incentrato sull’osservazione
dell’influenza del preparato Biobran MGN-3 e della sua azione biofilattica, nonché sul tasso
di sopravvivenza dopo induzione di sepsi letale con lipopolisaccaride (LPS).
Per questo esperimento sono stati utilizzati dei topi BALB/c (maschi di età 5-7 settimane).
Un giorno su due, su un periodo di due settimane (ovvero sette volte in tutto), mediante
sonda orale sono state somministrate ai topi dosi da 20 mg/kg e 200 mg/kg di preparato
Biobran MGN-3 disciolto in tampone fosfato salino (PBS) di volume 0,5 ml. Quanto ai topi del
gruppo controllo, sono stati somministrati 0,5 ml di PBS ad eguali intervalli. Dodici ore
dopo l’ultima dose orale, in ciascun esemplare murino sono stati iniettati
intraperitonealmente 200 µg di LPS, con successivo monitoraggio delle condizioni degli
stessi esemplari. In un secondo esperimento, nei topi di entrambi i gruppi (gruppo Biobran e
controllo) sono stati iniettati intraperitonealmente 100 µg di LPS; i topi sono stati
successivamente soppressi ad intervalli di 0, 2, 4 e 8 dopo somministrazione di LPS ed è
stato prelevato del sangue periferico del loro cuore. Dopo la separazione del siero sono
stati misurati i valori di IL-6 e TNF. L’attività di IL-6 è stata misurata mediante impiego
di cellule della linea B9, mentre per l’attività TNF si è ricorso ad esame biologico sulle
cellule della linea WEHI164-13.
Come risulta chiaro dalla fig. 9, dopo somministrazione di 200 µg LPS il tasso di
sopravvivenza (rispetto al gruppo controllo) si è rivelato sostanzialmente migliore nei
gruppi in cui gli esemplari assumevano ogni giorno 20 mg/kg e 200 mg/kg di preparato Biobran
MGN-3 (gruppo Biobran MGN-3 20 mg/kg vs. gruppo controllo, p = 0,0456; gruppo Biobran MGN-3
200 mg/kg vs. gruppo controllo, p = 0,0232, analisi con test Mantel-Cox). Nel caso della
somministrazione di 100 µg di LPS/esemplare nei gruppi in cui precedentemente era stato
somministrato Biobran MGN-3 a dosi da 20 mg/kg e 200 mg/kg, tutti i topi sono sopravvissuti;
mentre nel gruppo controllo sono morti 3 esemplari su 10.
Nel tentativo di svelare il meccanismo responsabile del miglioramento del tasso di
sopravvivenza nel gruppo Biobran MGN-3 sono state misurate le concentrazioni di IL-6 e TNF
nel sangue. Nel gruppo in cui era stato somministrato Biobran MGN-3 la concentrazione
ematica di IL-6 (dopo due ore dalla somministrazione di LPS) risultava significativamente
più bassa rispetto al gruppo controllo (gruppo controllo 702,9 ± 24,7 ng/ml, gruppo Biobran
MGN-3 403,1 ± 59,6 ng/ml; p < 0.01); tuttavia, dopo 8 ore dalla somministrazione, veniva ad
essere notevolmente aumentata (gruppo controllo 88,5 ± 50,0 ng/ml, gruppo Biobran
MGN-3 441,0 ± 115,0 ng/ml; p < 0.05). Quattro ore dopo la somministrazione di LPS nel gruppo
Biobran MGN-3 la concentrazione ematica di TNF ha fatto registrare aumenti notevoli rispetto
al gruppo controllo (gruppo controllo 492 ± 187, gruppo Biobran MGN-3 1816 ± 307 pg/ml; p <
0.01).
Nell’ambito del modello sperimentale della sepsi letale indotta da LPS si prevedeva che la
gran quantità di citochine infiammatorie (IL-1, 6, TNF-α) rilasciate dalle cellule del
sistema reticoloendoteliale in tutto l’organismo sarebbe stata la causa del deficit di
svariati organi – e dunque del decesso. Tuttavia, in questo studio, nel gruppo sottoposto a
somministrazione del preparato MGN-3 è stato osservato un notevole aumento del tasso di
sopravvivenza. Come possibili cause possiamo pensare al fatto che l’assunzione del preparato
Biobran MGN-3 inibisce la formazione di citochine istotossiche prodotte dai macrofagi oppure
che il Biobran MGN-3 blocca la strada all’istotossicità a livello di cellule bersaglio.
Sudo N., Kubo C. (Università di Kyushu, GIAPPONE): The Japanese Journal of Clinical and
Experimental Medicine (Rivista giapponese per la medicina clinica e sperimentale), Vol. 78,
1, 2001
(c) Riduzione del calo ponderale nei topi dopo somministrazione di cisplatino grazie al
preparato Biobran MGN-3.
Nel trattamento del cancro, i medicinali contenenti platino causano spesso effetti
collaterali importanti, come nausea, vomito, nefropatie e ipomagnesemia, con danni ai tubuli
renali (Lajer & Dangaard 1999); si osservano inoltre anche deficit dell’udito, nefropatie
periferiche e mielosoppressione, uno degli effetti collaterali più devastanti (Prestayko et
al. 1979) che porta all’indebolimento delle difese immunitarie. Per questo motivo, qualsiasi
limitazione degli effetti collaterali del cisplatino è sempre preziosa e ben gradita. Ci
siamo dunque incentrati sull’analisi dell’influenza del preparato Biobran MGN-3 sulla
riduzione del calo ponderale in topi sottoposti a dosi massime tollerabili di cisplatino.
Una settimana prima della somministrazione del cisplatino abbiamo iniziato la
somministrazione anche di Biobran MGN-3 in due gruppi di topi, a dosi di 10 mg/ml (di
materia asciutta) in acqua, oppure con iniezione intraperitoneale di volume 0,1 ml, dove la
dose equivalente del preparato è stata disciolta in una soluzione fisiologica di fosfato
(PBS). La dose da 1 mg per esemplare è stata dedotta dalla dose consigliata per l’essere
umano (50 mg/kg). La dose da 15 mg/kg è stata somministrata intraperitonealmente in 0,1 ml
di tampone fosfato salino (PBS) con contenuto pari allo 0,5% di acido DMSO come vettore. Due
gruppi di topi hanno ricevuto acqua mediante una sonda oppure PBS intraperitonealmente. Dopo
una settimana, è stato dato inizio alla somministrazione di cisplatino in entrambi i gruppi.
Il calo ponderale è insorto già dal primo giorno successivo all’iniezione
intraperitoneale di cisplatino in entrambi i gruppi (sia quello che assumeva Biobran MGN-3
sia quello senza). Sempre in entrambi i gruppi, il calo ponderale massimo è stato osservato
il 5° giorno dopo somministrazione di cisplatino – anche qui il dato è stato registrato in
entrambi i gruppi (sia quello che assumeva Biobran MGN-3 sia quello senza) e sia con
somministrazione orale sia intraperitoneale. Il calo ponderale più importante è stato
osservato nei topi soggetti a cisplatino senza preparato Biobran MGN-3. Se da un lato è vero
che la perdita di peso nei topi con Biobran MGN-3 si avvicinava al 20% di quanto osservato
nei topi del gruppo cisplatino senza Biobran MGN-3, dall’altro lato bisogna constatare che
in quest’ultimo gruppo nessun topo è morto, né ha presentato diarrea o sangue fecale –
ovvero effetti collaterali che di norma accompagnano la sommistrazione del cisplatino.
Durante la fase di convalescenza, i topi del gruppo Biobran MGN-3 hanno fatto registrare una
riassunzione di peso ben più rapida che nel gruppo senza Biobran MGN-3.
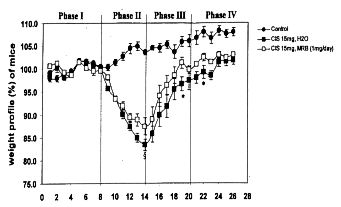 Fig. 10 Legenda: profilo ponderale dei topi (v%)
Fig. 10 Legenda: profilo ponderale dei topi (v%)
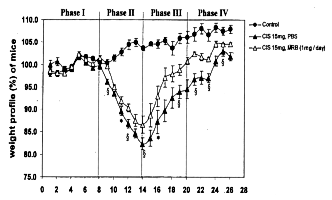 Fig. 11
Fig. 11
Endo Y., Kanbayashi H. (Università McMaster, CANADA): Pharmacology and Toxicology
(Farmacologia e tossicologia), 2003
(d) Influenza del preparato Biobran MGN-3 sul cisplatino e sulla tossicità indotta da
adriamicina nei ratti
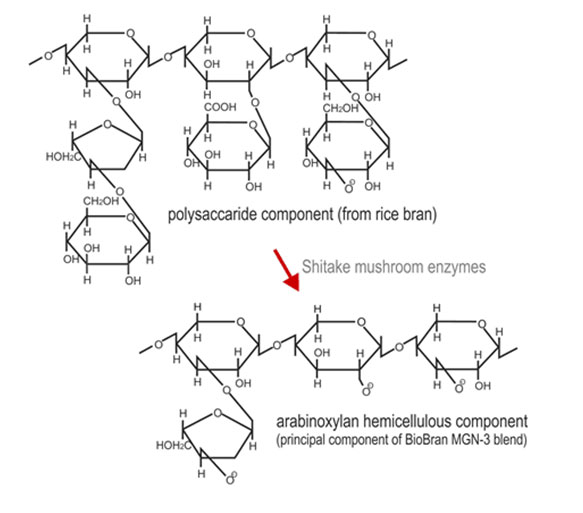
Biobran MGN-3 è un derivato della crusca di riso, prodotto mediante idrolisi parziale in
acqua di frazioni solubili di fibra di riso tramite carboidrasi ricavata dal fungo lentinus
edodes [n. brevetto USA 5560914]. È stato dimostrato che il Biobran MGN-3 è un modificatore
della risposta biologica in grado di favorire l’aumento dell’attività delle cellule NK nei
pazienti con deficit immunitari [Int. J. Immunother. 14 (1) 1998].
Obiettivo: mediante somministrazione giornaliera del preparato Biobran
MGN-3 a dosi di 5 e 50 mg/kg, evitare modifiche patologiche gravi e cali ponderali connessi
alla somministrazione di una dose unica di cisplatino (CIS) o adriamicina (ADR). Dopo 13
giorni di ambientamento, secondo il criterio selettivo del peso corporeo sono stati scelti
per il test alcuni individui maschi di ratto Spaque-Dawley, suddivisi successivamente in
otto gruppi da 10 membri (dosi riportate in mg/ml):
-
Biobran 5 mg p.o. + vettore i.p.
-
Biobran 50 mg p.o. + vettore i.p.
-
Biobran controllo p.o. + CIS 8 mg i.p.
-
Biobran 5 mg p.o. + CIS 8 mg i.p.
-
Biobran 50 mg p.o. + CIS 8 mg i.p.
-
Biobran controllo p.o. + ADR 10 mg i.p.
-
Biobran 5 mg p.o. + ADR 10 mg i.p.
-
Biobran 50 mg p.o. + ADR 10 mg i.p.
Per 11 giorni i ratti sono stati sottoposti a somministrazione per via orale (p.o.) di
preparato MGN-3 disciolto in acqua distillata oppure vettore. Il farmaco chemoterapeutico o
il vettore sono stati somministrati nel 3° giorno a ciascuno degli individui testati
attraverso iniezione intraperitoneale (i.p.) unica. Durante queti 11 giorni sono stati
quotidianamente monitorati i sintomi clinici dei ratti. Il peso corporeo è stato registrato
un giorno sì e uno no. All’11° giorno i ratti sono stati soppressi con inalazione di CO2 ed
è stata eseguita l’autopsia. È stato effettuato un controllo visivo degli organi principali
e sono stati verbalizzati i danni all’apparato gastro-intestinale.
Risultati: Tra il 7° e l’11° giorno sono morti cinque ratti del gruppo 3,
tre ratti del gruppo 5 e un ratto del gruppo 4. I ratti cui era stato somministrato
esclusivamente Biobran MGN-3 a dosi di 5 o 50 mg/kg p.o. hanno fatto registrare un aumento
di peso statisticamente significativo (+72%). I ratti cui era stato somministrato
esclusivamente CIS o ADR hanno fatto registrare un aumento di peso esiguo (-1,5% per CIS e
+30% per ADR). I ratti cui era stato somministrato Biobran MGN-3 a dosi di 5 o 50 mg + CIS o
ADR hanno fatto registrare un aumento di peso ben più importante rispetto ai ratti del
gruppo puramente chemioterapico (+11% nel gruppo Biobran MGN-3 5 mg + CIS e +46% nel gruppo
+ ADR). Nel gruppo Biobran MGN-3 50 mg + CIS l’aumento ponderale è stato +44% e nel gruppo
Biobran MGN-3 50 mg + ADR +43%. I ratti sopravvissuti cui era stato somministrato Biobran
MGN-3, rispetto a quelli che avevano ricevuto solo CIS o ADR senza preparato Biobran MGN-3,
avevano un aspetto più sano, avevano preso peso e mostravano minore frequenza di patologie
intestinali gravi.
Tabella 4: Effetto del preparato Biobran sulla riduzione del calo ponderale
indotto da cisplatino e doxorubicina
| Terapia (tutto intraperitoneale) |
Giorno 0 |
Giorno 3 |
Giorno 5 |
Giorno 7 |
Giorno 9 |
Giorno 11 |
5mg/kg p.o. + vettore
50mg/kg p.o. + vettore
Gruppo controllo p.o.+ Cp8mg/kg
5mg/kg p.o. + Cp8mg/kg
50mg/kg p.o. + Cp8mg/kg
Gruppo controllo p.o. + Dx10mg/kg
5mgn/kg p.o. + Dx10mg/kg
50mg/kg p.o. + Dx10mg/kg
|
100
100
103
99
101
103
101
101
|
100
98
101
99
99
100
100
101
|
100
100
82
85
92
88
92
92
|
100
97
69
76
90
82
89
87
|
100
97
55
68
85
77
86
85
|
100
97
57
65
84
76
85
83 |
p.o.- per via orale, Dx-doxorubicina, Cp-cisplatino
Jacoby H. I. (USA): Journal of Nuturaceuticals, Function & Medical Foods (Časopis pre
naturaceutíka a funkčné a zdravotné potraviny), Vol.3 (4) 2001
(e) Effetto del preparato Biobran MGN-3 sulla tossicità indotta da radioterapia nei
topi
L’obiettivo di questo studio è stato quello di analizzare l’effetto modificatore del
preparato Biobran MGN-3 sulla radiosensibilità che si manifesta con riduzione del midollo
osseo in conseguenza di irradiazione totale dell’organismo. Nell’intento di contemplare
un’eventuale applicabilità clinica, gli autori hanno testato gli effetti a livello
quantitativo nell’arco dell’intero spettro delle dosi radioterapiche (da 4,5 a 8,5 Gy).
Per l’esperimento sono stati impiegati esemplari maschi di topo dell’età di 4 o 5 settimane,
di tipo SPF BALB/c (gruppo F2). Nei gruppi selezionati è stato aggiunto all’alimentazione
degli animali anche il preparato MGN-3 a dosi di 50 mg/kg di massa corporea. I gruppi erano
formati da 10 – 50 individui. Dopo due giorni di ambientamento è stato aggiunto Biobran
MGN-3 alla dieta dei topi del gruppo test (F2). Dopo 8 e 15 giorni di somministrazione del
preparato Biobran MGN-3 i topi sono stati esposti ad irradiazione. Successivamente il loro
peso corporeo è stato controllato 3 volte a settimana ed ogni giorno veniva monitorato il
tasso di decesso. In alcuni casi, nell’ambito dell’esperimento, il Biobran MGN-3 è stato
somministrato ai topi per due settimane intere prima dell’irradiazione; in altri casi la sua
somministrazione è stata iniziata solo dopo l’irradiazione.
Nel gruppo F2 i decessi dei topi sono stati osservati già a partire dal settimo giorno dopo
irradiazione, in conseguenza della riduzione di midollo osseo. I topi dei gruppi Biobran
MGN-3 tendevano invece a morire per le radiazioni diverso tempo dopo. La dose LD50 (che ha
causato la morte di almeno metà degli animali colpiti) era pari a ca. 5,15 Gy e il fattore
di riduzione di dose (DRF) si assestava ad un livello di ca. 1,14. Per quanto riguarda il
peso corporeo, nei gruppi Biobran MGN-3 è stata osservata una tendenza al mantenimento di un
peso più alto. Gli effetti osservati con inizio precoce della somministrazione del preparato
Biobran MGN-3 suggeriscono che è più opportuno iniziare ad assumere il preparato prima
ancora della radioterapia.
La dose di irradiazione dei topi al centro dell’organismo è stata calcolata come un multiplo
di 1,21 volte rispetto alle dosi sopra riportate; vale a dire che la dose LD50 per gli
esemplari del gruppo controllo era pari a 6,23 Gy. Sebbene l’effetto radioprotettivo (DRF)
del Biobran (pari a 1,14) non si sia rivelato altissimo, bisogna aggiungere che nell’ambito
dell’intero studio non è stato osservato neppure un effetto collaterale.
Nakatugawa S. (Università di Nagoya, GIAPPONE): The Report of Nagoya Univ. (Rapporto
dell’Univ. di Nagoya), 2003
(f) Effetto del preparato Biobran MGN-3 sulla disfunzione epatica sperimentalmente indotta
nei ratti
Nell’ambito di questo studio è stato analizzato l’effetto del preparato Biobran MGN-3 sulla
disfunzione epatica. In modo particolare è stato studiato l’effetto del preparato sullo
sviluppo di disfunzioni epatiche sperimentalmente indotte in conseguenza di somministrazione
di galattosammina (GaIN) e acetaminofene (AAP). La GaIN è stata somministrata negli
esperimenti da 1 a 3, mentre l’AAP negli esperimenti 4 e 5.
Nell’esperimento n. 1 il preparato MGN-3 è stato somministrato ai ratti per via
intraperitoneale a diverse concentrazioni; dopo 1 ora è stata introdotta nel corpo la GaIN a
dosi di 800 mg/kg.
Nell’esperimento n. 2 Biobran MGN-3 è stato somministrato per via orale, mentre per via
intraperitoneale sono state introdotte solo le sue frazioni con peso molecolare basso o
alto. Dopo 1 ora è stata introdotta nell’organismo dei ratti anche la GaIN a dosi di 800
mg/kg.
Nell’esperimento n. 3 Biobran MGN-3 è stato somministrato per via intraperitoneale dopo
essere stato previamente scaldato, idrolizzato e filtrato con resina a scambio ionico. Dopo
1 ora è stata introdotta nei ratti anche la GaIN a dosi di 800 mg/kg.
Nell’esperimento n. 4 Biobran MGN-3 è stato somministrato per via sia intraperitoneale sia
orale. Dopo 1 ora è stato introdotto nell’organismo dei ratti anche l’AAP a dosi di 700
mg/kg.
Nell’esperimento n. 5 Biobran MGN-3 è stato somministrato per via intraperitoneale dopo
essere stato previamente scaldato, idrolizzato e filtrato con resina a scambio ionico. Dopo
1 ora è stato introdotto nei ratti anche l’AAP a dosi di 500 mg/kg.
In tutti gli esperimenti i ratti sono stati soppressi dopo 24 ore dalla somministrazione di
GaIN o AAP e sono stati stabiliti i valori di transaminasi sierica (GOT, GPT).
Risultati
Esperimento 1: In tutti i gruppi cui era stato somministrato Biobran MGN-3
l’attività della transaminasi sierica (GOT e GPT) scatenata dalla disfunzione epatica
indotta da GaIN appariva significamente repressa, rispetto all’attività osservata nel gruppo
controllo. L’effetto soppressivo del preparato Biobran MGN-3 sulla disfunzione epatica
indotta da GaIN arrivava al suo culmine alla dose di 20 mg/kg, mentre a dosi più alte di
Biobran MGN-3 smetteva di salire ulteriormente.
Esperimento 2: In tutti i gruppi cui era stato somministrato Biobran MGN-3
(non frazionato, frazionato, con peso molecolare alto o basso) gli aumenti dell’attività
della GPT sierica conseguenti a disfunzione epatica indotta da GaIN sono apparsi
significativamente repressi, rispetto agli aumenti riscontrati nel gruppo controllo. Gli
effetti soppressivi del preparato Biobran MGN-3 frazionato o non frazionato si sono rivelati
di simile intensità.
Esperimento 3: Nei gruppi in cui era stato somministrato Biobran MGN-3
idrolizzato, gli aumenti dell’attività della GOT sierica conseguenti a disfunzione epatica
indotta da GaIN sono apparsi significativamente repressi, rispetto agli aumenti riscontrati
nel gruppo controllo.
Esperimento 4: Nei gruppi in cui era stato somministrato Biobran MGN-3 per
via sia intraperitoneale sia orale, gli aumenti dell’attività della GOT sierica conseguenti
a disfunzione epatica indotta da AAP sono apparsi significativamente repressi, rispetto agli
aumenti riscontrati nel gruppo controllo.
Esperimento 5: Risultati simili all’esperimento n. 3 sono stati raggiunti
con il Biobran MGN-3 idrolizzato anche dopo somministrazione di AAP. Nei gruppi in cui era
stato somministrato Biobran MGN-3 idrolizzato, gli aumenti dell’attività della GOT sierica
sono apparsi significativamente repressi, rispetto agli aumenti riscontrati nel gruppo
controllo.
È stato dunque confermato che Biobran MGN-3 ha effetti soppressivi sulla disfunzione epatica
indotta da GaIN o AAP. La componente attiva HCl del preparato sembra non essere
idrolizzante.
Yamada T. (Università di Chiba, GIAPPONE): Sintesi dell’intervento alla 6° riunione
dell’Associazione giapponese per la ricerca sulle fibre alimentari, 2002
(g) L’assunzione orale del preparato Biobran MGN-3 mitiga gli effetti della sindrome del
raffreddore comune nelle persone anziane
Nelle persone ad alto rischio (come anziani e bambini) è importante prestare attenzione alle
misure di prevenzione contro le infezioni (come il vaccino antinfluenzale) e soprattutto
alla misure volte ad impedire infezioni batteriali secondarie. Studiando in base all’età i
casi di polmonite contratta dall’ambiente e sviluppatasi tramite peggioramento di un
raffreddore comune, è stato scoperto che il rischio di infezioni batteriali secondarie è più
elevato negli anziani al di sopra di 75 anni. Il rischio di infiammazione concomitante dei
polmoni è anch’esso più elevato nei pazienti anziani con patologie neurologiche, dov’è
presente un alto rischio di aspirazione. Per questo motivo abbiamo studiato clinicamente
l’apporto del preparato Biobran MGN-3 come forma di prevenzione contro lo sviluppo di
raffreddore comune negli anziani con capacità reattiva immunitaria ridotta in conseguenza di
diversi fattori.
Tra il mese di gennaio e marzo 2002, tra i clienti del centro sanitario “Atreyu Uozaki” di
Kobe, prefettura di Hjógó, è stato selezionato un gruppo di persone anziane senza alcuna
patologia grave precedente e che hanno dato il proprio consenso alla partecipazione allo
studio. Oggetto del test è stato un integratore alimentare, frazione del preparato Biobran
MGN-3 (HRB). Nel gruppo controllo è stata impiegata fibra di riso contenente principalmente
componenti solubili in acqua (RB).
Per quanto riguarda i sintomi del raffreddore (febbre, mal di testa, stanchezza, brividi,
tosse, muco, naso chiuso, mal di gola, dolore al torace), è stato calcolato il numero di
giorni durante il quale si è manifestato anche uno solo di questi sintomi. Ciascun sintomo è
stato caratterizzato da un punteggio a seconda dell’intensità (non manifesto = 0,
moderatamente manifesto = 1, mediamente = 2, significativamente = 3). Successivamente il
punteggio totale di ciascun paziente è stato diviso per il numero di giorni di assunzione di
sostanza test e si è così passati al calcolo del “punteggio sintomatico del raffreddore” in
ciascun paziente.
Risultati: tra i singoli sintomi, all’inizio del trattamento in entrambi i
gruppi si osservavano alti livelli di “tosse”, “astenia”, “febbre” e “mal di gola”. Nel
gruppo HRB il numero totale di giorni di presenza dei sintomi è risultato minore rispetto al
gruppo RB. Nel gruppo RB è stato registrato il punteggio sintomatico più alto in termini
assoluti. Nel gruppo RB il punteggio dei “sintomi nasali” è risultato relativamente basso,
ma gli altri sintomi presentavano valori assai alti (“tosse”, “astenia” e “febbre”). Per
questo motivo si è giunti alla conclusione che i sintomi del raffreddore comune erano
presenti solo in misura minore nel gruppo HRB.
Lo studio ha mostrato che, in caso di somministrazione orale di HRB a pazienti anziani con
raffreddore comune, l’azione immuno-stimolante dell’estratto accorcia la durata delle
manifestazioni sintomatiche, senza peggioramento degli stessi sintomi e con riduzione del
bisogno di ricorrere a terapie sintomatiche.
Tazawa K. (Università di Medicina e Farmacia di Toyama, GIAPPONE): Rivista di medicina
tradizionale, 20 (3), 2003
3.7. Azione antiallergica
(a) Valutazione dell’azione di prevenzione del preparato Biobran MGN-3 e mitigazione dei
sintomi dell’asma nel modello asmatico murino
Nell’ambito di questo studio è stata monitorata l’azione preventiva del preparato Biobran
MGN-3 e la mitigazione dei sintomi dell’asma nel modello murino di asma indotta da
diisocianato di toluene (TDI).
In fase iniziale è stata preparata una soluzione di acqua potabile e preparato Biobran MGN-3
a concentrazioni di 2 g/litro. La stessa è stata poi somministrata ai topi (femmine di
BALB/c), suddivisi in 4 gruppi (A-D):
Gruppo A: Biobran MGN-3 è stato somministrato un mese prima e durante la
fase di sensibilizzazione al TDI, ed ancora durante il periodo di tempo successivo.
Gruppo B: Biobran MGN-3 è stato somministrato un mese prima e dopo, fino al
termine della fase di sensibilizzazione al TDI.
Gruppo C: Biobran MGN-3 è stato somministrato solo durante la fase di
sensibilizzazione al TDI.
Gruppo D: Gruppo controllo.
Nel gruppo B è stata valutata l’azione preventiva. Nel gruppo C è stato invece studiato
l’effetto di mitigazione dei sintomi. L’effetto del preparato Biobran è stato valutato in
base alle concentrazioni ematiche di istamina, numero di eosinofili nel lavaggio del
parenchima polmonare (BALF), test di applicazione di TDI dall’auricola e valori di anticorpi
tipo-specifici IgG1, IgG2a, IgE nel sangue durante la sensibilizzazione.
Le concentrazioni più alte di istamina nel sangue sono state misurate 7 minuti dopo la
somministrazione di TDI, con i seguenti risultati: gruppo A: 2.5±0.53, gruppo B: 4.2±0.75,
gruppo C: 4.3±7.8, gruppo D: 6.4±0.87 (ng/ml); dunque nei gruppi con somministrazione di
Biobran MGN-3, rispetto al gruppo controllo, sono stati osservati valori significativamente
più bassi. Nell’ambito del test della sensibilità a diverse concentrazioni di TDI (0,01-10%)
nei gruppi con somministrazione di Biobran MGN-3 si è verificata una riduzione di 10-100
volte della sensibilità rispetto al gruppo controllo. Inoltre, nei gruppi Biobran MGN-3 sono
state riscontrate quantità assai più basse di eosinofili nel BALF ed anche valori più bassi
nel testi di applicazione TDI. Dall’altro lato, nei valori degli anticorpi ematici, tra i
singoli gruppi non sono state registrate differenze di grossa entità.
In conclusione si constata che la somministrazione del preparato Biobran MGN-3 ha effetti
manifestamente preventivi e mitigatori sui sintomi dell’asma nel modello murino di asma
indotta da diisocianato di toluene (TDI). Lo studio suggerisce anche che Biobran MGN-3 non
ha influenza sulla formazione di anticorpi IgG1 o IgE (indotta da Th2) e che il preparato
funziona come fattore soppressivo contro i mastociti.
Kobayashi H., Endo Y. (Università McMaster, CANADA): Sintesi dell’intervento alla 52°
riunione annuale della Società giapponese degli allergologi, 2002
(b) Azione inibitoria del preparato Biobran MGN-3 sulla progressione della dermatite atopica
nei topi NC
Oggetto dello studio è stata l’analisi dell’azione immuno-regolatoria del preparato Biobran
MGN-3 sui topi NC, nei quali si sviluppa in maniera naturale un livello aumentato di IgE nel
siero e – come reazione alla sensibilizzazione alle ovalbumine (OVA) – insorgono lesioni
cutanee simili a dermatite. Il Biobran MGN-3 è stato somministrato per via orale a cinque
esemplari di topi NC; gli esiti sono stati poi confrontati con il gruppo controllo senza
assunzione di preparato Biobran MGN-3. I topi sono stati successivamente sensibilizzati alle
ovalbumine. Ogni due settimane prima e dopo la sensibilizzazione sono stati prelevati
campioni di sangue. Le quantità di IgE in generale, così come anche di IgE OVA-specifici nel
siero (stabilite con test ELISA) apparivano ben più basse nei topi trattati con Biobran
MGN-3 rispetto al gruppo controllo. Inoltre, negli esemplari di NC senza Biobran MGN-3 si
sono sviluppate lesioni cutanee simili a dermatite atopica, mentre nei topi NC trattati con
Biobran MGN-3 questo tipo di lesione non si è sviluppata in cinque casi su cinque. In
conclusione è stato constatato che Biobran MGN-3 ha un’azione inibitoria sulla progressione
della dermatite atopica nei topi NC.
Nonoyama S. (Università di Medicina e Odontoiatria di Tokyo, GIAPPONE): Sintesi
dell’intervento all’11° riunione del Congresso internazionale degli immunologi, 2001
© Diritti d’autore 2003: Hiroaki Maeda / Daiwa Pharmaceutical
(Si ringrazia per l’autorizzazione a pubblicare il presente articolo sul sito Biobran.org.)
 Alla guida delle ricerche sul
Biobran v’è il Dr. Mamdooh Ghoneum, professore presso la Cattedra di Immunologia
dell’Università di Medicina e Scienze Charles R. Drew, USA. Il Dr. Ghoneum, attualmente
una personalità di caratura internazionale nel campo dell’approccio immunoterapeutico
nella cura del cancro, ha conseguito il dottorato (PhD.) in radioimmunologia presso
l’Università di Tokyo e da allora si dedica proprio al settore dell’immunologia presso
l’Università della California, a Los Angeles. Nel corso degli ultimi 20 anni ha
esaminato diverse sostanze che sono in grado di migliorare il funzionamento del sistema
immunitario. Secondo quanto da egli stesso descritto, Biobran MGN-3 è il composto
immunomodulatore più potente che egli abbia mai testato. I risultati lo hanno
galvanizzato a tal punto che attualmente dedica l’integrità della propria attività
scientifica alla terapia tramite questo tipo di composto.
Alla guida delle ricerche sul
Biobran v’è il Dr. Mamdooh Ghoneum, professore presso la Cattedra di Immunologia
dell’Università di Medicina e Scienze Charles R. Drew, USA. Il Dr. Ghoneum, attualmente
una personalità di caratura internazionale nel campo dell’approccio immunoterapeutico
nella cura del cancro, ha conseguito il dottorato (PhD.) in radioimmunologia presso
l’Università di Tokyo e da allora si dedica proprio al settore dell’immunologia presso
l’Università della California, a Los Angeles. Nel corso degli ultimi 20 anni ha
esaminato diverse sostanze che sono in grado di migliorare il funzionamento del sistema
immunitario. Secondo quanto da egli stesso descritto, Biobran MGN-3 è il composto
immunomodulatore più potente che egli abbia mai testato. I risultati lo hanno
galvanizzato a tal punto che attualmente dedica l’integrità della propria attività
scientifica alla terapia tramite questo tipo di composto.
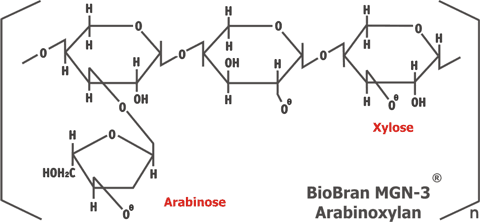



 Fig 5: Percentuale di formazione di legami tra natural killer (cellule
NK) e cellule bersaglio K562. Legenda:% di legami > Prima dell’assunzione > Dopo
l’assunzione
Fig 5: Percentuale di formazione di legami tra natural killer (cellule
NK) e cellule bersaglio K562. Legenda:% di legami > Prima dell’assunzione > Dopo
l’assunzione
 Fig 6: Formazioni letali di cellule NK e cellule tumorali bersaglio.
Fig 6: Formazioni letali di cellule NK e cellule tumorali bersaglio.
 Figure 7: Matsuura M. (Scuola di Medicina di Jichi, GIAPPONE): Rapporto
della Scuola di Medicina di Jichi
Figure 7: Matsuura M. (Scuola di Medicina di Jichi, GIAPPONE): Rapporto
della Scuola di Medicina di Jichi

 Fig. 10 Legenda: profilo ponderale dei topi (v%)
Fig. 10 Legenda: profilo ponderale dei topi (v%)
 Fig. 11
Fig. 11