3. DZIAŁANIE FIZJOLOGIICZNE ARABINOKSYLANOWYCH PRODUKTÓW POCHODZĄCYCH Z OTRĘBÓW RYŻOWYCH (Biobranu)
3.1 Immunoregulacja
(a) Zwiększanie aktywności ludzkich komórek NK z użyciem zmodyfikowanego arabinoksylanu z otrębów ryżowych (Biobran MGN-3)
1. Badania in vitro
Komórki NK szczura hodowano z docelowymi komórkami nowotworowymi K-562 w obecności preparatu Biobran MGN-3, a następnie w teście separacyjnym 51Cr zbadano liczbę rozłożonych komórek K-562. Wzrost stężenia rozłożonych komórek zależał od stężenia preparatu Biobran MGN-3 (25 µg/ml lub 100 µg/ml), co potwierdziło, że wzrost aktywności komórek NK wynika z działania preparatu Biobran MGN-3.
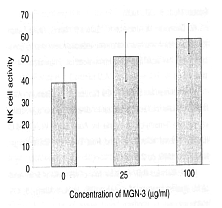
2. Badanie in vivo (na szczurach)
Biobran MGN-3 podawano doustnie szczurom Sprague-Dawley i po dwóch tygodniach zbadano aktywność komórek NK. Szczury podzielono na trzy grupy po 5 osobników, którym podawano dawki w stężeniu 0,5 mg, 5 mg lub 50 mg/kg/dzień. W zależności od stężenia podawanej dawki Biobranu MGN-3 odnotowywano większą aktywność komórek NK. W grupach otrzymujących dawki 0,5 mg, 5 mg i 50 mg odnotowano wzrost tej aktywności odpowiednio o 119%, 130% i 142% w porównaniu z grupą kontrolną. W grupie otrzymującej 50 mg aktywność wzrosła do poziomu 132% w porównaniu z grupą kontrolną już po trzech dniach podawania preparatu. Wzrost aktywności komórek NK dzięki preparatowi Biobran MGN-3 wiązał się z jednej strony z większą siłą niszczenia komórek NK, ale zależał również od ogólnej ich liczby. Zaobserwowano różnicę w działaniu u samców i samic, przy czym u samic działanie było silniejsze (wyk. 3).
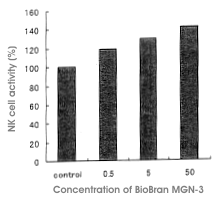
3. Wpływ na ludzi
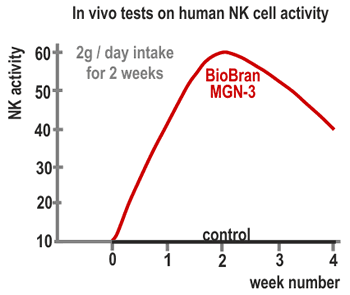
W badaniach wpływu preparatu Biobran MGN-3 na ludzi wzięły udział 24 osoby zdrowe (15 kobiet i 9 mężczyzn, średnia wieku 34 lata), które przyjmowały preparat przez okres 60 dni bez przerwy i u których monitorowano aktywność komórek NK. Uczestników podzielono na 3 grupy po 8 osób i podawano im dawki dzienne 15 mg/kg, 30 mg/kg i 45 mg/kg masy ciała. Każdemu uczestnikowi pobrano próbkę krwi (20 ml) przed pierwszym podaniem preparatu, po tygodniu jego używania, po miesiącu, po dwóch miesiącach (na zakończenie prowadzonego badania) i miesiąc po skończeniu stosowania w celu zbadania aktywności komórek NK. W grupach otrzymujących dawkę 30 mg i 45 mg aktywność komórek NK wzrosła dwukrotnie po tygodniu stosowania i trzykrotnie po dwóch miesiącach stosowania preparatu. W grupie otrzymującej dawkę 15 mg aktywność gwałtownie wzrosła po miesiącu stosowania, zaś po dwóch miesiącach osiągnęła poziom zbliżony do grupy otrzymującej 30 mg i 45 mg. Miesiąc po zakończeniu podawania preparatu aktywność komórek NK wróciła do poziomu sprzed badania (wyk. 4). Takie wyniki sugerują, że dzienna dawka 15 – 45 mg/kg preparatu Biobran MGN-3 ma realny wpływ na aktywność ludzkich komórek NK.
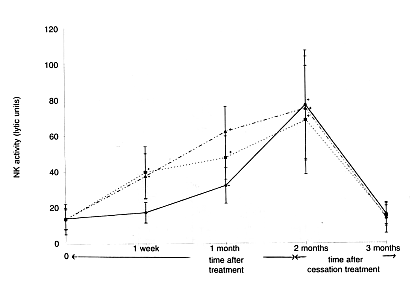
Wykres 4: Zależność od czasu i dawki aktywizacji działania komórek NK przez preparat Biobran MGN-3 w odniesieniu do komórek nowotworowych K562
.._.._.._.._ = 45 mg/kg/dzień;
………… = 30 mg/kg/dzień;
________ = 15 mg/kg/dzień
4. Mechanizm działania preparatu Biobran MGN-3 na komórki NK
Oba badania, in vitro i in vivo, potwierdziły, że liczba ziaren cytotoksycznych w komórkach NK modulowanych preparatem Biobran MGN-3 wzrasta. Badano również zdolność tych komórek do wiązania się z komórkami docelowymi. W teście hodowano komórki NK osoby otrzymującej dawkę 45 mg/kg preparatu Biobran MGN-3 przez okres 30 dni z komórkami docelowymi K-562, a następnie zmierzono ich zdolność do wiązania się na komórkach docelowych. Po wspólnej godzinnej inkubacji w temperaturze 4°C oznaczono 200 komórek NK i obliczono wskaźnik tworzenia powiązań z K-562. U pacjenta, któremu podawano preparat Biobran MGN-3 wskaźnik tworzenia powiązań komórek NK z komórkami docelowymi (K-562) był znacznie wyższy (38,5%) niż przed podaniem preparatu (9,4%). Wyk. 6 przedstawia zdjęcie tych wiązań.
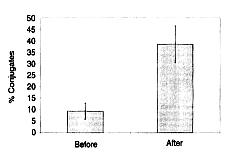 Wykres 5: Procentowy udział tworzenia wiązań przez komórki NK i komórki docelowe K562. Legenda: % wiązań > Przed stosowaniem > Po stosowaniu
Wykres 5: Procentowy udział tworzenia wiązań przez komórki NK i komórki docelowe K562. Legenda: % wiązań > Przed stosowaniem > Po stosowaniu
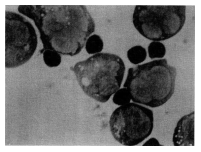 Wykres 6: Śmiertelne formacje komórek NK i docelowych komórek
Wykres 6: Śmiertelne formacje komórek NK i docelowych komórek
Ghoneum M. (Drew Univ., USA):INT. IMMUNO THERAPY XIV (2) PP.89-99, 1998
(b) Wpływ in vitro preparatu Biobran MGN-3 na aktywność komórek z grupy makrofagów
Zbadano działanie preparatu Biobran MGN-3 na komórki z grupy makrofagów, na modulację produkcji mediatorów farmakologicznych, konkretnie zaś mediatorów TNF-A, IL-6 i NO. Makrofagi hodowano z preparatem Biobran MGN-3 w różnych stężeniach (od 1 do 100 µg/ml), a następnie supernatanty badano na obecność wspomnianych mediatorów. TNF-a analizowano według cytotoksyczności względem L929, IL-6 według cytozy B13.19, a NO metodą kolorymetryczną według reakcji z odczynnikiem Griessa. Jako odczynnik kontrolny zastosowano LPS
- i. Mysia linia makrofagów RAW264.7. Po podaniu preparatu Biobran MGN-3 ujawniło się jego silne działanie na trzy wspomniane mediatory już przy stężeniu powyżej 10 µg/ml, tak jak LPS.
- ii. Zastosowanie mysich makrofagów otrzewnowych (C3H/He). Wpływ preparatu Biobran MGN-3 na makrofagi z otrzewnej zdrowej myszy pokazano na wyk. 7. Tu również stwierdzono silne działanie Biobranu MGN-3 w stężeniach powyżej 10 µg/ml.
- iii. Linia makrofagów ludzkich U937. MGN-3 wywołał wzmożoną aktywność, co stwierdzono na podstawie oznaczania poziomu wyprodukowanych cytokin TNF-A i IL-6, ekwiwalentnych do LPS przy stężeniu 100 µg/ml.
Wyniki potwierdzają duży potencjał Biobran MGN-3 do aktywowania zdrowych mysich i ludzkich makrofagów.
Z badań wynika, że aktywne są stężenia powyżej 10 µg/ml.
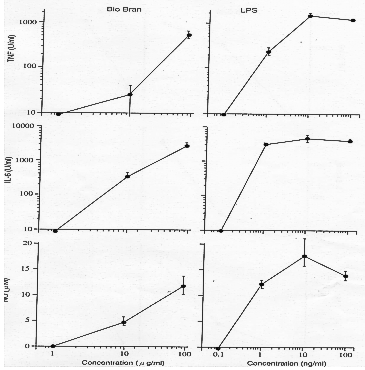 Wykres 7: Mysie makrofagi otrzewnowe (myszy C3H/He) Matsuura M. (Akademia Medyczna Jichi, Japonia) : Raport Akademi Medycznej Jichi
Wykres 7: Mysie makrofagi otrzewnowe (myszy C3H/He) Matsuura M. (Akademia Medyczna Jichi, Japonia) : Raport Akademi Medycznej Jichi
(c) Immunomodulacja a prewencja chorób nowotworowych
W wielu badaniach potwierdzono, że u osób narażonych na działanie różnych substancji chemicznych w miejscu pracy istnieje podwyższone ryzyko chorób nowotworowych. Jedno z tych badań miało na celu zbadanie zmian odporności w związku z działaniem toksycznych substancji chemicznych i potencjału do lepszego tolerowania toksyczności chemicznej dzięki zastosowaniu preparatu Biobran MGN-3.
W badaniu wzięło udział jedenaście osób narażonych na działanie substancji chemicznych w miejscu pracy. Cierpiały one na zaburzenia odporności przejawiające się niskim poziomem aktywności komórek NK (10,2±4,2 LU), blastogenną odpowiedzią limfocytów krwi na mitogeny limfocytów T (PHA, 39060±12517cpm i COMA, 36224±11922cpm) i limfocytów B (PWM, 16550±6330cpm) w porównaniu z odpowiedzią w grupie kontrolnej. Pacjentom przez okres czterech miesięcy podawano 15 mg/kg preparatu Biobran MGN-3 dziennie. Terapia z użyciem preparatu podniosła aktywność komórek NK 4-krotnie po dwóch miesiącach i 7-krotnie po czterech miesiącach, zaś funkcje limfocytów T i B wzrosły odpowiednio o 130% i 150% w porównaniu z wartościami początkowymi.
Ghoneum M. (Ch. R. Drew University, USA): Streszczenie ze zbioru referatów z VII Międzynarodowego Kongresu Technologii Biomedycznych i Hamowania Starzenia, 1999
(d) Wytwarzanie TNF-α i IF-γ w limfocytach ludzkiej krwi obwodowej, modulowane przez zmodyfikowany arabinoksylan z otrębów ryżowych, zawarty w preparacie Biobran MGN-3
Zbadano mechanizm sprawiający, że Biobran MGN-3 podnosi aktywność cytotoksyczną komórek NK. Testowano wpływ preparatu Biobran MGN-3 na intensywność wydzielania czynnika martwicy guza α, (TNF-α) i interferonu-γ (IFN-γ) oraz na ekspresję kluczowych receptorów na powierzchni komórek.
Limfocyty z krwi obwodowej były hodowane z preparatem Biobran MGN-3 w stężeniach 0,1 i 1 mg/ml a następnie roztwory zostały zbadane przy pomocy testu ELISA. Wyniki pokazują, że Biobran MGN-3 to potężny czynnik indukujący TNF-α, zaś jego efekty zależą od podanej dawki. Stężenie Biobranu MGN-3 na poziome 0,1 i 1 mg/ml zwiększyło produkcję TNF-α odpowiednio 22,8- i 47,1-krotnie. Biobran MGN-3 zwiększył również wytwarzanie IFN-γ, choć w niższym stopniu niż w przypadku TNF-α. Jeżeli chodzi o kluczowe powierzchniowe receptory komórkowe, Biobran MGN-3 zwiększył ekspresję antygenu wczesnej aktywacji CD69 po 16 godzinach inkubacji. Ponadto po inkubacji z preparatem Biobran MGN-4 zaobserwowano zwiększenie ekspresji receptora interleukiny 2, CD25 i adhezyny ICAM-1 (CD54). Natomiast inkubacja wysoko oczyszczonych komórek NK z preparatem MGN-3 skutkowała zwiększonym wydzielaniem TNF-α i IFN-γ wraz z poprawą funkcji cytotoksycznych komórek NK. Co więcej, po dodaniu preparatu Biobran MGN-3 do komórek NK aktywowanych interleukiną-2 nastąpiła synergiczna modulacja wydzielania TNF-α i IFN-γ.
Ghoneum M. (Ch. R. Drew University, USA), Jewett A. (UCLA, USA) : Cancer Detection and Prevention (Wykrywanie i profilaktyka chorób nowotworowych) tom 24/numer 4, 2000
(e) Wpływ zmodyfikowanego arabinoksylanu z otrębów ryżowych na aktywność ludzkich komórek NK z krwi obwodowej
Zbadano wpływ preparatu Biobran MGN-3 i jego frakcji molekularnych na aktywność komórek NK. Do ludzkich limfocytów z krwi obwodowej dodano frakcje z wysoką masą cząsteczkową (10 – 50 kDa), otrzymane w filtracji żelowej na złożu Sephadex G-25 i G-75. Po 3 dniach inkubacji zmierzono aktywność komórek NK. Jako komórki docelowe wykorzystano znaczone fluorescencyjnie komórki linii K-562, a aktywność komórek NK została ustalona przy użyciu metody fluorescencyjnej z Tere Scan. Podobne doświadczenie przeprowadzono w obecności IL-2.
W eksperymentach nie wykryto zasadniczych różnic w aktywacji komórek NK przez preparat Biobran MGN-3 lub jego frakcje o wyższej masie cząsteczkowej. Kiedy jednak do pożywki dodano IL-2, w roztworach, w których był oprócz niej obecny również Biobran MGN-3 lub jego frakcja, w porównaniu z roztworem zawierającym tylko IL-2, zaobserwowano większą aktywność NK-komórkową. Sugeruje to, że Biobran MGN-3 aktywuje komórki NK w obecności IL-2 oraz że taka aktywność pojawia się również w przypadku jego frakcji o wyższej masie cząsteczkowej.
Ueda Y., Shimomura C. (Uniwersytet Chiba, JAPONIA): Streszczenie wystąpienia z dorocznego zjazdu Japońskiego Towarzystwa Bionauki, Biotechnologii i Agrochemii, 2002
3.2. Działanie antywirusowe
Działanie antywirusowe preparatu Biobran MGN-3 na HIV in vitro
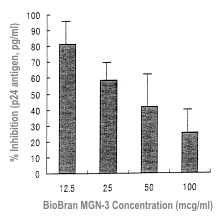
Działanie antywirusowe Biobranu MGN-3 na HIV zostało przebadane in vitro. Najpierw zbadano działanie wstrzymujące produkcję antygenu HIV-1 p24. Jednojądrowe komórki pobrane od trzech zdrowych osób były hodowane ze szczepem HIV-1 SF w temperaturze 37ºC przez godzinę w obecności Biobranu MGN-3. Stężenia Biobranu MGN-3 wynosiły 0-100 μg/ml. Zależnie od stężenia Biobran MGN-3 hamował wytwarzanie antygenu HIV-1 p24 (Wykres 8) i zespólni, a maksymalny stopień tego hamowania utrzymywał się na poziomie 75% dla stężenia 100/ml) (Tabela 1).
 |
|
Tabela 1
| Zahamowanie powstawania zespólni przez preparat Biobran |
| Dawka Biobranu (μg/ml) |
Zespólnie (SF) |
| Liczba SF |
% zahamowania |
0
12.5
25
50
100
|
42.0±8
25.8±7
21.5±5
15.8±4
10.5±3
|
00.0
38.5
50.0
62.5
75.0
|
|
| Figure 8 |
|
|
Ghoneum M. (Ch. R. Drew University, USA): Biochemical and Biophysical Research Communications (Komunikacja między badaniami biochemicznymi i biofizycznymi) 243, (1998)
3.3. Działanie antyrakowe
(a) Badanie wpływu składników zmodyfikowanego arabinoksylanu z otrębów ryżowych na hamowanie rozwoju komórek rakowych różnych linii
Badanie było poświęcone wpływowi zmodyfikowanego arabinoksylanu z otrębów ryżowych, zawartego w preparacie Biobran MGN-3, na hamowanie rozwoju komórek rakowych różnych linii, takich jak HL60, K562 i HLE oraz na zdolność wywoływania różnicowania w HL60 i K562. Do kultury z liniami komórkowymi dodano Biobran MGN-3. Po 3 dniach inkubacji udział komórek, które przeżyły we wszystkich liniach komórkowych obniżył się proporcjonalnie do dodanej ilości preparatu Biobran MGN-3.
Po precypitacji z etanolem, precypitat zmieszano z wodą destylowaną, a otrzymany w ten sposób supernatant poddano frakcjonowaniu z użyciem kolumny Sephadex G-25 na 3 frakcje (A, B, C), które dodano do kultur z liniami komórkowymi. Działanie hamujące wzrost zaobserwowano we frakcji C dla linii HL60 i K562, oraz we frakcji B i C dla linii HLE. Co więcej, w barwieniu metodą Giemsy i esterazą nieswoistą stwierdzono zdolność wywoływania różnicowania u HL60 i K562. Takie wyniki sugerują, że Biobran MGN-3 zawiera składniki mogące hamować rozwój komórek nowotworowych i potencjalnie wywoływać różnicowanie linii HL60 i K562.
Masada M. (Uniwersytet Chiba, JAPONIA): Streszczenie wystąpienia z dorocznego zjazdu Japońskiego Towarzystwa Bionauki, Biotechnologii i Agrochemii 2002
(b) Wpływ preparatu Biobran MGN-3 na rozwój komórek nowotworowych
Zbadano bezpośredni wpływ preparatu Biobran MGN-3 na rozwój komórek raka skóry i wytwarzanie cytokiny. W porównaniu z grupą kontrolną komórek raka kolczystokomórkowego linii komórkowej SCC13, hodowanej na pożywce MEM gdzie następował wzrost liczby komórek, inkubacja komórek tej linii [SCC13] z preparatem Biobran MGN-3 zatrzymała rozwój komórek rakowych (po 48 godzinach zaobserwowano o 30% mniej komórek, a po 72 godzinach o 50% mniej w porównaniu z hodowlą kontrolną).
W analizach metodą cytometrii przepływowej stwierdzono, że po 16 godzinach inkubacji komórek SCC13 z preparatem Biobran MGN-3 nastąpił pięciokrotny wzrost poziomu interleukiny wewnątrzkomórkowej 10 [IL-10], jednak nie nastąpiła żadna wyraźna zmiana zawartości interferonu-γ [INF-γ]. W badaniach pożywki kultywacyjnej ELISA z komórkami SCC13 stwierdzono 8-krotny wzrost poziomu IL-10 i 3-krotny wzrost IL-12. Odnotowano tylko niewielką zmianę stężenia INF-γ. Ponadto zbadano wpływ preparatu Biobran MGN-3 również na inne linie komórkowe, takie jak komórki zdrowe, komórki raka piersi i komórki raka prostaty.
Wyniki sugerują, że Biobran MGN-3 nie tylko wzmacnia odporność organizmu pacjenta, ale również bezpośrednio wpływa na rozwój komórek nowotworowych i produkcję cytokin. Takie wyniki mogą przybliżyć niepoznany dotąd mechanizm działania, który wyjaśniałby znaczne osiągnięcia kliniczne i imponujące korzyści z leczenia preparatem Biobran MGN-3, obserwowane przez autora w ciągu 4 ostatnich lat.
Ghoneum M. (Ch. R. Drew University, USA): Streszczenie ze zbioru referatów z VIII Międzynarodowego Kongresu Technologii Biomedycznych i Hamowania Starzenia, 2000
3.4. Efekt komplementarny w leczeniu chorób nowotworowych
(a) Analiza związku między aktywnością komórek NK a wskaźnikiem przeżywalności u pacjentów z różnymi typami nowotworu po zastosowaniu multi-immunologicznych protokołów terapeutycznych
Niniejsze badanie miało na celu stwierdzenie, czy podawanie preparatu Biobran MGN-3 może wpływać na przedłużanie i poprawienie jakości życia na próbce 205 pacjentów onkologicznych po operacji z nowotworem postępującym i częściowymi przerzutami późnego stopnia III – IV. W badaniu klinicznym wzięli udział pacjenci hospitalizowani w klinice chirurgicznej Sano w Japonii. Leczono ich uzupełniającymi środkami alternatywnymi i konwencjonalnymi lekami na choroby nowotworowe z niewielkimi skutkami ubocznymi.
205 pacjentów hospitalizowanych przez okres 6 miesięcy podzielono na dwie grupy: 109 pacjentów z grupy kontrolnej leczono z zastosowaniem standardowej uzupełniającej klinicznej terapii alternatywnej, natomiast 96 pacjentom podawano dodatkowo przez półtora roku preparat Biobran MGN-3.
U wszystkich pacjentów badano aktywność komórek NK jako wskaźnik zmian parametrów odpornościowych. U wszystkich pacjentów monitorowano również jakość życia. Aktywność komórek NK u pacjentów po operacji była zazwyczaj niska, jednak u pacjentów przyjmujących Biobran MGN-3 stwierdzono wyższy stopień apotanazji (większa przeżywalność), przy czym efekt ten był tym silniejszy, im wyższa była u tych pacjentów aktywność komórek NK (Tabela 2). Wyniki te sugerują, że poziom aktywności komórek NK w przypadku postępujących typów choroby nowotworowej można uznać za wskaźnik patologiczny. W grupie otrzymującej dodatkowo Biobran MGN-3 zaobserwowano również poprawę jakości życia.
Tabela 2: Zależność między całkowitym wskaźnikiem przeżywalności a aktywnością komórek NK w 2 analizowanych grupach
| Grupa |
Grupa Biobran |
Grupa kontrolna |
| Całkowity wskaźnik przeżywalności |
52/96 (54.2%) |
19/63 (33.9%) |
Kategorie według aktywności komórek NK
Poniżej 19.9%
20%-40%
Ponad 40%
|
17/40 (42.5%)**
18/35 (51.4%)*
17/21 (81.0%)
|
2/16 (12.5%)
7/25 (28.0%)
10/15 (66.7%)
|
% istotności na tle grupy kontrolnej **p<0.01 *p<0.05
Takahara K. (Klinika Chirurgii w Sano, JAPONIA) : Streszczenie referatu z III Dorocznego Zjazdu Japońskiego Towarzystwa Medycyny i Terapii Komplementarnej i Alternatywnej, 2000
(b) Działanie immunomodulacyjne i antynowotworowe preparatu Biobran MGN-3 u 5 pacjentek z nowotworem piersi
Pięciu pacjentkom z nowotworem piersi podawano preparat Biobran MGN-3 w dawce 3 g/dziennie, a następnie w teście separacyjnym 51Cr oznaczono aktywność komórkową NK na docelowych komórkach nowotworowych linii K562. Wyniki były następujące:
-
Dla niskiego poziomu aktywności komórek NK (12,7 – 58,3%) i stosunku efektor : cel 12 i 100:1, aktywność komórek NK u pacjentek leczonych z użyciem preparatu Biobran MGN-3 istotnie wzrosła (41,8 – 89,5%), zaś stosunek efektor : cel został utrzymany.
-
Wzrost aktywności komórek NK zaobserwowano już po 1-2 tygodniach od podjęcia leczenia, zaś w przypadku dalszego podawania preparatu Biobran MGN-3 aktywność ta nadal rosła.
-
U dwóch pacjentek uczestniczących w badaniu od samego początku nastąpiła całkowita remisja (pacjentki leczone przez 6-8 miesięcy).
Ghoneum M. (Ch. R. Drew University, USA): Materiały z nadzwyczajnej konferencji Amerykańskiego Stowarzyszenia Badań nad Nowotworami, 1995
(c) Działanie immunomodulacyjne zmodyfikowanego arabinoksylanu z otrębów ryżowych, zawartego w preparacie Biobran MGN-3, na komórki NK w grupie 27 pacjentów onkologicznych
Badano działanie immunomodulacyjne preparatu Biobran MGN-3 u 27 pacjentów onkologicznych. Pacjenci chorowali na różne typy zaawansowanych nowotworów: 7 pacjentek miało raka piersi, 7 – prostaty, 8 – szpiczaka mnogiego, 3 – białaczkę i 2 – raka szyjki macicy. Wszyscy pacjenci byli leczeni w sposób konwencjonalny a uzupełniająco podawano im preparat Biobran MGN-3 w dawce 3 mg/dziennie, po czym zbadano aktywność komórek NK po 2 tygodniach, 3 miesiącach i 6 miesiącach. Aktywność komórek NK mierzono w teście separacyjnym 51Cr, jako docelowe komórki zastosowano komórki nowotworowe linii K562, a relacja efektor : cel wynosiła od 12:1 do 100:1. Wyniki sugerują co następuje:
-
Wyjściowa aktywność komórek NK u pacjentów była niska.
-
Leczenie z użyciem preparatu Biobran MGN-3 spowodowało znaczny wzrost aktywności komórek NK już po 2 tygodniach. Pobudzenie aktywności dla poszczególnych typów nowotworu wyrażone procentowo było następujące: rak piersi 154-332%, prostaty 174-385%, białaczka 100-240%, szpiczak mnogi 100-537% i rak szyjki macicy 100-275%.
-
Aktywność komórek NK rosła w sposób ciągły również po 3 i 6 miesiącach leczenia.
Ghoneum M. (Ch. R. Drew University, USA): Streszczenie referatu z 87. Dorocznego Zjazdu Amerykańskiego Stowarzyszenia Badań nad Nowotworami, 1996
(d) Przypadek terapii komplementarnej raka płuc z przerzutami z użyciem preparatu Biobran MGN-3
Niniejszy artykuł prezentuje przypadek, w którym osiągnięto pozytywne wyniki po zastosowaniu terapii komplementarnej z użyciem preparatu Biobran MGN-3 u pacjenta z przerzutowym rakiem płuc, który zaatakował znaczną część kości.
Pacjentem był 67-letni mężczyzna. W sierpniu 1996 roku zgłosił się do lekarza z powodu drastycznego spadku masy ciała, uciążliwego kaszlu i odkrztuszania. Zdiagnozowano raka płuc (rak płaskonabłonkowy) z powikłaniami w postaci gruźlicy (M. tuberculosis). Terapię zaczęto od leczenia antybiotykowego gruźlicy, po czym w październiku podjęto również naświetlania nowotworu. W grudniu tego samego roku pacjentowi usunięto operacyjnie dolną połowę prawego płuca z nowotworem. Pacjenta po radioterapii wypisano ze szpitala w styczniu 1997 roku.
W czerwcu tego samego roku pacjent ponownie zjawił się u lekarza, uskarżając się na bóle po prawej stronie klatki piersiowej. W badaniu scyntygraficznym kości potwierdzono liczne przerzuty do kości. Nowotwór rozprzestrzenił się przede wszystkim prawostronnie na żebrach, ale był też rozsiany w tkance kostnej praktycznie w całym organizmie. W lipcu rozpoczęto leczenie analgetyczne z użyciem morfiny o przedłużonym uwalnianiu. Jednocześnie od końca maja podjęto leczenie z użyciem preparatu Biobran MGN-3 w dawce 3 g dziennie. Od stycznia 1998 roku bóle zaczęły ustępować. Pacjentowi nadal podawano Biobran MGN-3, stopniowo redukując dawki morfiny o przedłużonym uwalnianiu, którą ostatecznie w lipcu całkowicie odstawiono. Marker rakowy ICPP w momencie potwierdzenia nawrotu choroby wynosił 16,8 ng/ml i stopniowo obniżył się do 7,6 ng/ml w grudniu 1997 roku i 6,7 ng/ml w lipcu 1998 roku. W scyntygrafii kości stwierdzono wyraźną poprawę i potwierdzono, że nowotwór przestaje się rozprzestrzeniać w kościach. Aktywność komórkowa NK w momencie nawrotu choroby wynosiła 9,0%, jednak stopniowo zaczęła rosnąć i obecnie utrzymuje się na wysokim poziomie.
Sobajima T. (Szpital Hoshigaoka Kosei Nenkin, JAPONIA): Streszczenie referatu z II dorocznego zjazdu Japońskiego Towarzystwa Medycyny i Terapii Komplementarnej i Alternatywnej, 1999
(e) Stosowanie preparatu Biobran MGN-3 w terapii po leczeniu konwencjonalnym
Leczenie nowotworów uśpionych to coraz częściej główna koncepcja terapeutyczna w podejściu do raka w Japonii. Tego typu terapia ma przede wszystkim na celu przedłużenie życia pacjenta, przy jednoczesnym zachowaniu jego wysokiej jakości. Lek. med. Tunekawa przepisuje ją pacjentom na życzenie, przy czym poprawę jakości życia uważa za ważny cel terapeutyczny. W raporcie pisze, iż u swoich trzydziestu czterech pacjentów onkologicznych stosuje na uśpiony nowotwór kombinację chemioterapii oraz terapii komplementarnej i alternatywnej, opisując schemat terapeutyczny trzech z nich:
-
Pacjenci (choroba główna): 3 z rakiem żołądka, 3 z rakiem płuc, 2 z chłoniakiem złośliwym, 6 z rakiem jelita grubego (odcinka odbytniczego), 3 z rakiem piersi i 17 z innymi rodzajami nowotworu
-
Okres leczenia: 6-18 miesięcy
-
Studium przypadku
-
iv. T.S. (60), kobieta, rak żołądka (stopień IV), nowotworowe zapalenie otrzewnej: W styczniu 2000 roku pacjentce usunięto operacyjnie raka włóknistego żołądka. W lutym 2000 roku u pacjentki wystąpiło nowotworowe zapalenie otrzewnej i przy IV stopniu choroby została poddana gastrektomii. CA19-9 wynosił 108. W sierpniu 2000 roku przybyła do naszej kliniki, uskarżając się na bóle brzucha, zaparcia, anemię i anoreksję. Wskaźnik CA19-9 wynosił 390, a aktywność komórek NK – 25,6. Pacjentce przepisano chemoterapię (TS1) w połączeniu z terapią holistyczną. W celu wzmocnienia odporności podawano jej Biobran MGN-3 w dawce 3 g dziennie. Miesiąc później wartość wskaźnika CA19-9 była na poziomie 63. Wartości markerów nowotworowych stopniowo spadały, zaś aktywność komórek NK rosła. W sierpniu 2001 roku, 11 miesięcy później, wartość CA19-9 wynosiła 25, a aktywność komórek NK – 51,5. Obecnie u pacjentki nie występują praktycznie żadne subiektywne objawy i jest dobrze odżywiona.
-
v. F.A. (46), kobieta, rak piersi z przerzutami do kręgów lędźwiowych i macicy: W lipcu 1998 roku pacjentka przeszła operację raka piersi, podjęto leczenie hormonalne i przeciwnowotworowe. W marcu 2001 roku wykryto przerzuty w kręgach lędźwiowych, w kwietniu również w macicy, dlatego w maju 2001 roku pacjentka poddała się histerektomii macicy. Wypisano ją do domu i przepisano Taxol i Paraplatin. W lipcu 2001 roku trafiła do lek.med. Tunekawy, skarżąc się na bóle kości. Jej poziom CA 153, NCC-ST wynosił wówczas 439, a aktywność komórek NK – 9,3. Pacjentce zalecono kontynuowanie leczenia Paraplatinem i podjęcie terapii holistycznej. W celu podniesienia odporności podano preparat Biobran MGN-3 w dawce 3 g dziennie. Dwa miesiące później markery CA wynosiły już tylko 18, NCC-ST 28,9, a aktywność komórek NK – 22,0. Bóle ustąpiły. Następnie u pacjentki stwierdzono stabilny spadek poziomu markerów nowotworowych i wzrost aktywności komórek NK. W lipcu 2002 roku CA było na poziomie 14, NCC-ST 3,2, aktywność komórek NK wynosiła 59, bóle całkowicie ustąpiły, zaś wyniki scyntygrafii kostnej były mniej wyraźne. Obecnie pacjentka jest dobrze odżywiona i cieszy się, że może znów grać na bębnach.
Tunekawa H. (Tokijskie Towarzystwo Promocji Medycyny Holistycznej, JAPONIA): Streszczenie referatu z warsztatów na temat preparatu Biobran w Berlinie, 2002
(f) Ocena działania preparatu Biobran MGN-3 w leczeniu raka w postępującym stadium
Lek.med. Mizukami ma doświadczenie w podawaniu preparatu Biobran MGN-3 grupie 97 pacjentów onkologicznych z różnymi typami nowotworu w fazie postępującej. W grupie znaleźli się pacjenci z rakiem żołądka, jelita grubego, piersi, płuc, trzustki, wątroby, przewodów żółciowych, gardła, jajników, szyjki macicy, macicy, nerek, tarczycy, prostaty, jamy ustnej, szpiczakiem mnogim, itp. Choć pacjenci już przeszli operacje, chemioterapię, radioterapię itp. w dużych szpitalach, u większości nie przyniosło to najlepszych rezultatów. Ze względu na przerzuty i nawroty postanowili skorzystać z usług kliniki lek. med. Mizukamiego i wypróbować immunoterapię. Praktycznie żaden z pacjentów, którym przepisano Biobran MGN-3, nie był już poddawany chemioterapii ani naświetlaniom. Następnie na podstawie obserwacji klinicznych i kwestionariuszy szczegółowo zbadano jakość życia pacjentów. U wszystkich pacjentów stosujących Biobran MGN-3 zaobserwowano jedno wspólne zjawisko.
W kilku przypadkach jakość życia wyraźnie poprawiła się wraz z podaniem preparatu Biobran MGN-3. I choć generalnie jakość życia u pacjentów z rakiem w fazie zaawansowanej wraz z upływem czasu raczej systematycznie spada, u pacjentów, którzy przyjmowali Biobran MGN-3 tendencja ta była mniejsza, a nawet zmieniła się w tendencję do dłuższego przeżycia z dobrą jakością życia, a nawet odnotowano przypadki długiego przeżycia.
Obserwacje dotyczące jakości życia:
-
Choć niełatwo kontrolować intensywny ból, a u pacjentów z rakiem w zaawansowanej fazie często jedyne wyjście stanowi morfina, niektórzy z pacjentów przyjmujących Biobran MGN-3 nie potrzebowali morfiny, a część z tych, którzy ją brali, miała tendencję do przyjmowania coraz niższych dawek.
-
Zaobserwowano ogólnie mniejszą tendencję do odczuwania osłabienia.
-
Zaobserwowano mniejszą tendencję do utraty apetytu.
-
Pojawiła się możliwość pozostania pacjentów w domu i relatywnie dobrego samopoczucia przed śmiercią.
-
Część pacjentów zachowała jasność umysłu przed śmiercią i była w stanie komunikować się z rodziną.
Lek.med. Mizukami podsumował swoje obserwacje stwierdzeniem, że dla pacjentów z rakiem w późnym stadium istotny jest fakt, że przyjmowany preparat Biobran MGN-3 sprawia, że jakość życia nie pogarsza się tak szybko, co wydaje się ważnym aspektem na przyszłość oraz dla podejścia medycznego w leczeniu raka.
Mizukami O. (Instytut Badań na rzecz Wspierania Zdrowia i Fundacja Laymana New Life, JAPONIA): Streszczenie referatu z warsztatów na temat preparatu Biobran w Berlinie, 2002
3.5. Wpływ na apoptozę
Biobran MGN-3 uwrażliwia komórki ludzkiej białaczki limfocytów T na apoptozę wywoływaną przez receptor śmierci (CD95)
Zbadano wpływ preparatu Biobran MGN-3 na apoptozę wywoływaną przez receptor śmierci w komórkach ludzkiej białaczki z linii HUT 78. Komórki HUT 78 najpierw poddano działaniu preparatu Biobran MGN-3, a następnie inkubowano je z agonistycznym przeciwciałem receptora śmierci (Fas, CD95). Stopień apoptozy określono w cytometrii przepływowej FACScan z zastosowaniem jodku propidyny. W cytometrii przepływowej stwierdzono aktywację kaspazy 3, kaspazy 8 i kaspazy 9. Potencjał błony mitochondrialnej zmierzono w FACScan z użyciem barwnika DIOC6. W cytometrii przepływowej zbadano ekspresję CD95 i BCI-2.
Wyniki sugerują, że Biobran MGN-3 w zależności od podanej dawki zwiększa stopień apoptozy wywoływanej przez anty-CD95. Większy stopień umieralności komórek korelował ze wzrostem depolaryzacji potencjału błony mitochondrialnej i z większą aktywizacją kaspazy 3, kaspazy 8 i kaspazy 9. Leczenie z użyciem preparatu Biobran-3 nie miało żadnego wpływu na poziom ekspresji CD95, jednak powodowało ograniczenie ekspresji BCI-2. Takie wyniki sugerują, że Biobran MGN-3 zwiększa skłonność komórek raka do apoptozy wywoływanej przez ligandy śmierci, co może być istotnym faktem w walce z rakiem.
Ghoneum M. (Ch. R. Drew University, USA): Cancer Letter (Magazyn Onkologiczny), 2003
3.6. Aktywacja obrony witalnej
(a) Aktywny wpływ preparatu Biobran MGN-3 na eliminację rodników tlenowych
Raport omawia badania nad oczyszczającym wpływem preparatu Biobran MGN-3 i jego frakcji na rodniki tlenowe. Biobran MGN-3 poddano frakcjonowaniu w kolumnie Sephadex G-25. Poszczególne frakcje oznaczono w zależności od rozmiaru literą L, M i S: L (masa cząsteczkowa > 10 000), M (masa cząsteczkowa od 10 000 do 3 000) i S (masa cząsteczkowa < 3 000).
Działanie eliminujące aktywnych enzymów oceniano przez pomiar działania eliminującego na anionorodnik ponadtlenkowy (•O2), działania eliminującego na rodnik hydroksylowy pochodzący z reakcji Fentona (•OH) i działania eliminacyjnego na rodnik hydroksylowy, uzyskany przez napromieniowanie ultrafioletowe.
Wyniki pomiarów przedstawiono w poniższej tabeli. Frakcja preparatu Biobran oznakowana jako S (z najniższą masą cząsteczkową) najlepiej hamowała powstawanie rodnika hydroksylowego •OH generowanego przez •O2 i promieniowanie ultrafioletowe. W eliminacji hydroksylu (•OH) wygenerowanego w reakcji Fentona wysoką efektywność wykazały wszystkie frakcje preparatu (Tabela 3).
Tabela 3
Działanie eliminacyjne preparatu Biobran MGN-3 na aktywne rodniki tlenowe (•O2 i •OH i •OH wywoływane przez UV)
| Typ aktywnego tlenu i działanie SOD
|
Stopień eliminacji anionorodnika ponadtlenkowego (%) |
Działanie SOD (dysmutazy ponadtlenkowej) (U/ml) |
Stopień eliminacji rodnika hydroksylowanego generowanego przez UV (%) |
| 20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
BioB
BioB-L
BioB-M
BioB-S
|
64.6
39.9
49.5
90.4
|
23.0
10.4
15.6
68.1
|
4.4
0
0
26.4
|
7.6
5.0
7.2
70.5
|
0.9
0.8
1.4
15.7
|
0
0
0
2.6
|
94.9
(72.6)
97.2
(41.8)
97.0
(45.4)
96.5
(71.0
|
78.9
(35.9)
34.4
(16.5)
68.4
(9.9)
55.1
(54.9)
|
3.3
(11.5)
3.3
(1.0)
8.7
(3.9)
4.2
(19.6)
|
·O2:w reakcji HPX-XOD,·OH: w reakcji Fentona
·OH generowane w reakcji UV:365nm,4×103J/m2/min×5
Tazawa K. (Akademia Medycyny i Farmacji w Toyama , JAPONIA) : Biotherapy (Bioterapia) ZESZYT 14, 2000
(b) Podstawowe badania wpływu związku arabinoksylanowego (Biobran MGN-3) na aktywację obrony witalnej
W badaniach doświadczalnych na zwierzętach obserwowano wpływ preparatu Biobran MGN-3 i jego działanie biofilaktyczne na wskaźnik przeżywalności po wywołaniu śmiertelnej sepsy przez lipopolisacharydy.
Eksperyment przeprowadzono na myszach BALB/c (samce w wieku 5-7 tygodni). Myszom z badanej grupy podawano doustnie przez sondę raz na dwa dni przez dwa tygodnie, czyli w sumie siedem razy, 20 mg/kg lub 200 mg/kg preparatu Biobran MGN-3, rozpuszczonego w 0,5 ml buforowanego roztworu soli (PBS). Myszom z grupy kontrolnej podawano z identyczną częstotliwością doustnie 0,5 PBS. 12 godzin po ostatniej dawce doustnej każdemu osobnikowi podano dootrzewnowo 200 µg LPS i obserwowano stan poszczególnych myszy. W kolejnym doświadczeniu myszom z obu grup, z grupy Biobran i z grupy kontrolnej, wprowadzono do organizmu dootrzewnowo 100 µg LPS; następnie myszy uśmiercono w interwałach 0, 2, 4 i 8 godzin po podaniu LPS i pobrano im krew obwodową z serca. Po odseparowaniu surowicy oznaczono poziom IL-6 i TNF. Aktywność IL-6 mierzono z zastosowaniem komórek linii B9, a aktywność TNF w teście biologicznym na komórkach linii WEHI164-13.
Jak widać na Wyk. 9, po podaniu 200 µg LPS wskaźnik przeżywalności w porównaniu z grupą kontrolną był znacznie lepszy tam, gdzie myszom podawano 20 mg/kg i 200 mg/kg preparatu Biobran MGN-3 (grupa Biobran MGN-3 20 mg/kg versus grupa kontrolna, p = 0,0456; grupa Biobran MGN-3 200 mg/kg versus grupa kontrolna, p = 0,0232, analiza w teście Mantela-Coxa). Po podaniu 100 µg LPS na osobnika w grupach, w których wcześniej podawano codziennie Biobran MGN-3 w dawkach 20 mg/kg i 200 mg/kg przeżyły wszystkie myszy, zaś w grupie kontrolnej – 3 z 10 osobników zmarły.
Poszukując odpowiedzi na pytanie, jaki mechanizm przyczynia się do podniesienia wskaźnika przeżywalności w grupie Biobran MGN-3, oznaczono stężenie IL-6 i TNF. W grupie, której podawano Biobran MGN-3, stężenie IL-6 we krwi po dwóch godzinach od podania LPS było znacznie niższe niż w grupie kontrolnej (grupa kontrolna 702,9 ± 24,7 ng/ml, grupa Biobran MGN-3 403,1 ± 59,6 ng/ml; p < 0,01), jednak po 8 godzinach od podania znacznie wzrosło (grupa kontrolna 88,5 ± 50,0 ng/ml, grupa Biobran MGN-3 441,0 ± 115,0 ng/ml; p < 0,05). Stężenie TNF we krwi 4 godziny po podaniu LPS w grupie Biobran MGN-3 znacznie wzrosło w porównaniu z grupą kontrolną (grupa kontrolna 492 ± 187, grupa Biobran MGN-3 1816 ± 307 pg/ml; p < 0,01).
W modelu doświadczalnym ze śmiertelną sepsą wywołaną przez LPS zakładano, że znaczna liczba cytokin prozapalnych (IL-1, 6, TNF-α) uwolnionych z komórek siateczkowo-śródbłonkowych do całego organizmu wywołuje zapaść wielu organów, prowadząc do śmierci. Jednak w niniejszym badaniu w grupie otrzymującej preparat Biobran MGN-3 zaobserwowano znaczny wzrost wskaźnika przeżywalności. Być może wynika to z tego, że podawanie preparatu Biobran MGN-3 hamuje wytwarzanie histotoksycznych cytokin, wydzielanych przez makrofagi, lub z tego, że Biobran MGN-3 blokuje drogę do histotoksyczności na poziomie komórek docelowych.
Sudo N., Kubo C. (Uniwersytet w Kiusiu, JAPONIA): The Japanese Journal of Clinical and Experimental Medicine (Japoński Magazyn Medycyny Klinicznej i Eksperymentalnej), Numer 78, 1, 2001
(c) Ograniczenie spadku masy ciała u myszy po podaniu cisplatyny dzięki preparatowi Biobran MGN-3
W leczeniu chorób nowotworowych leki zawierające platynę często wywołują poważne skutki uboczne, takie jak nudności, wymioty, nefropatia i niedobór magnezu we krwi z powodu uszkodzeń kanalików nerkowych (Lajer & Dangaard, 1999), dochodzi również do utraty słuchu, neuropatii obwodowej i zahamowania czynności szpiku, należącego do najbardziej dewastujących organizm skutków ubocznych (Prestayko z zespołem, 1979), prowadzących do osłabienia odporności. Dlatego każde ograniczenie skutków ubocznych cisplatyny jest niezwykle cenne i pożądane. W naszych badaniach zbadaliśmy wpływ preparatu Biobran MGN-3 na ograniczanie spadku masy ciała u myszy, którym podawano maksymalną tolerowaną dawkę cisplatyny.
Tydzień przed podaniem cisplatyny dwóm grupom myszy zaczęliśmy podawać preparat Biobran MGN-3 w dawkach 10 mg/ml (suchej masy) w wodzie lub w dootrzewnowych zastrzykach o obj. 0,1 ml, gdzie równoważna dawka preparatu została rozpuszczona w buforowanej soli izotonicznej (PBS). Dawkę 1 mg na osobnika obliczono według zalecanej dawki dla człowieka (50 mg/kg). Cisplatynę w ilości 15 mg/kg podano dootrzewnowo w 0,1 ml buforowanego roztworu soli (PBS) z 0,5% dimetylosulfotlenku (DMSO) w funkcji podłoża. Dwie grupy myszy dostały przez sondę wodę lub dootrzewnowo PBS, a po tygodniu podano obu grupom cisplatynę.
Spadek masy ciała odnotowano już następnego dnia po podaniu dootrzewnowego zastrzyku cisplatyny w obu grupach, w grupie z preparatem Biobran MGN-3 i bez niego. Największy spadek stwierdzono piątego dnia po podaniu cisplatyny, również w obu grupach, z preparatem Biobran i bez niego, oraz bez względu na sposób podania (doustny lub dootrzewnowy). Największy spadek masy ciała zaobserwowano u myszy, którym podano cisplatynę bez preparatu Biobran MGN-3. Choć spadek masy ciała u myszy, którym podawano Biobran MGN-3 zbliżał się do 20 procent zaobserwowanych u myszy z grup, którym podano cisplatynę bez Biobranu MGN-3, trzeba zaznaczyć, że w tej grupie nie zdechła żadna mysz, żadna również nie miała biegunki ani krwi w stolcu, czyli skutków ubocznych zazwyczaj towarzyszących przyjmowaniu cisplatyny. W fazie rekonwalescencji w porównaniu z grupami, którym nie podawano Biobranu MGN-3, myszy z grup z preparatem Biobran szybciej przybierały na wadze.
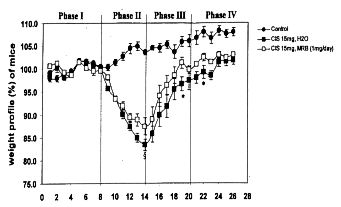
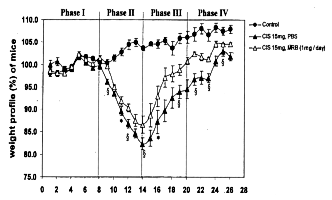
Endo Y., Kanbayashi H. (Mac Master University, KANADA): Pharmacology and Toxicology (Farmakologia i toksykologia), 2003
(d) Wpływ preparatu Biobran MGN-3 na toksyczność wywołaną przez cisplatynę i adriamycynę u szczurów
Biobran MGN-3 to produkt pochodzący z otrębów ryżowych, otrzymywany w procesie częściowej hydrolizy frakcji błonnika rozpuszczalnych w wodzie przez karbohydrazy z grzyba lentinus edodes [nr patentu w USA 5560914]. Udowodniono, że Biobran MGN-3 jest modyfikatorem odpowiedzi biologicznej, wywołującym u pacjentów z osłabioną odpornością wzrost aktywności komórek NK [Int. J. Immunother. 14 (1) 1998].
Cel: Zapobieżenie poważnym zmianom patologicznym i spadkowi masy w związku z podaniem jednej dawki cisplatyny (CIS) lub adriamycyny (ADR) przez codzienne podawanie preparatu Biobran MGN-3 w ilości 5 lub 50 mg/kg. Po 13-dniowej aklimatyzacji do testu wybrano według masy ciała samce szczurów z linii Spaque-Dawley, które podzielono na osiem grup po 10 osobników (dawki podano w mg/ml):
-
1. Biobran 5 mg p.o. + podłoże dootrzewnowo
-
2. Biobran 50 mg p.o. + podłoże dootrzewnowo
-
3. Grupa kontrolna p.o. + CIS 8 mg dootrzewnowo
-
4. Biobran 5 mg p.o. + CIS 8 mg dootrzewnowo
-
5. Biobran 50 mg p.o. + CIS 8 mg dootrzewnowo
-
6. Grupa kontrolna p.o. + ADR 10 mg dootrzewnowo
-
7. Biobran 5 mg p.o. + ADR 10 mg dootrzewnowo
-
8. Biobran 50 mg p.o. + ADR 10 mg dootrzewnowo
Szczurom podawano doustnie preparat Biobran MGN-3 (rozpuszczony w wodzie destylowanej) lub podłoże (podłoże leku bez substancji czynnej) codziennie przez okres 11 dni. Chemoterapeutyk lub podłoże podano każdemu z testowanych osobników w jednej dawce, wstrzykniętej dootrzewnowo trzeciego dnia. Przez wszystkie 11 dni u codziennie monitorowano objawy kliniczne u szczurów. Co drugi dzień badano masę ciała. Jedenastego dnia zwierzęta uśpiono przez inhalację CO2 i wykonano sekcję zwłok. Skontrolowano wizualnie główne organy i zbadano uszkodzenia przewodu żołądkowo-jelitowego.
Wyniki: Między 7 i 11 dniem zmarło pięć szczurów z grupy 3, trzy z grupy 5 i jeden z grupy 4. Szczury, którym podawano doustnie wyłącznie Biobran MGN-3 w ilości 5 lub 50 mg/kg wykazywały statystycznie istotny przyrost masy ciała (+72%). Szczury przyjmujące wyłącznie CIS lub ADR miały niewielki przyrost masy ciała (-1,5% dla CIS i +30% dla ADR). Szczury otrzymujące Biobran MGN-3 w ilości 5 lub 50 mg plus CIS lub ADR wykazywały znacznie większy przyrost masy ciała niż szczury z czysto chemoterapeutycznej grupy (+11% w grupie Biobran MGN-3 5 mg + CIS i +46% w grupie + ADR). W grupie Biobran MGN-3 50 mg + CIS odnotowano przyrost masy ciała na poziomie +44%, zaś w grupie Biobran MGN-3 50 mg + ADR +43%. Szczury, które przeżyły, a którym podawano Biobran MGN-3 w porównaniu ze szczurami przyjmującymi wyłącznie CIS lub ADR bez preparatu Biobran MGN-3, wyglądały na zdrowsze i przybierały na wadze, zaobserwowano u nich również rzadsze występowanie poważnych patologii jelitowych.
Tabela 4: Wpływ preparatu Biobran na spadek masy ciała wywołany przez podawanie cisplatyny i doksorubicyny
| Terapia (wszystko dootrzewnowo) |
Dzień 0 |
Dzień 3 |
Dzień 5 |
Dzień 7 |
Dzień 9 |
Dzień 11 |
5mg/kg p.o. + podłoże
50mg/kg p.o. +podłoże
Grupa kontrolna p.o.+ Cp8mg/kg
5mg/kg p.o. + Cp8mg/kg
50mg/kg p.o. + Cp8mg/kg
Grupa kontrolna p.o. + Dx10mg/kg
5mgn/kg p.o. + Dx10mg/kg
50mg/kg p.o. + Dx10mg/kg
|
100
100
103
99
101
103
101
101
|
100
98
101
99
99
100
100
101
|
100
100
82
85
92
88
92
92
|
100
97
69
76
90
82
89
87
|
100
97
55
68
85
77
86
85
|
100
97
57
65
84
76
85
83 |
p.o.- doustnie, Dx-doksorubicyna, Cp-cisplatyna
Jacoby H. I. (USA) : Journal of Nuturaceuticals, Function & Medical Foods (Magazyn Żywienia Terapeutycznego, Żywności Funkcjonalnej i Medycznej), Numer 3 (4) 2001
(e) Wpływ preparatu Biobran MGN-3 na toksyczność wywołaną przez radioterapię u myszy
Badanie miało na celu analizę wpływu modyfikowanego preparatu Biobran MGN-3 na promienioczułość przejawiającą się ubywaniem szpiku kostnego wskutek pełnego naświetlania organizmu. Aby uwzględnić ewentualne zastosowanie kliniczne autorzy przetestowali działanie metodą ilościową dla całego spektrum dawek naświetlań od 4,5 do 8,5 Gy.
Doświadczenie przeprowadzono na cztero- i pięciotygodniowych samcach myszy z linii SPF BALB/c (grupa F2). W wybranych grupach zwierzętom dodano do pokarmu preparat MGN-3 w ilości 50 mg/kg masy ciała. Grupy składały się z 10-50 osobników. Po dwóch dniach aklimatyzacji myszom z badanej grupy (F2) dodano do pożywienia Biobran MGN-3. Po 8 i 15 dniach podawania preparatu Biobran MGN-3 osobnicy zostali poddani naświetlaniom. Następnie 3 razy w tygodniu badano ich masę ciała oraz codzienne sprawdzano odsetek padłych zwierząt. W niektórych przypadkach w doświadczeniu podawano myszom Biobran MGN-3 przez całe dwa tygodnie przed naświetlaniem, w innych zaczęto go podawać dopiero po naświetlaniu.
Choć w grupie F2 zgony myszy wskutek ubytku szpiku kostnego zaobserwowano już od siódmego dnia po naświetlaniu, myszy z grup, którym podawano Biobran MGN-3 ginęły wskutek naświetlań nieco później. Dawka LD50 (powodująca śmierć co najmniej połowy naświetlonych zwierząt) wynosiła około 5,15 Gy, zaś DRF (czynnik redukcji dawki) wynosił około 1,14. Jeżeli chodzi o masę ciała, w grupach Biobran MGN-3 zaobserwowano tendencję do utrzymywania wyższej masy ciała. Efekt późniejszego rozpoczęcia podawania preparatu Biobran MGN-3 sugeruje, że stosowanie preparatu jeszcze przed rozpoczęciem naświetlania daje lepsze rezultaty.
Dawka naświetlania myszy w środku organizmu została obliczona jako 1,21-krotność wyżej wskazanych dawek, co oznacza, że dawka LD50 dla osobników w grupie kontrolnej była na poziomie 6,23 Gy. I chociaż działanie promieniochronne (DRF) Biobranu (wynoszące 1,14) nie było zbyt wysokie, należy dodać, że w całym badaniu nie zaobserwowano żadnych efektów ubocznych.
Nakatugawa S. (Uniwersytet Nagoya, JAPONIA) : The Report of Nagoya Univ. (Raport Uniwersytetu Nagoya), 2003
(f) Wpływ preparatu Biobran MGN-3 na wywołane doświadczalnie zaburzenia czynności wątroby u szczurów
W badaniu analizowano wpływ preparatu Biobran MGN-3 na zaburzenia czynności wątroby, a konkretnie wpływ preparatu na rozwój wywołanych doświadczalnie zaburzeń czynności wątroby wskutek podania D-galaktozaminy (GaIN) i acetaminofenu (AAP). GaIN podano w doświadczeniach 1 - 3, zaś AAP w doświadczeniach 4 i 5.
W doświadczeniu 1 szczurom podano dootrzewnowo preparat Biobran MGN-3 w różnych stężeniach, po czym po 1 godzinie wprowadzono im do organizmu GaIN w ilości 800 mg/kg.
W doświadczeniu 2 podano doustnie niefrakcjonowany Biobran MGN-3 i dootrzewnowo jego frakcje o wysokiej lub niskiej masie cząsteczkowej. Po 1 godzinie do organizmu szczurów wprowadzono GaIN w ilości 800 mg/kg.
W doświadczeniu nr 3 Biobran MGN-3 podano dootrzewnowo po uprzednim podgrzaniu, zhydrolizowaniu i przefiltrowaniu przez żywicę jonowymienną. Po 1 godzinie szczurom podano GaIN w ilości 800 mg/kg.
W doświadczeniu nr 4 Biobran MGN-3 wprowadzono dootrzewnowo i doustnie, a po 1 godzinie do organizmu szczurów wprowadzono AAP w ilości 700 mg/kg.
W doświadczeniu nr 5 Biobran MGN-3 podano dootrzewnowo po uprzednim podgrzaniu, zhydrolizowaniu i przefiltrowaniu przez żywicę jonowymienną. Po 1 godzinie szczurom podano AAP w ilości 500 mg/kg.
We wszystkich doświadczeniach szczury uśpiono 24 godziny po podaniu GaIN lub AAP i zbadano poziom transaminazy w surowicy krwi (GOT, GPT).
Wyniki
Doświadczenie 1: We wszystkich grupach, w których podawano Biobran
MGN-3 aktywność GOT i GPT w surowicy, wywołana przez zaburzenia funkcji wątroby
po podaniu GaIN została znacznie ograniczona w porównaniu z aktywnością zbadaną
w grupie kontrolnej. Działanie supresyjne preparatu Biobran MGN-3 na zaburzenia
funkcji wątroby wywołane przez GaIN było najwyższe
dla dawki 20 mg/kg, przy wyższych dawkach preparatu Biobran MGN-3 już nie wzrastało.
Doświadczenie 2: We wszystkich grupach, w których podawano Biobran MGN-3 w postaci niefrakcjonowanej lub frakcjonowanej, z wyższą lub niższą masą cząsteczkową, odnotowano znaczne ograniczenie wzrostu aktywności GPT w surowicy wskutek zaburzeń czynności wątroby wywołanych przez GaIN w porównaniu ze wzrostami w grupie kontrolnej. Działanie supresyjne frakcjonowanego i niefrakcjonowanego preparatu Biobran MGN-3 było podobne.
Doświadczenie 3: W grupach, w których podawano hydrolizowany Biobran MGN-3, odnotowano ograniczony wzrost aktywności GOT w surowicy wskutek zaburzeń czynności wątroby wywołanych przez GaIN w porównaniu ze wzrostami w grupie kontrolnej.
Doświadczenie 4: W grupach, w których podawano Biobran MGN-3 dootrzewnowo, odnotowano znacznie mniejszy wzrost aktywności GOT w surowicy wskutek zaburzeń czynności wątroby wywołanych przez AAP w porównaniu ze wzrostami w grupie kontrolnej.
Doświadczenie 5: Podobne wyniki jak w doświadczeniu nr 3 udało się osiągnąć z hydrolizowanym Biobranem MGN-3 również po podaniu AAP. W grupach, którym podawano hydrolizowany Biobran MGN-3, odnotowano znacznie ograniczony wzrost aktywności GOT w surowicy w porównaniu ze wzrostami w grupie kontrolnej.
Powyższe wynik doświadczeń potwierdzają, że Biobran MGN-3 ma działanie supresyjne na zaburzenia funkcji wątroby wywołane przez GaIN lub AAP. Wydaje się, że HCl nie hydrolizuje aktywnego składnika preparatu.
Yamada T. (Uniwersytet Chiba, JAPONIA): Streszczenie referatu z 87. Dorocznego Zjazdu Japońskiego Stowarzyszenia Badań nad Błonnikiem Pokarmowym, 2002
(g) Stosowanie preparatu Biobran MGN-3 doustnie łagodzi objawy zwykłego przeziębienia u osób starszych
W przypadku grup podwyższonego ryzyka, takich jak osoby starsze i dzieci, szczególnie ważna jest profilaktyka, taka jak szczepienia przeciwko grypie, ale przede wszystkim stosowanie środków, które pomagają zapobiegać wtórnej infekcji bakteryjnej. W badaniach zapalenia płuc nabytego wskutek pogorszenia się stanu w zwykłym przeziębieniu badano profil wiekowy i okazało się, że ryzyko wtórnej infekcji bakteryjnej jest wyższe u osób powyżej 75 roku życia. Niebezpieczeństwo współistniejącego zapalenia płuc jest również wyższe u starszych pacjentów ze schorzeniami neurologicznymi, u których istnieje znaczne ryzyko aspiracji. Dlatego zbadaliśmy kliniczne korzyści podawania preparatu Biobran MGN-3 w profilaktyce rozwoju zwykłego przeziębienia u osób starszych, u których zdolność do odpowiedzi immunologicznej jest z wielu powodów niższa.
Wśród pacjentów znajdujących się pod opieką ośrodka zdrowia Atreyu Uozaki w Kobe, prefektura Hyōgo, w okresie od stycznia do marca 2002 roku wybrano grupę starszych osób, które nie cierpiały na żadną poważną chorobę i zgodziły się na udział w badaniu. Badano suplement diety, frakcję preparatu Biobran MGN-3 (HRB), zaś w grupie kontrolnej zastosowano błonnik ryżowy zawierający przede wszystkim elementy rozpuszczalne w wodzie (RB).
Liczono dni, kiedy występował choć jeden z objawów przeziębienia (gorączka, bóle głowy, zmęczenie, dreszcze, kaszel, plwociny, wydzielina z nosa, niedrożność nosa, ból gardła, bóle w klatce piersiowej). Każdy objaw był oceniany w zależności od intensywności występowania (brak = 0, łagodne objawy = 1, średnie = 2, wyraźne = 3), a następnie podzielono całkowity wynik każdego pacjenta przez liczbę dni, kiedy podawano mu badaną substancję, otrzymując w ten sposób „objawowy wskaźnik przeziębienia”.
Wyniki:Spośród poszczególnych objawów, kaszel, zmęczenie, gorączka i ból gardła występowały w znacznym stopniu na początku terapii w obu grupach. W grupie HRB całkowita liczba dni, kiedy występowały objawy, była niższa niż w grupie RB. W grupie RB odnotowano ogólnie wyższy objawowy wskaźnik przeziębienia. I chociaż wskaźnik objawów nosowych był niższy w grupie RB, wskaźniki pozostałych zwykłych objawów, takich jak kaszel, zmęczenie i gorączka były wyższe. Prowadzi to zatem do wniosku, że objawy zwykłego przeziębienia występowały w mniejszym stopniu w grupie HRB.
Badanie pokazało, że przez podawanie doustnie starszym pacjentom cierpiącym na zwykłe przeziębienie HRB, czas występowania objawów skrócił się, objawy nie pogarszały się, co dzięki immunomodulującemu działaniu wyciągu, zmniejszyło konieczność prowadzenia leczenia objawowego.
Tazawa K. (Akademia Medycyny i Farmacji w Toyama , JAPONIA): Magazyn Medycyny Tradycyjnej, 20 (3), 2003
3.7. Działanie antyalergiczne
(a) Ocena działania profilaktycznego preparatu Biobran MGN-3 oraz łagodzenia objawów astmy w mysim modelu astmatycznym
W badaniu obserwowano działanie profilaktyczne preparatu Biobran MGN-3 i łagodzenie objawów astmy w mysim modelu astmy wywołanej przez diizocyjanianotoluen (TDI).
Na początku przygotowano roztwór wody pitnej i preparatu Biobran MGN-3 w stężeniu 2 g/litr, który podano myszom (samicom linii BALB/c), podzielonym na 4 grupy (A-D):
Grupa A: Biobran MGN-3 podawano miesiąc przed i w trakcie fazy uczulania TDI oraz po niej.
Grupa B: Biobran MGN-3 podawano miesiąc przed oraz po zakończeniu fazy uczulania TDI.
Grupa C: Biobran MGN-3 podawano wyłącznie w trakcie fazy uczulania TDI.
Grupa D: Grupa kontrolna.
W grupie B oceniano działanie profilaktyczne, a w grupie C – efekt łagodzenia objawów. Działanie preparatu Biobran badano na podstawie stężenia histaminy we krwi, liczby eozynofili w popłuczynach oskrzelowo-pęcherzykowych (BALF), testu podania TDI na płatku ucha i parametrów swoistych przeciwciał typu IgG1, IgG2a, IgE we krwi w trakcie uczulania.
Najwyższe stężenie histaminy we krwi stwierdzono 7 minut po podaniu TDI i było ono następujące: grupa A: 2,5±0,53, grupa B: 4,2±0,75, grupa C: 4,3±7,8, grupa D: 6,4±0,87 (ng/ml), zatem w grupach otrzymujących Biobran MGN-3 wartości były znacznie niższe niż w grupie kontrolnej. W badaniach wrażliwości dla różnych stężeń TDI (0,01-10%) w grupach, w których podawano Biobran MGN-3 nastąpiło nawet 10-100-krotne obniżenie wrażliwości w porównaniu z grupą kontrolną. Ponadto w grupach otrzymujących Biobran MGN-3 stwierdzono znacznie niższy poziom eozynofili w BALF oraz niższe parametry w teście podania TDI. Z drugiej strony, między poszczególnymi grupami nie odnotowano żadnych istotnych różnic jeżeli chodzi o poziom przeciwciał we krwi.
Wniosek końcowy zatem jest taki, że podawanie preparatu Biobran MGN-3 w udowodniony sposób działa profilaktycznie i łagodzi objawy astmy w mysim modelu astmy wywołanej przez diizocyjanianotoluen (TDI). Ponadto badania sugerują, że Biobran MGN-3 nie wpływa na wytwarzanie przeciwciał typu IgG1 czy IgE, wywołane przez Th2 oraz że działa jako czynnik supresyjny względem komórek tucznych.
Kobayashi H., Endo Y. (Mc Master University, KANADA): Streszczenie referatu z 52. Dorocznego Spotkania Japońskiego Towarzystwa Alergologicznego, 2002
(b) Wpływ preparatu Biobran MGN-3 na hamowanie rozwoju atopowego zapalenia skóry u myszy NC
Badanie było poświęcone działaniu immunoregulacyjnemu preparatu Biobran MGN-3 na myszy NC, u których w naturalny sposób następuje wzrost poziomu IgE w surowicy, zaś jako reakcja na uczulenie owoalbuminą (OVA) pojawiają się u nich zmiany skórne przypominające atopowe zapalenie skóry (AZS). Biobran MGN-3 podawano doustnie pięciu osobnikom myszy linii NC, które porównywano z grupą kontrolną bez preparatu Biobran MGN-3. Następnie myszy uczulono owoalbuminą. Próbki krwi pobrano dwa tygodnie przed i po uczuleniu. Ilość całkowita IgE, a także poziom swoistych IgE anty-OVA w surowicy krwi oznaczona w teście ELISA u myszy leczonych preparatem Biobran MGN-3 w porównaniu z osobnikami z grupy kontrolnej była znacznie niższa. Oprócz faktu, że u osobników NC otrzymujących Biobran MGN-3 wystąpiły zmiany skórne przypominające atopowe zapalenie skóry (AZS), u myszy NC leczonych preparatem Biobran MGN-3 takie zmiany nie wystąpiły u pięciu z pięciu osobników. Stwierdzono zatem, że preparat Biobran MGN-3 wpływa na hamowanie rozwoju atopowego zapalenia skóry u myszy NC
Nonoyama S. (Akademia Medycyny i Stomatologii w Tokio, JAPONIA): Streszczenie referatu z 11. Dorocznego Spotkania Międzynarodowego Kongresu Immunologicznego, 2001
© Copyright 2003: Hiroaki Maeda / Daiwa Pharmaceutical
(Dziękujemy za pozwolenie na zamieszczenie tego artykułu na stronie Biobran.org.)
 Kierownikiem badań nad preparatem Biobran jest dr Mamdooh Ghoneum, profesor w Katedrze Immunologii Charles R. Drew University of Medicine and Science w USA. Dr Ghoneum jest znanym na całym świecie ekspertem w dziedzinie immunoterapeutycznego podejścia do leczenia nowotworów, który zdobył tytuł doktora radioimmunologii na Uniwersytecie Tokijskim i od tamtej pory poświęca się pracy w dziedzinie immunologii na Uniwersytecie Kalifornijskim (UCLA) w Los Angeles. W ciągu ostatnich 20 lat badał różne substancje poprawiające funkcjonowanie układu odpornościowego, jednak, jak twierdzi, nie spotkał się jeszcze z preparatem wzmacniającym odporność o równie silnym działaniu jak Biobran MGN-3. Był pod tak dużym wrażeniem wyników badań, iż obecnie poświęca całą swoją uwagę naukową leczeniu z użyciem tego związku.
Kierownikiem badań nad preparatem Biobran jest dr Mamdooh Ghoneum, profesor w Katedrze Immunologii Charles R. Drew University of Medicine and Science w USA. Dr Ghoneum jest znanym na całym świecie ekspertem w dziedzinie immunoterapeutycznego podejścia do leczenia nowotworów, który zdobył tytuł doktora radioimmunologii na Uniwersytecie Tokijskim i od tamtej pory poświęca się pracy w dziedzinie immunologii na Uniwersytecie Kalifornijskim (UCLA) w Los Angeles. W ciągu ostatnich 20 lat badał różne substancje poprawiające funkcjonowanie układu odpornościowego, jednak, jak twierdzi, nie spotkał się jeszcze z preparatem wzmacniającym odporność o równie silnym działaniu jak Biobran MGN-3. Był pod tak dużym wrażeniem wyników badań, iż obecnie poświęca całą swoją uwagę naukową leczeniu z użyciem tego związku.



 Wykres 5: Procentowy udział tworzenia wiązań przez komórki NK i komórki docelowe K562. Legenda: % wiązań > Przed stosowaniem > Po stosowaniu
Wykres 5: Procentowy udział tworzenia wiązań przez komórki NK i komórki docelowe K562. Legenda: % wiązań > Przed stosowaniem > Po stosowaniu
 Wykres 6: Śmiertelne formacje komórek NK i docelowych komórek
Wykres 6: Śmiertelne formacje komórek NK i docelowych komórek
 Wykres 7: Mysie makrofagi otrzewnowe (myszy C3H/He) Matsuura M. (Akademia Medyczna Jichi, Japonia) : Raport Akademi Medycznej Jichi
Wykres 7: Mysie makrofagi otrzewnowe (myszy C3H/He) Matsuura M. (Akademia Medyczna Jichi, Japonia) : Raport Akademi Medycznej Jichi


