3. FYZIOLOGICKÉ PÔSOBENIE ARABINOXYLÁNOVÉHO DERIVÁTU Z RYŽOVÝCH OTRÚB (Biobran)
3.1. ImunoREGULÁCIA
(a) Zvyšovanie aktivity ľudských NK buniek za pomoci modifikovaného arabinoxylánu z ryžových
otrúb (Biobran MGN-3)
1. In vitro test
NK bunky z potkana boli inkubované s cieľovými nádorovými bunkami K-562 za prítomnosti
prípravku Biobran MGN-3 a následne bolo 51Cr separačným testom zmerané množstvo rozložených
buniek K-562. Zvýšená koncentrácia rozložených buniek bola nameraná v závislosti od
koncentrácie prípravku Biobran MGN-3 (ktorá bola 25 µg/ml, resp. 100 µg/ml), čo potvrdilo,
že nárast aktivity NK buniek bol zapríčinený pôsobením prípravku Biobran MGN-3.
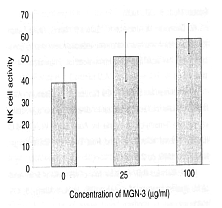 Legenda: Aktivita NK buniek > Koncentrácia MGN-3 (µg/ml)
Legenda: Aktivita NK buniek > Koncentrácia MGN-3 (µg/ml)
2. In vivo test (na potkanoch)
Biobran MGN-3 bol orálne podávaný potkanom Sprague-Dawley a po dvoch týždňoch bola zmeraná
aktivita NK buniek. Potkany boli rozdelené do troch skupín po 5 jedincoch s podávanými
dávkami v koncentráciách 0,5 mg, 5 mg, resp. 50 mg/kg/denne. V závislosti od koncentrácie
podávanej dávky Biobran MGN-3 bola nameraná aj zvýšená aktivita NK buniek. V skupinách
s dávkami 0,5 mg, 5 mg a 5 mg bola oproti kontrolnej skupine táto aktivita zvýšená o 119 %,
130 %, resp. 142 %. V skupine s 50 mg dávkou sa aktivita zdvihla na úroveň 132 % oproti
kontrolnej skupine už po troch dňoch od začiatku podávania prípravku. Nárast aktivity NK
buniek, zapríčinený prípravkom Biobran MGN-3, možno pripísať zvýšenej ničivej sile NK
buniek, no zároveň závisel aj od celkového počtu NK buniek. Bol pozorovaný rozdiel v účinku
u samcov a u samíc, pričom účinok bol intenzívnejší u samíc (Obr. 3).
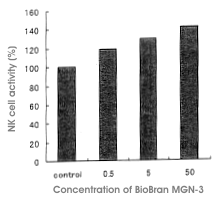 Legenda: Aktivita NK buniek (%) > Koncentrácia prípravku BioBran MGN-3
Legenda: Aktivita NK buniek (%) > Koncentrácia prípravku BioBran MGN-3
3. Pôsobenie na ľudí
V rámci testovania pôsobenia prípravku Biobran MGN-3 na ľudí 24 zdravých jedincov (15 žien
a 9 mužov s priemerným vekom 34 rokov) užívalo prípravok nepretržite po dobu 60 dní a bola
pozorovaná u nich aktivita NK buniek. Účastníci boli rozdelení do 3 skupín po 8 ľudí
s dennými dávkami 15 mg/kg, 30 mg/kg, resp. 45 mg/kg/telesnej hmotnosti. Každému účastníkovi
bola odobraná vzorka krvi (20 ml) pred užívaním prípravku, po týždni užívania, po mesiaci,
po dvoch mesiacoch (po skončení užívania) a mesiac od skončenia užívania a bola zmeraná
aktivita NK buniek. V skupinách s dávkou 30 mg a 45 mg vzrástla aktivita NK buniek po týždni
od začatia užívania na dvojnásobok a po dvoch mesiacoch na trojnásobok. V skupine s dávkou
15 mg vzrástla aktivita rapídne po mesiaci užívania a po dvoch mesiacoch dosiahla takmer
rovnakú úroveň ako v skupinách 30 mg a 45 mg. Mesiac po skončení užívania sa aktivita NK
buniek vrátila na úroveň pred testom (Obr. 4). Tieto výsledky naznačujú, že príjem 15 – 45
mg/kg prípravku Biobran MGN-3 denne má reálny dopad na aktivitu ľudských NK buniek.
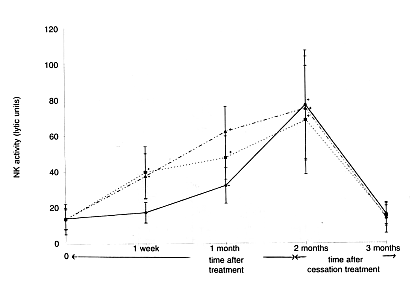
Obr. 4: Časová a dávková závislosť aktivácie NK buniek prípravkom Biobran
MGN-3 voči
nádorovým bunkám K562…_.._.._.._ = 45mg/kg/denne; …………=30mg/kg/denne; _______=15mg/kg/denne
4. Mechanizmus pôsobenia prípravku Biobran MGN-3 na NK bunky
Oba testy, in vitro aj in vivo, potvrdili, že množstvo cytotoxických granúl v NK bunkách
stimulovaných prípravkom Biobran MGN-3 sa zvyšuje. Preskúmaná bola aj schopnosť týchto
buniek viazať sa na cieľové bunky. V teste boli NK bunky jedinca, ktorý užíval 45 mg/kg
prípravku Biobran MGN-3 denne po dobu 30 dní inkubované s cieľovými bunkami K-562 a následne
bola zmeraná ich schopnosť viazať sa na cieľové bunky. Po hodinovej spoločnej inkubácii pri
teplote 4°C bolo zmeraných 200 NK buniek a vyrátaná miera vytvárania väzieb s K-562. Miera
vytvárania väzieb NK buniek s cieľovými bunkami (K-562) bola u jedinca po užívaní prípravku
Biobran MGN-3 výrazne vyššia než pred užívaním, o 38,5 % oproti 9,4 %. Na Obr. 6 je
fotografia takýchto väzieb.
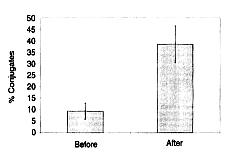 Obr. 5: Percentuálny podiel formovania väzieb medzi prirodzenými zabíjačmi
(NK bunkami)
a cieľovými bunkami K562. Legenda: % väzieb > Pred užívaním > Po užívaní
Obr. 5: Percentuálny podiel formovania väzieb medzi prirodzenými zabíjačmi
(NK bunkami)
a cieľovými bunkami K562. Legenda: % väzieb > Pred užívaním > Po užívaní
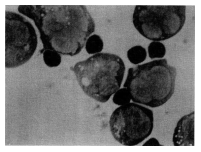 Obr. 6: Smrtiace formácie NK buniek a cieľových nádorových buniek.
Obr. 6: Smrtiace formácie NK buniek a cieľových nádorových buniek.
Ghoneum M. (Univerzita Ch. R. Drewa, USA):INT. IMMUNO THERAPY XIV (2) s.89-99, 1998
(b) In vitro účinok prípravku Biobran MGN-3 na aktivitu buniek zo skupiny makrofágov
Skúmaný bol účinok prípravku Biobran MGN-3 na bunky zo skupiny makrofágov, na indukovanie
produkovania farmakologických mediátorov, konkrétne mediátorov TNF-A, IL-6 a NO. Makrofágy
boli inkubované s prípravkom Biobran MGN-3 v rôznych koncentráciách (od 1 do 100 µg/ml)
a supernatanty boli následne testované na prítomnosť uvedených mediátorov. TNF-a bol
analyzovaný podľa cytotoxicity voči L929, IL-6 podľa cytózy B13.19 a NO kolorimetricky podľa
reakcie s Griessovym reagentom. Ako pozitívna kontrola bol použitý LPS (lipopolysacharid? –
pozn. prekl.).
- Pri použití myšacej bunkovej línie makrofágov RAW264.7, Biobran MGN-3 vykázal silné
pôsobenie na uvedené tri mediátory už pri koncentráciách vyšších než 10 µg/ml, rovnako
ako LPS.
- Použitie myšacích peritoneálnych makrofágov (C3H/He). Účinok prípravku Biobran MGN-3
proti vylučovaniu makrofágov z peritoneálnej dutiny u normálnej myši je zobrazený na
Obr. 7. Biobran MGN-3 opäť vykázal silné pôsobenie pri koncentráciách nad 10 µg/ml.
- Bunková línia ľudských makrofágov U937. MGN-3 indukoval silnú aktivitu, čo naznačujú
namerané hladiny vyprodukovaných cytokínov TNF-A a IL-6, ktoré boli ekvivalentné LPS na
úrovni 100 µg/ml.
Výsledky ukazujú, že Biobran MGN-3 má silný potenciál aktivovať normálne myšacie aj ľudské
makrofágy. Zo štúdií vyplýva, že aktívne sú koncentrácie nad 10 µg/ml.
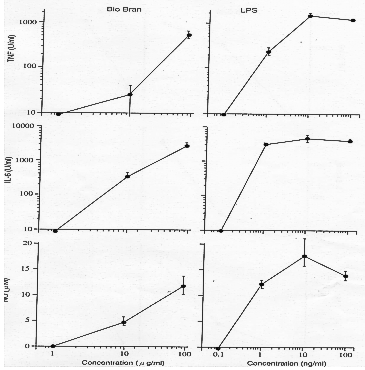 Obr. 7: Myšacie peritoneálne makrofágy (C3H/He)
Obr. 7: Myšacie peritoneálne makrofágy (C3H/He)
(c) Imunostimulácia a prevencia rakoviny
Množstvo štúdií preukázalo, že u ľudí, ktorí sú na pracovisku vystavení vplyvu rôznych
chemikálií existuje zvýšené riziko rakoviny. Jedna z takýchto štúdií si dala za cieľ
preskúmať zmenu imunity súvisiacu s vplyvom toxických chemikálií a možnosť organizmu lepšie
reagovať na chemickú toxicitu pomocou prípravku Biobran MGN-3.
Štúdie sa zúčastnilo jedenásť ľudí, ktorí bývajú v práci vystavení vplyvu chemikálií.
Účastníci trpeli imunitnou dysfunkciou, ktorá sa prejavovala nízkymi hladinami NK bunkovej
aktivity (10,2±4,2 LU (lytických jednotiek – pozn. prekl.), blastogénnou odpoveďou krvných
lymfocytov na T-bunkové mitogény (PHA, 39060±12517cpm a COMA, 36224±11922cpm) a B-bunkové
mitogény (PWM, 16550±6330cpm) oproti odpovediam v kontrolnej skupine. Účastníci dostávali
denne počas štyroch mesiacov 15 mg/kg prípravku Biobran MGN-3. Liečba prípravkom zvýšila NK
bunkovú aktivitu 4-násobne po dvoch a 7-násobne po štyroch mesiacoch a fungovanie T- a B
buniek sa zvýšilo na úroveň 130, resp. 150 % oproti pôvodným hodnotám.
Ghoneum M. (Univerzita Ch. R. Drewa, USA) : Abstrakt z konferenčného zborníka zo 7.
medzinárodného kongresu o biomedicínskych technológiách zameraných proti starnutiu, 1999
(d) Stimulovaná produkcia TNF-α a IF-γ v lymfocytoch z ľudskej periférnej krvi
sprostredkovaná modifikovaným arabinoxylánom z ryžových otrúb obsiahnutým v prípravku
Biobran MGN-3.
Skúmaný bol mechanizmus, ktorým Biobran MGN-3 zvyšuje NK bunkovú cytotoxickú aktivitu.
Testované bolo pôsobenie prípravku Biobran MGN-3 na intenzitu vylučovania tumor
nekrotizujúceho faktora-α, (TNF-α) a interferónu-γ (IFN-γ) a na expresiu kľúčových
receptorov na povrchu buniek.
Lymfocyty z periférnej krvi boli inkubované s prípravkom Biobran MGN-3 v koncentráciách 0,1
a 1 mg/ml a roztoky boli podrobené testu ELISA. Výsledky preukázali, že Biobran MGN-3 je
potentný induktor TNF-α, pričom účinok závisel od dávky. Koncentrácie Biobran MGN-3 na
úrovni 0,1 a 1 mg/ml zdvihli produkciu TNF-α 22,8-, resp. 47,1-násobne. Biobran MGN-3
taktiež zvýšil produkciu IFN-γ, i keď v porovnaní s TNF-α v nižšej miere. Čo sa týka
kľúčových povrchových bunkových receptorov, Biobran MGN-3 zvýšil expresiu antigénu včasnej
aktivácie CD69 po 16 hodinách inkubácie. Okrem toho, po inkubácii s prípravkom Biobran MGN-3
bola pozorovaná upregulácia receptora interleukínu-2, CD25 a medzibunkovej adhezívnej
molekuly ICAM-1 (CD54). Aj inkubácia vysoko purifikovaných NK buniek s prípravkom MGN-3 mala
za následok zvýšené hladiny vylučovania TNF-α a IFN-γ v kombinácii so zlepšením NK-bunkovej
cytotoxickej funkčnosti. Navyše, pridanie prípravku Biobran MGN-3 k NK bunkám aktivovaným
interleukínom-2 malo za následok synergickú indukciu vylučovania TNF-α a IFN-γ.
Ghoneum M. (Univerzita Ch. R. Drewa, USA), Jewett A. (UCLA, USA) : Cancer Detection and
Prevention (Odhaľovanie a prevencia rakoviny) Zv.24/Číslo 4, 2000
(e) Účinok modifikovaného arabinoxylánu z ryžových otrúb na NK-bunkovú aktivitu ľudských
lymfocytov z periférnej krvi.
Skúmané boli účinky prípravku Biobran MGN-3 a jeho molekulárnych frakcií na NK-bunkovú
aktivitu. K ľudským lymfocytom z periférnej krvi boli pridané frakcie s vysokou molekulárnou
hmotnosťou (10 – 50 kDa), získané gélovou filtráciou s použitím média Sephadex G-25 a G-75.
Po 3-dňovej inkubácii bola stanovená aktivita NK buniek. Ako cieľové bunky boli použité
fluorescenčne označené bunky línie K-562 a NK-bunková aktivita bola stanovená fluorescenčnou
metódou Tere Scan. Rovnaký experiment bol uskutočnený za prítomnosti IL-2.
Pokusy neodhalili zásadné rozdielnosti v aktivácii NK buniek či už prípravkom Biobran MGN-3
alebo jeho frakciami s vyššou molekulárnou hmotnosťou. Keď však bol do média pridaný IL-2,
v roztokoch, kde bol okrem neho prítomný aj Biobran MGN-3 alebo jeho frakcie, bola, oproti
roztoku, kde bol prítomný len samotný IL-2, pozorovaná zvýšená NK-bunková aktivita.
Naznačuje to, že Biobran MGN-3 aktivuje NK bunky v prítomnosti IL-2 a že takáto aktivita je
prítomná aj s jeho frakciami s vyššou molekulárnou hmotnosťou.
Ueda Y., Shimomura C. (Univerzita v Čibe, JAPONSKO) : Abstrakt z výročného stretnutia
Japonskej spoločnosti pre biovedy, biotechnológie a agrochémiu 2002
3.2. Protivírusové účinky
Protivírusové pôsobenie prípravku Biobran MGN-3 proti HIV in vitro
Najprv bolo hodnotené protivírusové pôsobenie prípravku Biobran MGN-3 proti produkcii HIV-1
antigénu p24 in vitro. Mononukleárne bunky získané od troch zdravých jedincov boli
inkubované s kmeňom HIV-1 SF pri teplote 37°C počas jednej hodiny za prítomnosti prípravku
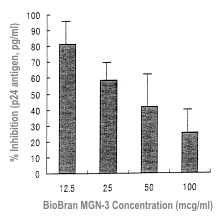
Biobran MGN-3 v koncentráciách od 0 do 100 µg/ml. V závislosti od koncentrácie, prípravok
Biobran MGN-3 inhiboval tvorbu syncytiálnych formácií, pričom maximálna miera tejto
inhibície bola na úrovni 75 % pri koncentrácii 100/ml) (Tabuľka 1).
 |
|
Tabuľka 1
| Inhibícia syncytiálnych formácií prípravkom Biobran
|
| Dávka Biobranu (μg/ml) |
Syncytiálne formácie (SF) |
| Počet SF |
% Inhibícia |
0
12.5
25
50
100
|
42.0±8
25.8±7
21.5±5
15.8±4
10.5±3
|
00.0
38.5
50.0
62.5
75.0
|
|
| Obr. 8 |
|
Legenda: % inhibície (antigén p24, pg/ml) > Koncentrácia
prípravku BioBran MGN-3 (µg/ml)
|
Ghoneum M. (Università Ch. R. Drew, USA): Biochemical and Biophysical Research
Communications (Comunicazioni tra ricerca biochimica e biofisica) 243, (1998)
3.3. Protinádorový účinok
(a) Štúdia pôsobenia zložiek modifikovaného arabinoxylánu z ryžových otrúb na inhibíciu
rastu rakovinových buniek rôznych línií
V tejto štúdii bol skúmaný inhibičný účinok modifikovaného arabinoxylánu z ryžových otrúb,
obsiahnutého v prípravku Biobran MGN-3, na rast rakovinových buniek rôznych línií, ako sú
HL60, K562 a HLE a na potenciálne indukovanie diferenciácie u HL60 a K562. Biobran MGN-3 bol
pridaný do kultúry s bunkovými líniami. Po 3-dňovej inkubácii sa pomer preživších buniek
u všetkých bunkových línií znížil úmerne s pridaným množstvom prípravku Biobran MGN-3.
Po precipitácii s etanolom bol precipitát zmiešaný s destilovanou vodou, vzniknutý
supernatant bol frakcionovaný pomocou stĺpca Sephadex G-25 na 3 frakcie (A, B, C) a tie boli
pridané do kultúr s bunkovými líniami. Inhibičné účinky na rast boli pozorované, pri frakcii
C, na línie HL60 a K562 a pri frakciách B a C, na líniu HLE. Na dôvažok, farbenie podľa
Giemsa a nešpecifickou esterázou vykázalo potenciálnu indukciu diferenciácie u HL60 a K562.
Tieto výsledky naznačujú, že Biobran MGN-3 obsahuje zložky, ktoré vykazujú inhibíciu rastu
rakovinových buniek a potenciálnu indukciu diferenciácie línií HL60 a K562.
Masada M. (Univerzita v Čibe., JAPONSKO) : Abstrakt z výročného stretnutia Japonskej
spoločnosti pre biovedy, biotechnológie a agrochémiu 2002
(b) Vplyv prípravku Biobran MGN-3 na rast nádorových buniek
Skúmaný bol priamy vplyv prípravku Biobran MGN-3 na rast kožných rakovinových buniek
a produkciu cytokínu. V porovnaní s kontrolnou skupinou buniek skvamózneho karcinómu
bunkovej línie SCC13, ktorá bola kultivovaná v MEM médiu, kde nárast počtu buniek
pokračoval, inkubácia buniek tejto línie [SCC13] s prípravkom Biobran MGN-3 rast nádorových
buniek zastavila (pozorovaných o 30 % menej buniek po 48 hodinách a o 50 % menej po 72
hodinách kultivácie oproti uvedenej kontrolnej kultivácii).
Analýzy prietokovou cytometriou ukázali, že po 16 hodinách inkubácie buniek SCC13
s prípravkom Biobran MGN-3 došlo k päťnásobnému zvýšeniu vnútrobunkových hladín interleukínu
10 [IL-10], no nedošlo k žiadnej zjavnej zmene v obsahu interferónu-γ [INF-γ]. ELISA testy
kultivačného média s bunkami SCC13 preukázali 8-násobne vyššie hladiny IL-10 a 3-násobný
nárast IL-12. Zaznamenaná bola len malá zmena v koncentrácii INF-γ. Okrem toho bol
zhodnotený vplyv prípravku Biobran MGN-3 aj na ďalšie bunkové línie, ako sú normálne
a nádorové prsníkové bunky a rakovinové bunky prostaty.
Tieto zistenia naznačujú, že Biobran MGN-3 pôsobí nielen zlepšovaním imunity hostiteľského
organizmu, ale aj priamym vplyvom na rast nádorových buniek a produkciu cytokínov. Zároveň
sa za týmito zisteniami môže ukrývať onen zatiaľ neznámy mechanizmus pôsobenia, ktorý by
vysvetlil pôsobivý klinický úspech a impozantný prínos liečby prípravkom Biobran MGN-3,
pozorovaný autorom v uplynulých 4 rokoch.
Ghoneum M. (Univerzita Ch. R. Drewa, USA) : Abstrakt z konferenčného zborníka z 8.
medzinárodného kongresu o biomedicínskych technológiách zameraných proti starnutiu, 2000
3.4. Doplnkový efekt pri liečbe rakoviny
(a) Vyhodnotenie súvisu NK-bunkovej aktivity a miery prežitia u pacientov s rôznymi typmi
rakoviny pri aplikovaní multiimunologických liečebných protokolov
Predložená štúdia si dala za cieľ stanoviť či administrácia prípravku Biobran MGN-3 mohla
mať efekt predlženia života a zlepšenia kvality prežívania na vzorke 205 onkologických
pacientov s progresívnou a čiastočne metastázujúcou rakovinou v neskorom III. – IV. štádiu,
po chirurgickom zákroku. Klinickej štúdie sa zúčastnili hospitalizovaní pacienti na
chirurgickej klinike Sano v Japonsku. Boli liečení doplnkovými alternatívnymi liekmi
a konvenčnými protirakovinovými liečivami so slabými vedľajšími účinkami.
205 pacientov hospitalizovaných po dobu 6 mesiacov bolo rozdelených do dvoch skupín: 109
pacientov z kontrolnej skupiny bolo liečených štandardnou klinickou doplnkovou alternatívnou
liečbou a 96 pacientom bol navyše po dobu jeden a pol roka pridávaný prípravok Biobran
MGN-3.
U všetkých pacientov bola na zistenie variácie imunoparametrov meraná aktivita NK buniek.
Súčasne bola u všetkých pacientov kontrolovaná kvalita prežívania. NK-bunková aktivita bola
u pacientov po chirurgickom zákroku prevažne nízka, no u pacientov, ktorým bol podávaný
Biobran MGN-3 bola vykázaná zvýšená miera apotanázie (dlhšieho prežitia), pričom tento efekt
bol u pacientov tým vyšší, čím vyššiu NK-bunkovú aktivitu vykazovali. (Tabuľka 2) Tieto
zistenia naznačili, že úroveň NK-bunkovej aktivity možno pri progresívnych typoch rakoviny
považovať za patologický ukazovateľ. V skupine, ktorej bol podávaný aj Biobran MGN-3 bolo
zároveň pozorované zlepšenie kvality života.
Tabuľka 2: Vzťah medzi celkovou mierou prežitia, NK-bunkovou aktivitou a mierou prežitia v 2
posudzovaných skupinách
| Skupina |
Skupina Biobran |
Kontrolná skupina |
| Celková miera prežitia |
52/96 (54.2%) |
19/63 (33.9%) |
Kategórie podľa NK-bunkovej aktivity
Nižšia než 19.9%
20%-40%
Vyššia než 40%
|
17/40 (42.5%)**
18/35 (51.4%)*
17/21 (81.0%)
|
2/16 (12.5%)
7/25 (28.0%)
10/15 (66.7%)
|
% významnosti voči kontrolnej skupine **p<0.01 *p<0.05
Takahara K. (Chirurgická klinika v Sano, JAPONSKO) : Abstrakt z 3. výročného stretnutia
Japonskej spoločnosti doplnkovú a alternatívnu medicínu a liečbu, 2000
(b) Imunomodulačné a protirakovinové účinky prípravku Biobran MGN-3 u 5 pacientok
s rakovinou prsníka
Piatimi pacientkam s rakovinou prsníka bol podávaný prípravok Biobran MGN-3 v dávke 3
g/denne a následne bola 51Cr separačným testom meraná NK-bunková aktivita na cieľových
nádorových bunkách línie K562. Výsledky ukázali nasledovné:
-
Pri nízkych hladinách základnej NK-bunkovej aktivity (12,7 – 58,3 %) a pomeroch
efektor : target 12 a 100:1 sa pri liečbe prípravkom Biobran MGN-3 NK-bunková
aktivita u pacientok významne zvýšila (41,8 – 89,5 %), pričom pomery efektor :
target zostali zachované.
-
Zvýšená NK-bunková aktivita bolo pozorovaná už po 1-2 týždňoch od začatia liečby
a pri pokračujúcej administrácii prípravku Biobran MGN-3 sa naďalej zvyšovala.
-
Dve pacientky, ktoré sa štúdie zúčastnili od samého začiatku (liečili sa 6-8
mesiacov) sa dostali do úplnej remisie.
Ghoneum M. (Univerzita Ch. R. Drewa, USA) : Zborník z mimoriadnej konferencie Amerického
združenia pre výskum rakoviny, 1995
(c) Imunomodulačný účinok modifikovaného arabinoxylánu z ryžových otrúb obsiahnutého
v prípravku Biobran MGN-3 na NK bunky v skupine 27 onkologických pacientov
Skúmaný bol imunomodulačný efekt prípravku Biobran MGN-3 u 27 onkologických pacientov.
Pacienti trpeli rôznymi typmi pokročilých malignancií: 7 pacientov malo rakovinu prsníka, 7
prostaty, 8 viacnásobný myelóm, 3 leukémiu a 2 rakovinu krčka maternice. Všetci pacienti
podstupovali konvenčnú liečbu, ktorá bola doplnená o prípravok Biobran MGN-3 v dávke 3
g/denne, a následne bola skúmaná NK-bunková aktivita po 2 týždňoch, 3 mesiacoch a 6
mesiacoch. Aktivita NK buniek bola meraná 51Cr separačným testom a za cieľové boli použité
nádorové bunky línie K562, pričom pomery efektor : target boli od 12:1 po 100:1. Výsledky
naznačili nasledovné:
- Základná aktivita NK buniek bola u pacientov na nízkej úrovni.
- Liečba prípravkom Biobran MGN-3 spôsobila významné zvýšenie NK-bunkovej aktivity už po 2
týždňoch. Indukcia aktivity bola u jednotlivých typov rakoviny v percentuálnom vyjadrení
nasledovná: r. prsníka 154-332 %, prostaty 174-385 %, leukémia 100-240 % viacnás. myelóm
100-537 % a krčok maternice 100-275 %.
- NK-bunková aktivita sa kontinuálne zvyšovala aj po 3 a 6 mesiacoch liečby.
Ghoneum M. (Univerzita Ch. R. Drewa, USA): Abstrakt z 87. výročného stretnutia Amerického
združenia pre výskum rakoviny, 1996
(d) Prípad doplnkovej liečby metastázujúcej rakoviny pľúc pomocou prípravku Biobran
MGN-3
V tejto správe je prezentovaný prípad, kde boli dosiahnuté priaznivé výsledky ako dôsledok
aplikácie doplnkovej liečby prípravkom Biobran MGN-3 u pacienta s metastázujúcou rakovinou
pľúc zasahujúcou veľký objem kostí.
Pacientom bol 67-ročný muž. V auguste 1996 prišiel za lekárom kvôli drastickému poklesu
telesnej hmotnosti a silnému kašľu a vykašliavaniu. Bola diagnostikovaná rakovina pľúc
(skvamózny karcinóm) komplikovaná tuberkulózou (M. tuberculosis). Po prednostnej
antibiotickej liečbe tuberkulózy sa ďalej k tejto liečbe v októbri pridalo ožarovanie
rakoviny. V decembri tohto istého roku bola operatívne odňatá spodná polovica pravých pľúc
s nádorom. Po liečbe ožarovaním bol pacient v januári 1997 z nemocničnej liečby
prepustený.
V júni toho istého roku pacient opäť navštívil lekára sťažujúc sa na bolesť v hrudi napravo.
Vyšetrenie kostnou scintigrafiou potvrdilo početné kostné metastázy. Nádor sa rozšíril
hlavne v pravostranných rebrách, no bol rozsiaty v kostnom tkanive prakticky v celom tele.
V júli bola nasadená analgetická liečba retardovanými formami morfínu. Medzitým, od konca
mája, bola taktiež iniciovaná liečba prípravkom Biobran MGN-3 v dávke 3 g denne. Od januára
1998 sa bolesti začali zmierňovať. Kým Biobran MGN-3 bol podávaný sústavne naďalej,
retardovaný morfín bol postupne redukovaný a v júni celkom vysadený. Nádorový marker ICPP
bol v čase, keď sa potvrdil návrat ochorenia na úrovni 16,8 ng/ml a postupne sa znížil na
7,6 ng/ml v decembri 1997 a 6,7 ng/ml v júni 1998. Kostná scintigrafia odhalila výrazné
zlepšenie a potvrdilo sa, že šírenie nádoru do kostí je na ústupe. NK-bunková aktivita bola
v čase návratu ochorenia na úrovni 9,0 %, no postupne sa zvýšila a v súčasnosti sa drží na
vysokej úrovni.
Sobajima T. (Nemocnica Hoshigaoka Kosei Nenkin, JAPONSKO) : Abstrakt z 2. výročného
stretnutia Japonskej spoločnosti doplnkovú a alternatívnu medicínu a liečbu, 1999
(e) Aplikácia prípravku Biobran MGN-3 v pokonvenčnej liečbe
Liečba spiaceho nádoru sa v prístupe k rakovine v Japonsku stáva hlavným liečebným
konceptom. Hlavným cieľom takejto liečby je predĺženie života pacienta a súčasne zachovanie
jeho vysokej kvality. Dr. Tunekawa ju pacientom predpisuje na želanie, pričom zlepšenie
kvality života považuje za dôležitý terapeutický cieľ. V svojej správe uvádza, že má tridsať
štyri onkologických pacientov, u ktorých aplikuje kombináciu chemoterapie na potlačenie
spiaceho nádoru a doplnkovej a alternatívnej liečby a poskytuje opis terapeutického postupu
u troch z nich:
-
Pacienti (hlavné choroby): rakovina žalúdka u 3, rakovina pľúc u 3, zhubný lymfóm u
2, rakovina hrubého čreva (rektálnej časti) u 6, rakovina prsníka u 3 a iné typy
rakoviny u 17
-
Doba liečby: 6-18 mesiacov
-
Prípadové štúdie
-
T.S. (60), žena, rakovina žalúdka (IV. štádium), karcionomatózny zápal pobrušnice:
Pacientke bol v januári 2000 vyoperovaný skirhotický nádor žalúdka. Vo februári 2000
sa u nej rozvinul karcinomatózny zápal pobrušnice a súc v IV. štádiu podstúpila
gastrektómiu. CA19-9 bol 108. V auguste 2000 navštívila našu kliniku so sťažnosťami
na bolesti v bruchu, zápchu, anémiu a anorexiu. CA19-9 bol 390 a aktivita NK buniek
25,6. Bola jej naordinovaná kombinácia chemoterapie (TS1) a holistickej liečby. Na
zlepšenie imunity jej bol podávaný Biobran MGN-3 v dávke 3 g denne. O mesiac neskôr
boli hodnoty CA19-9 na úrovni 63. Hodnoty nádorových markerov sa postupne znižovali
a NK-bunková aktivita zvyšovala. V auguste 2001, o 11 mesiacov neskôr, bola hodnota
CA19-9 na úrovni 25 a aktivita NK buniek 51,5. U pacientky už v súčasnosti
nepretrvávajú takmer žiadne subjektívne symptómy a je aj dobre živená.
-
F.A. (46), žena, rakovina prsníka, s metastázami v driekovom stavci a maternici:
Pacientka podstúpila v júli 1998 operáciu rakoviny prsníka a bola jej nasadená
hormonálna a protirakovinová liečba. V marci 2001 jej boli zistené metastázy
v driekovom stavci a v apríli aj v maternici, na čo v máji 2001 podstúpila
hysterektómiu maternice. Bola prepustená domov s nasadeným Taxolom a Paraplatinom.
V júli 2001 navštívila Dr. Tunekawu so sťažnosťami na bolesti kostí. V tom čase bola
hladina CA 153, NCC-ST bola 439 a aktivita NK buniek 9,3. V liečbe bol ponechaný
Paraplatin a bola začatá holistická liečba. Do liečby bol na zlepšenie imunity
pridaný Biobran MGN-3 v dávke 3 g denne. O dva mesiace neskôr, boli markery CA už
len 18, NCC-ST 28,9 a aktivita NK buniek 22,0 a bolesť ustúpila. Následne pacientka
vykazovala stabilné znižovanie hladín nádorových markerov a zvyšovanie NK-bunkovej
aktivity. V júli 2002 boli hladiny CA na úrovni 14, NCC-ST 3,2, NK-bunková aktivita
59, bolesť úplne ustúpila a zistenia z kostnej scintigrafie boli menej nápadné.
V súčasnosti je pacientka dobre živená a teší sa, že sa môže opäť venovať hraniu na
bicích.
Tunekawa H. (Tokaiská Spoločnosť pre propagáciu holistickej medicíny, JAPONSKO): Abstrakt
z workshopu venovaného prípravku Biobran v Berlíne, 2002
(f) Hodnotenie pôsobenia prípravku Biobran MGN-3 pri liečbe rakoviny v progresívnom štádiu
Dr. Mizukami má skúsenosti s podávaním prípravku Biobran MGN-3 vzorke 97 onkologických
pacientov s rôznymi typmi rakovinou v progresívnom štádiu. Typy rakovín zahrňovali rakovinu
žalúdka, hrubého čreva, prsníka, pľúc, pankreasu, pečene, žlčovodu, hltanu, vaječníkov,
krčka maternice, maternice, obličiek, štítnej žľazy, prostaty, ústnej dutiny, viacnásobný
myelóm atď. Hoci pacienti už absolvovali chirurgické zákroky, chemoterapiu či ožarovanie vo
veľkých nemocniciach, prognóza u väčšiny z nich bola biedna. Trpeli metastázami a recidívou
a tak sa rozhodli navštíviť kliniku Dr. Mizukamiho a skúsiť imunoliečbu. Takmer všetci
pacienti, ktorým bol nasadený Biobran MGN-3 už v tom čase nepodstupovali chemoterapiu ani
ožarovanie. Na základe klinického pozorovania a dotazníkov bola následne podrobne skúmaná
kvalita prežívania. U všetkých pacientov užívajúcich Biobran MGN-3 bol pozorovaný jeden
spoločný fenomén.
V niekoľkých prípadoch sa kvalita prežívania pri užívaní prípravku Biobran MGN-3 zreteľne
zlepšila. Aj keď vo všeobecnosti kvalita prežívania u pacientov s rakovinou v pokročilom
štádiu má tendenciu s pribúdajúcim časom rovnomerne klesať, u pacientov, ktorí užívali
Biobran MGN-3 bola táto tendencia miernejšia a dokonca sa zmenila na tendenciu dlhšieho
prežívania pri dobrej kvalite života a dokonca boli zaznamenané aj príklady dlhodobého
prežívania.
Ohľadne kvality prežívania boli zaznamenané tieto pozorovania:
-
Napriek tomu, že dostať pod kontrolu silné bolesti nie je jednoduché a u pacientov
s rakovinou v pokročilom štádiu v mnohých prípadoch nie je iná možnosť než siahať po
morfíne, niektorí z tých pacientov, čo brali Biobran MGN-3 morfín nepotrebovali
a u ďalších, ktorí ho predsa len brali sa prejavila tendencia znižovania dávok.
-
Celkovo bola pozorovaná nižšia tendencia k pocitom slabosti.
-
Bola pozorovaná nižšia tendencia k strate chuti do jedla.
-
Tendencia k schopnosti zostávať doma a cítiť sa pred smrťou relatívne dobre.
-
Tendencia zachovávať si tesne pred smrťou jasnú myseľ a schopnosť komunikovať s
rodinou.
Dr Mizukami zhrnul svoje pozorovanie do konštatovania, že pre pacientov s rakovinou vo
vysokom štádiu je zásadná skutočnosť, že kvalita prežívania sa pri užívaní prípravku Biobran
MGN-3 nezhoršuje tak prudko, čo sa pre budúcnosť javí ako dôležitý aspekt aj pre medicínsky
prístup k liečbe rakoviny.
Mizukami O. (Výskumný inštitút na podporu zdravia a Laymanova nadácia New Life, JAPONSKO) :
Abstrakt z workshopu venovaného prípravku Biobran v Berlíne, 2002
5. Účinok na apoptózu
Biobran MGN-3 senzitivizuje ľudské leukemické T-bunky na apoptózu indukovanú receptorom
smrti (CD95)
V tejto štúdii bol skúmaný efekt prípravku Biobran MGN-3 na apoptózu indukovanú receptorom
smrti v ľudských leukemických bunkách línie HUT 78. Bunky HUT 78 boli najskôr ošetrené
prípravkom Biobran MGN-3 a následne boli inkubované s agnostickou protilátkou receptoru
smrti (Fas, CD95). Miera apoptózy bola stanovená prietokovou cytometriou FACScan s použitím
farbiva propidia jodného. Aktivácia kaspázy 3, kaspázy 8 a kaspázy 9 bola stanovená
prietokovou cytometriou. Potenciál na mitochondriálnej membráne bol zmeraný pomocou FACScan
s použitím farbiva DIOC6. Expresia CD95 a BCI-2 bola zmeraná prietokovou cytometriou.
Podľa zistení, Biobran MGN-3 v závislosti od veľkosti dávok zvyšuje mieru apoptózy
indukovanej anti-CD95. Zvýšená miera úmrtia buniek korelovala s nárastom depolarizácie
potenciálu na mitochondriálnej membráne a so zvýšenou aktivizáciou kaspázy 3, kaspázy 8
a kaspázy 9. Liečba prípravkom Biobran MGN-3 nemala žiadny vplyv na úroveň expresie CD95, no
spôsobovala downreguláciu expresie BCI-2. Tieto výsledky naznačujú, že Biobran MGN-3 zvyšuje
náchylnosť rakoviny k apoptóze sprostredkovanej ligandami smrti, čo môže byť pre
protirakovinové úsilie podstatná skutočnosť.
Ghoneum M. (Univerzita Ch. R. Drewa, USA) : Cancer Letter (Onkologické listy), 2003
3.6. Aktivácia vitálnej obrany
(a) Aktívne pôsobenie prípravku Biobran MGN-3 pri eliminácii kyslíkových radikálov
Správa referuje o výskume eliminačného pôsobenia prípravku Biobran MGN-3 a jeho zlomkov na
kyslíkové radikály. Biobran MGN-3 bol frakcionovaný na zlomky pomocou stĺpca Sephadex G-25.
Jednotlivé zlomky boli označené podľa veľkosti písmenami L, M a S (L molekulárna hmotnosť >
10000), M (molekulárna hmotnosť od 10000 do 3000) a S (molekulárna hmotnosť < 3,000).
Eliminačné pôsobenie aktívnych enzýmov bolo hodnotené meraním eliminačného pôsobenia na
superoxidový anión-radikál (•O2), eliminačného pôsobenia na hydroxylový radikál pochádzajúci
z Fentonovej reakcie (•OH) a eliminačného pôsobenia na hydroxylový radikál generovaný
ultrafialovým ožiarením.
Výsledky meraní sú zobrazené v nižšie uvedenej tabuľke. Najlepšie zo všetkých tvorbu
hydroxylového radikálu •OH generovanú •O2 a ultrafialovým žiarením inhiboval zlomok
prípravku Biobran s označením S (s najnižšou molekulárnou hmotnosťou). Vysokú mieru
pôsobenia vykázali všetky zlomky prípravku pri eliminácii hydroxylu (•OH) generovaného
Fentonovou reakciou. (Tabuľka 3)
Tabuľka 3
Eliminačné pôsobenie prípravku Biobran MGN-3 na aktívne kyslíkové radikály
(•O2 a •OH a UV indukované •OH)
| Typ aktívneho kyslíka a pôsobenie SOD |
Miera eliminácie superoxidového anión-radikálu (%) |
Pôsobenie SOD (superoxiddismutázy) (U/ml) |
Miera eliminácie UV-generovaného hydroxylového radikálu (%) |
| 20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
20 |
2.0
(mg/ml)
|
0.2 |
BioB
BioB-L
BioB-M
BioB-S
|
64.6
39.9
49.5
90.4
|
23.0
10.4
15.6
68.1
|
4.4
0
0
26.4
|
7.6
5.0
7.2
70.5
|
0.9
0.8
1.4
15.7
|
0
0
0
2.6
|
94.9
(72.6)
97.2
(41.8)
97.0
(45.4)
96.5
(71.0
|
78.9
(35.9)
34.4
(16.5)
68.4
(9.9)
55.1
(54.9)
|
3.3
(11.5)
3.3
(1.0)
8.7
(3.9)
4.2
(19.6)
|
·O2:HPX-XOD reakciou,·OH:Fentonovou reakciou
·OH generované UV-reakciou:365nm,4×103J/m2/min×5
Tazawa K. (Univerzita lekárstva a farmácie v Tojame, JAPONSKO) : Biotherapy (Bioterapia)
Zv.14, 2000
(b) Základná štúdia vplyvu arabinoxylánovej zlúčeniny (Biobran MGN-3) na aktiváciu vitálnej
obrany.
V tejto štúdii bol v zvieracom experimente pozorovaný vplyv prípravku Biobran MGN-3, jeho
biofylaktické pôsobenie, na mieru prežitia po indukovaní smrtiacej sepsy lipopolysacharidom
(LPS).
Na experiment boli použité myši kmeňa BALB/c (samce vo veku 5-7 týždňov). Myšiam
z testovanej skupiny bolo každý druhý deň po dobu dvoch týždňov, čiže celkovo sedem krát,
orálnou sondou podané 20 mg/kg, resp. 200 mg/kg prípravku Biobran MGN-3 rozpusteného vo
fosfátovom pufri (PBS) v objeme 0,5 ml. Myšiam z kontrolnej skupiny bolo v rovnakých
intervaloch orálne podávané 0,5 ml PBS. 12 hodín po poslednej orálnej dávke bolo každému
myšiemu jedincovi intraperitoneálne do tela vpravené 200 µg LPS a následne bol pozorovaný
stav jedincov. V ďalšom experimente bolo myšiam z oboch skupín, zo skupiny Biobran aj z
kontrolnej, každej vpravené do tela intraperitoneálne 100 µg LPS; myši boli následne
usmrtené v intervaloch 0, 2, 4 a 8 hodín po podaní LPS a bola im odobratá periférna krv zo
srdca. Po oddelení séra boli zmerané hodnoty IL-6 a TNF. Aktivita IL-6 bola meraná
s použitím buniek línie B9 a aktivita TNF biologickou skúškou na bunkách línie WEHI164-13.
Ako je vidno na obr. 9, po podaní 200 µg LPS miera prežitia, v porovnaní s kontrolnou
skupinou, bola podstatne lepšia v skupinách, kde bolo jedincom denne podávané 20 mg/kg a 200
mg/kg prípravku Biobran MGN-3 (skupina Biobran MGN-3 20 mg/kg verzus kontrolná skupina, p =
0,0456; skupina Biobran MGN-3 200 mg/kg verzus kontrolná skupina, p = 0,0232, analýza
Mantel-Coxovým testom). Pri podaní 100 µg LPS na jedinca v skupinách, kde bol predtým denne
podávaný Biobran MGN-3 v dávkach 20 mg/kg a 200 mg/kg prežili všetky myši, kým v kontrolnej
skupine 3 z 10 jedincov uhynuli.
V snahe odhaliť mechanizmus, ktorý stojí za zlepšenou mierou prežívania v skupine Biobran
MGN-3 boli zmerané krvné koncentrácie IL-6 a TNF. V skupine, kde bol podávaný Biobran MGN-3
bola krvná koncentrácia IL-6 po dvoch hodinách od podania LPS výrazne nižšia ako
v kontrolnej skupine (kontrolná skupina 702,9 ± 24,7 ng/ml, skupina Biobran MGN-3 403,1 ±
59,6 ng/ml; p < 0.01), avšak po 8 hodinách od podania sa výrazne zvýšila (kontrolná skupina
88,5 ± 50,0 ng/ml, skupina Biobran MGN-3 441,0 ± 115,0 ng/ml; p < 0.05). Krvná koncentrácia
TNF sa 4 hodiny po podaní LPS v skupine Biobran MGN-3 v porovnaní s kontrolnou skupinou
výrazne zvýšila (kontrolná skupina 492 ± 187, skupina Biobran MGN-3 1816 ± 307 pg/ml; p <
0.01).
Pri experimentálnom modeli s LPS-indukovanou smrteľnou sepsou sa predpokladalo, že veľké
množstvo zápalových cytokínov (IL-1, 6, TNF-α) uvoľnených z buniek retikuloendoteliálneho
systému do celého organizmu spôsobí zlyhanie početných orgánov, čo povedie k smrti. V tejto
štúdii však bolo v skupine, ktorej bol podávaný prípravok Biobran MGN-3 pozorované významné
zvýšenie miery prežitia. Možné príčiny sú, že príjem prípravku Biobran MGN-3 inhibuje tvorbu
histotoxických cytokínov produkovaných makrofágmi alebo že Biobran MGN-3 blokuje cestu
k histotoxicite na úrovni cieľových buniek.
Sudo N., Kubo C. (Univerzita v Kjúšú, JAPONSKO) : The Japanese Journal of Clinical and
Experimental Medicine (Japonský časopis pre klinickú a experimentálnu medicínu), Zv.78, 1,
2001
(c) Redukcia úbytku telesnej hmotnosti u myší po podaní Cisplatiny vďaka prípravku Biobran
MGN-3.
Pri liečbe rakoviny, lieky obsahujúce platinu často spôsobujú závažné vedľajšie účinky, ako
sú nevoľnosť, zvracanie, nefropatia a hypomagneziémia, vyvolané poškodením obličkových
tubulov (Lajer & Dangaard 1999), ďalej tiež dochádza k strate sluchu, periférnej neuropatii
a k myelosupresii, čo je jeden z najdevastačnejších vedľajších účinkov (Prestayko a kol.
1979), ktorý vedie k oslabeniu imunity. Akékoľvek obmedzenie vedľajších účinkov cisplatiny
je preto veľmi cenné a žiaduce. V rámci našich snáh sme študovali vplyv prípravku Biobran
MGN-3 na zmierňovanie úbytku hmotnosti u myší, ktorým bola podávaná maximálna tolerovateľná
dávka cisplatiny.
Týždeň pred podávaním cisplatiny, sme u dvoch skupín myší začali s podávaním prípravku
Biobran MGN-3 v dávkach 10 mg/ml (sušiny) vo vode, resp. intraperitoneálnou injekciou v
objeme 0,1 ml, kde bola ekvivalentná dávka prípravku rozpustená vo fosfátovom fyziologickom
roztoku (PBS). Dávka 1 mg na jedinca bola odvodená od odporúčanej ľudskej dávky (50 mg/kg).
Cisplatina v množstve 15 mg/kg bola podaná intraperitoneálne v 0,1 ml fosfátového pufru
(PBS) s obsahom 0,5 % kyseliny dimerkaptojantárovej (DMSO) ako nosiča. Dve skupiny myší
dostali sondou vodu, resp. intraperitoneálne PBS a po týždni bola obom podaná cisplatina.
K úbytku telesnej hmotnosti došlo hneď na ďalší deň po intraperitoneálnom injekčnom podaní
cisplatiny v oboch skupinách, v skupinách s prípravkom Biobran MGN-3 aj bez neho. Najväčší
úbytok bol v oboch skupinách pozorovaný na 5. deň po podaní cisplatiny, taktiež v oboch
skupinách, s prípravkom Biobran aj bez neho, a s prípravkom podávaným orálne aj
intraperitoneálne. Najväčší úbytok telesnej hmotnosti bol zaznamenaný u myší, ktorý bola
podaná cisplatina bez prípravku Biobran MGN-3. Hoci úbytok telesnej hmotnosti u myší, ktorým
bol podávaný Biobran MGN-3 sa blížil k 20 percentám pozorovaným u myší zo skupín, kde bola
podaná cisplatina bez Biobranu MGN-3, treba skonštatovať, že z onej skupiny žiadna myš
nezdochla, ani nemala hnačku či krvavú stolicu, čo sú vedľajšie účinky, ktoré spravidla
sprevádzajú podanie cisplatiny. Vo fáze rekonvalescencie, v porovnaní so skupinami, kde
nebol podávaný Biobran MGN-3, myši zo skupín s prípravkom Biobran naberali hmotnosť
rýchlejšie.
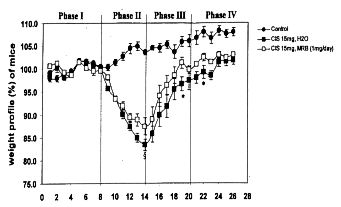 10 Legenda: hmotnostný profil myší (v %)
10 Legenda: hmotnostný profil myší (v %)
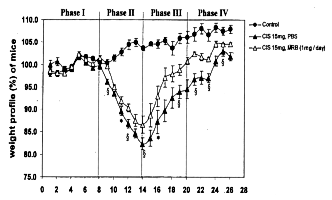 Obr. 11
Obr. 11
Endo Y., Kanbayashi H. (Univerzita Mac Master, KANADA) : Pharmacology and Toxicology
(Farmakológia a toxikológia), 2003
(d) Vplyv prípravku Biobran MGN-3 na cisplatinou a adriamycinom indukovanú toxicitu u
potkanov
Biobran MGN-3 je derivát z ryžových otrúb, vyrábaný čiastočnou hydrolýzou vo vode
rozpustných frakcií ryžovej vlákniny karbohydrázami z huby lentinus edodes [Č. patentu v USA
5560914]. Bolo preukázané, že Biobran MGN-3 je modifikátorom biologickej odozvy,
spôsobujúcim u pacientov s oslabenou imunitou nárast NK-bunkovej aktivity [Int. J.
Immunother. 14 (1) 1998].
Cieľ: Dennou administráciou prípravku Biobran MGN-3 v množstve 5,
resp. 50 mg/kg predísť závažným patologickým zmenám a úbytku hmotnosti súvisiacim s podaním
jedinej dávky cisplatiny (CIS), resp. adriamycinu (ADR). Po 13-dňovej aklimatizácii boli do
testu na základe telesnej hmotnosti vybraní samčí jedinci potkana kmeňa Spaque-Dawley, ktorí
boli rozdelení do ôsmych 10-členných skupín (dávky sú uvedené v mg/ml):
-
Biobran 5 mg p.o. + nosič i.p.
-
Biobran 50 mg p.o. + nosič i.p.
-
Kontrolná skupina p.o. + CIS 8 mg i.p.
-
Biobran 5 mg p.o. + CIS 8 mg i.p.
-
Biobran 50 mg p.o. + CIS 8 mg i.p.
-
Kontrolná skupina p.o. + ADR 10 mg i.p.
-
Biobran 5 mg p.o. + ADR 10 mg i.p.
-
Biobran 50 mg p.o. + ADR 10 mg i.p.
Potkanom bol perorálne (p.o.) podávaný prípravok Biobran MGN-3 (rozpustený v destilovanej
vode), resp. nosič denne po dobu 11 dní. Chemoterapeutikum, resp. nosič boli každému
z testovaných jedincov podané v jedinej intraperitoneálnej (i.p.) injekčnej dávke na 3. deň.
Po celých 11 dní boli u potkanov denne sledované klinické príznaky. Telesná hmotnosť bola
zaznamenávaná každý druhý deň. Na 11. deň boli zvieratá usmrtené inhaláciou CO2 a bola
vykonaná pitva. Boli vizuálne skontrolované hlavné orgány a zaznamenané poškodenia
gastrointestinálneho traktu.
Výsledky: Medzi 7. a 11. dňom došlo k úhynu piatich potkanov z 3. skupiny,
troch z 5. skupiny a jedného zo 4. skupiny. Potkany, ktorým bol podávaný výlučne Biobran
MGN-3 v množstve 5 alebo 50 mg/kg p.o. vykázali štatisticky významný nárast hmotnosti
(+72%). Potkany, ktoré dostali iba CIS alebo ADR samotné vykázali malý hmotnostný prírastok
(-1,5% u CIS a +30% u ADR). Potkany, ktoré dostávali Biobran MGN-3 v množstve 5 alebo 50 mg
plus CIS alebo ADR vykázali významne väčší hmotnostný prírastok než potkany z čisto
chemoterapeutickej skupiny (+11% v skupine Biobran MGN-3 5 mg + CIS a +46% v skupine + ADR).
V skupine Biobran MGN-3 50 mg + CIS bol hmotnostný prírastok +44% a v skupine Biobran MGN-3
50 mg + ADR +43%. Preživšie potkany, ktorým bol podávaný Biobran MGN-3 vyzerali v porovnaní
s potkanmi, ktoré dostali len CIS alebo ADR bez prípravku Biobran MGN-3 zdravšie, pribrali
a bol u nich pozorovaný nižší výskyt závažných intestinálnych patológií.
Tabuľka 4: Účinok prípravku Biobran na úbytok telesnej hmotnosti
indukovaný cisplatinou a doxorubicínom
| Terapia(všetko intraperitoneálne) |
Deň 0 |
Deň 3 |
Deň 5 |
Deň 7 |
Deň 9 |
Deň 11 |
5mg/kg p.o. + nosič
50mg/kg p.o. +nosič
Kontrolná skupina p.o.+ Cp8mg/kg
5mg/kg p.o. + Cp8mg/kg
50mg/kg p.o. + Cp8mg/kg
Kontrolná skupina p.o. + Dx10mg/kg
5mgn/kg p.o. + Dx10mg/kg
50mg/kg p.o. + Dx10mg/kg
|
100
100
103
99
101
103
101
101
|
100
98
101
99
99
100
100
101
|
100
100
82
85
92
88
92
92
|
100
97
69
76
90
82
89
87
|
100
97
55
68
85
77
86
85
|
100
97
57
65
84
76
85
83 |
p.o.- perorálne, Dx-doxorubicín, Cp-cisplatina
Jacoby H. I. (USA) : Journal of Nuturaceuticals, Function & Medical Foods (Časopis pre
naturaceutíka a funkčné a zdravotné potraviny), Zv.3 (4) 2001
(e) Efekt prípravku Biobran MGN-3 na toxicitu indukovanú rádioterapiou u myší
Táto štúdia mala za cieľ preskúmať modifikačný účinok prípravku Biobran MGN-3 na
rádiosenzitivitu prejavujúcu sa úbytkom kostnej drene spôsobeným celkovým ožiarením
organizmu. V snahe zohľadniť prípadnú klinickú aplikovateľnosť, autori otestovali účinky
kvantitatívne naprieč celým spektrom ožarovacích dávok od 4,5 po 8,5 Gy.
Pokusom boli podrobené 4-, resp. 5-týždňové samce myši kmeňa SPF BALB/c (skupina F2). Vo
vybraných skupinách bol zvieratám do stravy pridaný prípravok MGN-3 v množstve 50 mg/kg
telesnej hmotnosti. Skupiny pozostávali z 10 až 50 jedincov. Po dvoch dňoch aklimatizácie
bol myšiam z testovanej skupiny (F2) pridaný do stravy Biobran MGN-3. Po 8, resp. 15 dňoch
podávania prípravku Biobran MGN-3 boli jedince vystavené ožiareniu. Následne bola 3-krát
týždenne kontrolovaná ich telesná hmotnosť a každodenne sledovaný úhyn. V niektorých
prípadoch v rámci experimentu bol Biobran MGN-3 myšiam podávaný celé dva týždne pred
ožiarením, v iných sa s jeho podávaním začalo až po ožiarení.
Hoci v skupine F2 bol úhyn myší v dôsledku úbytku kostnej drene pozorovaný už od siedmeho
dňa po ožiarení, myši zo skupín, kde bol podávaný Biobran MGN-3 mali tendenciu podliehať
ožiareniu o čosi neskoršie. Dávka LD50 (spôsobujúca úhyn aspoň polovice ožiarených zvierat)
bola zhruba 5,15 Gy, pričom DRF (faktor redukujúci dávku) bol približne na úrovni 1,14.
Pokiaľ ide o telesnú hmotnosť, v skupinách Biobran MGN-3 bola pozorovaná tendencia
k udržaniu vyššej hmotnosti. Efekt skoršieho začatia s administráciou prípravku Biobran
MGN-3 naznačuje, že je vhodnejšie začať s užívaním tohto prípravku ešte pred ožarovaním.
Dávka ožiarenia myší v strede organizmu bola vyrátaná ako 1,21-násobok vyššie uvedených
dávok, čo znamená, že dávka LD50 pre jedincov v kontrolnej skupine bola na úrovni 6,23 Gy.
Aj keď rádioprotektívny efekt (DRF) Biobranu (ktorý bol 1,14) nebol príliš vysoký, treba
dodať, že v rámci celej štúdie neboli pozorované žiadne vedľajšie účinky.
Nakatugawa S. (Univerzita v Nagoji, JAPONSKO) : The Report of Nagoya Univ. (Správa
z Nagojskej univerzity), 2003
(f) Efekt prípravku Biobran MGN-3 na experimentálne vyvolanú dysfunkciu pečene u potkanov
V tejto štúdii bol skúmaný účinok prípravku Biobran MGN-3 na dysfunkciu pečene. Konkrétne
bol skúmaný účinok prípravku na rozvoj experimentálne, v dôsledku podania galaktozamínu
(GaIN) a acetaminofenu (AAP), vyvolanej dysfunkcie pečenie. GaIN bol podaný v experimentoch
č. 1 až 3 a AAP v experimentoch 4 a 5.
V experimente č. 1 bol potkanom intraperitoneálne podaný prípravok Biobran MGN-3 v rôznych
koncentráciách a po 1 hodine im bol do tela vpravený GaIN v množstve 800 mg/kg.
V experimente č. 2 bol orálne podávaný nefrakcionovaný Biobran MGN-3, a intraperitoneálne
boli podávané jeho frakcie s vysokou, resp. nízkou molekulárnou hmotnosťou. Po 1 hodine bol
do organizmov potkanov vpravený GaIN v množstve 800 mg/kg.
V experimente č. 3 bol Biobran MGN-3 podaný intraperitoneálne po tom, čo bol predtým
zahriaty, hydrolyzovaný a prefiltrovaný iontomeničovou živicou. Po 1 hodine bol potkanom
vpravený GaIN v množstve 800 mg/kg.
V experimente č. 4 bol Biobran MGN-3 podaný intraperitoneálne aj orálne a po 1 hodine bol do
organizmov potkanov vpravený AAP v množstve 700 mg/kg.
V experimente č. 5 bol Biobran MGN-3 podaný intraperitoneálne po tom, čo bol najprv
zahriaty, hydrolyzovaný a prefiltrovaný iontomeničovou živicou. Po 1 hodine bol vpravený AAP
v množstve 500 mg/kg.
Vo všetkých experimentoch boli potkany po 24 hodinách od podania GaIN, resp. AAP utratené
a boli stanovené hodnoty sérovej transaminázy (GOT, GPT).
Výsledky
Experiment 1: Vo všetkých skupinách, kde bol podaný Biobran MGN-3, bola
aktivita sérovej GOT a GPT, vyvolaná GaIN-indukovanou dysfunkciou pečene, v porovnaní
s aktivitou nameranou v kontrolnej skupine, významne potlačená. Supresívny účinok prípravku
Biobran MGN-3 na GaIN-indukovanú dysfunkciu pečene vyvrcholil pri dávke 20 mg/kg a pri
vyšších dávkach prípravku Biobran MGN-3 sa už ďalej nezvyšoval.
Experiment 2: Vo všetkých skupinách, kde bol podaný Biobran MGN-3, či už
nefrakcionovaný, alebo frakcionovaný a s vyššou alebo nižšou molekulárnou hmotnosťou, boli
nárasty aktivity sérovej GPT v dôsledku dysfunkcie pečene indukovanej GaIN, v porovnaní
s nárastmi v kontrolnej skupine, výrazne potlačené. Supresívne účinky frakcionovaného
a nefrakcionovaného prípravku Biobran MGN-3 boli podobné.
Experiment 3: V skupinách, kde bol podaný hydrolyzovaný Biobran MGN-3 boli
nárasty aktivity sérovej GOT v dôsledku dysfunkcie pečene indukovanej GaIN v porovnaní
s nárastmi v kontrolnej skupine výrazne potlačené.
Experiment 4: V skupinách, kde bol Biobran MGN-3 podaný intraperitoneálne
aj orálne boli nárasty aktivity sérovej GOT v dôsledku dysfunkcie pečene indukovanej AAP
v porovnaní s nárastmi v kontrolnej skupine výrazne potlačené.
Experiment 5: Podobné výsledky ako pri experimente č. 3 boli
s hydrolyzovaným Biobranom MGN-3 dosiahnuté aj po podaní AAP. V skupinách, kde bol podaný
hydrolyzovaný Biobran MGN-3 boli nárasty aktivity sérovej GOT v porovnaní s nárastmi v
kontrolnej skupine výrazne potlačené.
Potvrdilo sa, že Biobran MGN-3 má supresívne účinky na dysfunkciu pečene indukovanú GaIN
alebo AAP. HCl aktívnu zložku prípravku, zdá sa, nehydrolyzuje.
Yamada T. (Univerzita v Čibe, JAPONSKO): Abstrakt zo 6. výročného stretnutia Japonského
združenia pre výskum potravinovej vlákniny, 2002
(g) Orálne užívanie prípravku Biobran MGN-3 zmierňuje syndróm bežného nachladnutia u starých
ľudí
U vysoko rizikových skupín, ako sú starí ľudia a deti, je dôležité dbať na protiinfekčné
preventívne opatrenia ako očkovanie proti chrípke a predovšetkým na opatrenia, ktoré môžu
zabrániť sekundárnej bakteriálnej infekcii. Keď boli prípady pneumónie získanej
z prostredia, ktoré sa rozvinuli zhoršením bežného nachladnutia skúmané z hľadiska veku,
zistilo sa, že riziko sekundárnej bakteriálnej infekcie je vyššie u starších ľudí vo veku
nad 75 rokov. Riziko sprievodného zápalu pľúc je tiež vyššie u starších pacientov
s neurologickými ochoreniami, u ktorých je vysoké riziko aspirácie. Z tohto dôvodu sme
podrobili výskumu klinický prínos prípravku Biobran MGN-3 ako prevencie proti rozvoju
bežného nachladnutia u starých ľudí, u ktorých je schopnosť imunitnej reakcie v dôsledku
rôznych faktorov znížená.
Spomedzi klientov v starostlivosti zdravotného strediska „Atreyu Uozaki“ v Kobe, prefektúra
Hjógó, bola v období január až marec 2002 vybraná skupina starších klientov, ktorí netrpeli
žiadnym vážnym onemocnením a súhlasili s účasťou v štúdii. Testovaný bol potravinový
doplnok, frakcia prípravku Biobran MGN-3 (HRB) a v kontrolnej skupine bola použitá ryžová
vláknina obsahujúca predovšetkým vo vode rozpustné súčasti (RB).
Pokiaľ ide o symptómy nachladnutia (horúčka, bolesť hlavy, únava, triaška, kašeľ,
zahlienenie, výtok z nosa, upchatý nos, boľavé hrdlo, bolesť v hrudi), rátal sa počet dní,
počas ktorých sa prejavoval hoci len jediný z nich. Každý symptóm bol označený skóre
v závislosti od svojej intenzity (neprejavoval sa = 0, prejavoval sa mierne = 1, stredne =
2, výrazne = 3) a následne, vydelením celkového skóre každého pacienta počtom dní príjmu
testovanej látky bolo vyrátané jeho „symptomatické skóre nachladnutia“.
Výsledky: Spomedzi jednotlivých symptómov sa „kašeľ“, „únava“, „horúčka“
a „boľavé hrdlo“ na začiatku liečby prejavovali v oboch skupinách vo vysokej miere.
V skupine HRB bol celkový počet dní, v ktorých sa symptómy prejavovali, oproti skupine RB,
menší. V skupine RB bolo celkovo zaznamenané vyššie symptomatické skóre nachladnutia.
A hoci skóre „nosových symptómov“ bolo v skupine RB nižšie, skóre ostatných bežných
symptómov, ako sú „kašeľ“, „únava“ a „horúčka“, bolo vyššie. Dospelo sa preto k záveru, že
symptómy bežného nachladnutia prevládali v menšej miere v skupine HRB.
Štúdia preukázala, že pri orálnom podávaní HRB starším pacientom s bežným nachladnutím sa
vďaka imunostimulačnému pôsobeniu extraktu čas symptomatických prejavov skrátil, symptómy sa
nezhoršovali a bola znížená potreba symptomatickej liečby.
Tazawa K. (Lekárska a farmaceutická univerzita v Tojame, JAPONSKO) : Žurnál tradičnej
medicíny, 20 (3), 2003
3.7. Protialergické pôsobenie
(a) Hodnotenie preventívneho pôsobenia prípravku Biobran MGN-3 a zmierňovania symptómov
astmy v myšacom astmatickom modeli
V rámci tejto štúdie bolo sledované preventívne pôsobenie prípravku Biobran MGN-3
a zmierňovanie symptómov astmy na myšacom modeli astmy indukovanej toluén diizokyanátom
(TDI).
Na začiatku bol vyrobený roztok pitnej vody a prípravku Biobran MGN-3 v koncentrácii 2
g/liter a ten bol podávaný myšiam (samiciam kmeňa BALB/c), rozdeleným do 4 skupín (A-D):
Skupina A: Biobran MGN-3 bol podávaný mesiac pred, potom počas
senzitivizačnej fázy TDI a ďalej počas nasledujúceho obdobia.
Skupina B: Biobran MGN-3 bol podávaný mesiac pred a potom do skončenia
senzitivizačnej fázy TDI.
Skupina C:Biobran MGN-3 bol podávaný len počas senzitivizačnej fázy TDI.
Skupina D: Kontrolná skupina.
V skupine B bolo hodnotené preventívne pôsobenie a v skupine C efekt zmierňovania symptómov.
Účinok prípravku Biobran bol hodnotený podľa krvných koncentrácií histamínu, počtu
eozinofilov vo výplachu pľúcneho parenchýmu (BALF), aplikačného testu TDI z ušnice a hodnôt
typovo špecifických protilátok IgG1, IgG2a, IgE v krvi počas senzitivizácie.
Najvyššie koncentrácie krvného histamínu boli namerané 7 minút po podaní TDI a boli
nasledovné: skupina A: 2.5±0.53, skupina B: 4.2±0.75, skupina C: 4.3±7.8, skupina D:
6.4±0.87 (ng/ml), čiže v skupinách, kde bol podávaný Biobran MGN-3 boli oproti kontrolnej
skupine vykázané významne nižšie hodnoty. Pri testovaní senzitivity pri rôznych
koncentráciách TDI (0,01-10%) došlo v skupinách, kde bol podávaný Biobran MGN-3 až
k 10-100-násobného zníženiu senzibilnosti oproti kontrolnej skupine. Okrem toho, v skupinách
Biobran MGN-3 boli zistené podstatne nižšie množstvá eozinofilov v BALF a tiež nižšie
hodnoty v aplikačnom teste TDI. Naproti tomu, v hodnotách krvných protilátok neboli medzi
jednotlivými skupinami zaznamenané žiadne významné rozdiely.
Záverečné konštatovanie znie, že podávanie prípravku Biobran MGN-3 pôsobí preukázateľne
preventívne a zmierňuje symptómy astmy v myšacom modeli astmy indukovanej toluén
diizokyanátom (TDI). Štúdia tiež naznačuje, že Biobran MGN-3 nemá vplyv na tvorbu protilátok
typu IgG1 alebo IgE, indukovanú Th2, a že prípravok funguje ako supresívny faktor voči
žírnym bunkám.
Kobayashi H., Endo Y. (Univerzita Mc Master, KANADA) : Abstrakt z 52. výročného stretnutia
Japonskej spoločnosti alergiológov, 2002
(b) Inhibičné pôsobenie prípravku Biobran MGN-3 na progresiu atopickej dermatitídy u myší NC
V tejto štúdii bolo skúmané imunoregulačné pôsobenie prípravku Biobran MGN-3 na myši NC,
u ktorých sa prirodzene rozvíja zvýšená hladina IgE v sére a v reakcii na senzitivizáciu
ovalbumínom (OVA) sa u nich rozvíjajú kožné lézie podobné dermatitíde. Biobran MGN-3 bol
podávaný orálne piatim jedincom myši NC, ktoré boli potom porovnávané s kontrolnou skupinou
bez prípravku Biobran MGN-3. Myši boli následne senzitivizované ovalbumínom. Krvné vzorky
boli brané čo dvojtýždenne pred a po senzitivizácii. Množstvá celkových IgE, ako aj OVA
špecifických IgE v sérach, stanovené testom ELISA, boli u myší liečených prípravkom Biobran
MGN-3 v porovnaní s jedincami z kontrolnej skupiny výrazne nižšie. Okrem toho, kým
u jedincov NC, ktorým nebol podávaný Biobran MGN-3 sa rozvinuli kožné lézie podobné
atopickej dermatitíde, u myší NC liečených prípravkom Biobran MGN-3 sa u piatich jedincov
z piatich tieto lézie nerozvinuli. Záverom bolo konštatované, že Biobran MGN-3 pôsobí
inhibične na progresiu atopickej dermatitídy u myší NC.
Nonoyama S. (Tokijská univerzita medicíny a zubného lekárstva., JAPONSKO) : Abstrakt z 11.
výročného stretnutia Medzinárodného kongresu imunológov, 2001
© Autorské práva 2003: Hiroaki Maeda / Daiwa Pharmaceutical
(Vďaka za povolenie publikovať tento článok na stránkach Biobran.org.)
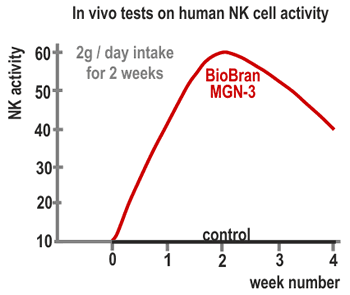 Legenda: Aktivita NK buniek > Príjem 2 g denne počas 2 týždňov / skupina BioBran MGN-3 /
kontrolná skupina / počet týždňov
Legenda: Aktivita NK buniek > Príjem 2 g denne počas 2 týždňov / skupina BioBran MGN-3 /
kontrolná skupina / počet týždňov
 Vedúcim výskumu prípravku
Biobran je Dr. Mamdooh Ghoneum, profesor na katedre imunológie Lekárskej a prírodovednej
univerzity Charlesa R. Drewa v Spojených štátoch. Dr. Ghoneum, v súčasnosti medzinárodne
uznávaná kapacita v oblasti imunoterapeutického prístupu k liečbe rakoviny, získal PhD.
z rádioimunológie na Tokijskej univerzite a odvtedy sa venuje práci v oblasti imunológie
na Kalifornskej univerzite v Los Angeles. Za uplynulých 20 rokov skúmal rozličné látky,
ktoré dokážu zlepšovať funkčnosť imunitného systému a podľa jeho slov Biobran MGN-3 je
najpotentnejší imunokomplex, aký kedy testoval. Výsledky ho natoľko ohúrili, že
v súčasnosti venuje celú svoju vedeckú pozornosť liečbe pomocou tejto zlúčeniny.
Vedúcim výskumu prípravku
Biobran je Dr. Mamdooh Ghoneum, profesor na katedre imunológie Lekárskej a prírodovednej
univerzity Charlesa R. Drewa v Spojených štátoch. Dr. Ghoneum, v súčasnosti medzinárodne
uznávaná kapacita v oblasti imunoterapeutického prístupu k liečbe rakoviny, získal PhD.
z rádioimunológie na Tokijskej univerzite a odvtedy sa venuje práci v oblasti imunológie
na Kalifornskej univerzite v Los Angeles. Za uplynulých 20 rokov skúmal rozličné látky,
ktoré dokážu zlepšovať funkčnosť imunitného systému a podľa jeho slov Biobran MGN-3 je
najpotentnejší imunokomplex, aký kedy testoval. Výsledky ho natoľko ohúrili, že
v súčasnosti venuje celú svoju vedeckú pozornosť liečbe pomocou tejto zlúčeniny.
 Legenda: Aktivita NK buniek > Koncentrácia MGN-3 (µg/ml)
Legenda: Aktivita NK buniek > Koncentrácia MGN-3 (µg/ml)
 Legenda: Aktivita NK buniek (%) > Koncentrácia prípravku BioBran MGN-3
Legenda: Aktivita NK buniek (%) > Koncentrácia prípravku BioBran MGN-3

 Obr. 5: Percentuálny podiel formovania väzieb medzi prirodzenými zabíjačmi
(NK bunkami)
a cieľovými bunkami K562. Legenda: % väzieb > Pred užívaním > Po užívaní
Obr. 5: Percentuálny podiel formovania väzieb medzi prirodzenými zabíjačmi
(NK bunkami)
a cieľovými bunkami K562. Legenda: % väzieb > Pred užívaním > Po užívaní
 Obr. 6: Smrtiace formácie NK buniek a cieľových nádorových buniek.
Obr. 6: Smrtiace formácie NK buniek a cieľových nádorových buniek.
 Obr. 7: Myšacie peritoneálne makrofágy (C3H/He)
Obr. 7: Myšacie peritoneálne makrofágy (C3H/He)

 10 Legenda: hmotnostný profil myší (v %)
10 Legenda: hmotnostný profil myší (v %)
 Obr. 11
Obr. 11